Триамифос
 | |
| Имена | |
|---|---|
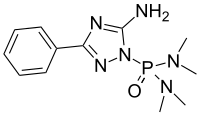
| Предпочтительное название ИЮПАК P- (5-амино-3-фенил- 1H- 1,2,4-триазол-1-ил) -N , N , N ′, N′ -тетраметилфосфоновый диамид | |
Другие имена
| |
| Идентификаторы | |
| |
3D модель ( JSmol ) |
|
| ChemSpider |
|
| Информационная карта ECHA | 100.149.164 |
| Номер ЕС |
|
CID PubChem |
|
| УНИИ | |
Панель инструментов CompTox ( EPA ) |
|
| |
| |
| Характеристики | |
| С 12 Н 19 Н 6 О П | |
| Молярная масса | 294,299 г·моль −1 |
| Появление | белый порошок |
| 0,25 г/л | |
| Опасности | |
| Маркировка СГС : | |
 | |
| Опасность | |
| Н300 , Н310 | |
| Р262 , Р264 , Р270 , Р280 , Р301+Р310 , Р302+Р350 , Р310 , Р321 , Р322 , Р330 , Р361 , Р363 , Р405 , Р501 | |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |
Триамифос ( химическая формула : C12H19N6OP ) — органофосфат, используемый в качестве пестицида и фунгицида . Он используется для борьбы с мучнистой росой на яблонях и декоративных растениях. Он был снят с производства производителем в США в 1998 году . [ 1 ]
История
Фосфорамид триамифос считается первым коммерчески доступным системным фунгицидом . [2] Несмотря на его активное использование в годы после его открытия , долгосрочные исследования токсичности не проводились до 1974 года. [3] Кроме того, с тех пор его заменили другие пестициды . Рекомендованная ВОЗ классификация пестицидов по степени опасности рассматривает триамифос как подлежащий прекращению использования в качестве пестицида. [4]
Структура и реакционная способность
Он классифицируется как фосфорорганическое соединение O=P(R)3 и, более конкретно, как фосфорамид O=P(NR2)3. Бис(диметиламидо)фосфорильная группа (Me2N)2-P(O)- присутствует в триамифосе, а также в ряде других фунгицидов. [2]
Он содержит две химические группы, используемые в синтезе пестицидов (триазол, фосфорил). Наиболее значимыми отдельными подчастями молекулы являются оксоновый центр (O=P) и уходящая группа (ароматическая группа триазола). Триамифос технически не является органофосфатом O=P(OR)3, подклассом фосфорорганических соединений O=PR3. Однако это различие не всегда последовательно в литературе, где фосфорорганические соединения без алкокси-боковых цепей или даже с группой O=S вместо группы O=P по-прежнему классифицируются как фосфорорганические пестициды (OP). [5] [6]
Schradan , другой фосфорорганический пестицид, можно рассматривать как аналог триамифоса, отличающийся только уходящей группой. Поскольку оба имеют сопоставимые токсические свойства, можно сделать вывод, что фениламинотриазольная часть триамифоса, по-видимому, не является жизненно важной для его антихолинэстеразного свойства. [3]
Синтез
Триамифос был впервые синтезирован Ван ден Босом и др. (1960) путем добавления соли 3-амино-5-фенил-1,2,4-триазола к раствору фосфорилхлорида . Затем в реакционную смесь вводят газообразный диметиламин для получения триамифоса. [7]
Биотрансформация
Исследований по точному определению пути биотрансформации и структуры активного метаболита триамифоса не проводилось.
Механизм действия и токсичность в исследованиях на животных
Токсическое действие триамифоса связано со способностью его активного метаболита ингибировать ацетилхолинэстеразу . [8] [9] Этот ингибирующий эффект наблюдается при всасывании через кожу, дыхательные пути или пищеварительный тракт. [10]
Национальный институт общественного здравоохранения в Нидерландах сообщил о дозозависимом эффекте триамифоса в краткосрочном исследовании на крысах. Они обнаружили ингибирование активности ацетилхолинэстеразы при концентрации 1 ppm в период кормления. После периода восстановления активность фермента вернулась к норме. [11] Однако долгосрочное кормление и исследование воспроизводства трех поколений, проведенное Verschuuren et al. (1974), обнаружили ингибирующие эффекты при еще более низкой концентрации 0,5 ppm. При этой концентрации активность холинэстеразы была ингибирована в поколениях P-, но не в поколениях F1, F2 или F3. Ингибирование во всех поколениях наблюдалось при концентрации 2,5 ppm, при которой последующие поколения уже подвергались воздействию токсиканта с момента зачатия. [3]
В обоих исследованиях сообщалось о неэффективной концентрации 0,1 ppm. [3] [11]
Кроме того, сообщалось о большем ингибирующем эффекте на холинэстеразу эритроцитов по сравнению с активностью холинэстеразы плазмы или мозга . [3] Таким образом, активный метаболит, по-видимому, не легко проникает в мозг, и в первую очередь наблюдаются мускариновые и никотиновые эффекты. [8] Было определено, что LD50 (внутрибрюшинный путь) составляет от 15 до 18 мг/кг у крыс и от 10 до 30 мг/кг у мышей. [3] [8] [12] Сообщалось, что животные, получившие летальную дозу, сохраняли активность при введении атропина в качестве антидота. [8] Важным фактором, ответственным за острую токсичность триамифоса, является скорость ингибирования холинэстеразы: если активность снижается на 70% в течение нескольких минут, сообщалось о смерти, в первую очередь из-за паралича дыхательных мышц у крыс. Ингибированный фермент не реактивируется, и вышеупомянутое восстановление животных было возможно только благодаря его ресинтезу. [8] Исследование 1976 года предположило повышенное содержание холестерина в аорте крыс и изменения в липидном обмене веществ как дополнительные эффекты триамифоса, что, однако, не было подтверждено другим, более подробным исследованием. [13] [14] Обзор эффектов триамифоса в различных концентрациях можно найти в таблице ниже.
| Доза | Эффект |
|---|---|
| 0,1 частей на миллион | NOAEL (уровень отсутствия эффекта) [3] [11] |
| 0,5 частей на миллион | Ингибирующие эффекты в P-генерации [3] |
| 2,5 частей на миллион | Ингибирующие эффекты в P- и последующих поколениях [3] |
| 15–18 мг/кг | Пероральная LD50 у крыс [3] [8] |
| 10–30 мг/кг | Пероральная LD50 у мышей [12] |
Показания
Предполагается, что триамифос оказывает такое же токсическое побочное действие на человека, как и другие фосфорорганические пестициды , хотя данные о воздействии триамифоса на человека отсутствуют. [15]
Ссылки
- ^ "TRIAMIPHOS | CAMEO Chemicals | NOAA". cameochemicals.noaa.gov . Получено 2022-07-04 .
- ^ ab Mavrommatis, Christakis Nikou (ноябрь 1983 г.). Синтез, спектроскопия и фунгицидная активность амидов фосфорной кислоты (докторская диссертация). Политехнический институт Северного Лондона.
- ^ abcdefghij Verschuuren, HG; Kroes, R. (декабрь 1974 г.). «Триамифос: долгосрочная токсичность и исследования репродукции в трех поколениях у крыс». Токсикология . 2 (4): 327–338. doi :10.1016/0300-483X(74)90025-0. PMID 4855258.
- ^ Рекомендованная ВОЗ классификация пестицидов по степени опасности и руководящие принципы классификации 2019 г. Женева: ВОЗ . 2020 г. ISBN 978-92-4-000566-2.
- ^ Гани, Шахид Юсуф; Джаваид, Дарахшан; Хаджам, Юнис Ахмад; Реши, Мохд. Салим (30.04.2022). «Механизмы и стратегии лечения нейротоксичности, вызванной органофосфатными пестицидами у людей: критическая оценка». Токсикология . 472 : 153181. doi : 10.1016/j.tox.2022.153181. ISSN 0300-483X. PMID 35439576. S2CID 248220887.
- ^ Buchet, JP; Roels, H.; Lauwerys, R. (1974-01-16). «Дальнейшая характеристика моно- и диглицеридлипазы в тканях крыс». Life Sciences . 14 (2): 371–385. doi :10.1016/0024-3205(74)90068-X. ISSN 0024-3205. PMID 4360447.
- ^ ван ден Бос, Б.Г.; Купманс, МЮ; Хейсман, ХО (2 сентября 2010 г.). «Исследования пестицидных соединений фосфора I. Фунгициды, инсектициды и акарициды, полученные из 3-амино-1,2,4-триазола». Recueil des Travaux Chimiques des Pays-Bas . 79 (8): 807–822. дои : 10.1002/recl.19600790806.
- ^ abcdef Lauwerys, R.; Buchet, J. -P. (1971-11-01). «Исследования механизма токсичности фосфорорганического пестицида триамифоса». European Journal of Pharmacology . 16 (3): 361–366. doi :10.1016/0014-2999(71)90039-2. ISSN 0014-2999. PMID 5132563.
- ^ Kwong, Tai C. (февраль 2002 г.). «Органофосфатные пестициды: биохимия и клиническая токсикология». Терапевтический лекарственный мониторинг . 24 (1): 144–149. doi :10.1097/00007691-200202000-00022. ISSN 0163-4356. PMID 11805735. S2CID 22423462.
- ^ Спенсер, EY (1982). «Руководство по химикатам, используемым для защиты растений». Agriculture Canada . 165 .
- ^ abc Неопубликованные отчеты . Билтховен: RIVM . 1962.
- ^ ab Tolkmith, Henry (апрель 1966 г.). «Острая токсичность для млекопитающих и структура гетероциклических фосфорорганических соединений». Annals of the New York Academy of Sciences . 136 (3 Acute Mammali): 61–94. Bibcode : 1966NYASA.136...61T. doi : 10.1111/j.1749-6632.1966.tb31409.x. ISSN 0077-8923. S2CID 83584149.
- ^ Lauwerys, RR; Buchet, JP; Roels, H. (1976). «Связь между воздействием кадмия или его содержанием в организме и концентрацией кадмия в крови и моче человека». Международный архив охраны труда и окружающей среды . 36 (4): 275–285. Bibcode : 1976IAOEH..36..275L. doi : 10.1007/BF00409357. ISSN 0340-0131. PMID 1254345. S2CID 8988637.
- ^ Buchet, JP; Lauwerys, R.; Roels, H. (февраль 1977 г.). «Длительное воздействие фосфорорганических пестицидов и липидный метаболизм у крыс». Бюллетень загрязнения окружающей среды и токсикологии . 17 (2): 175–183. Bibcode : 1977BuECT..17..175B. doi : 10.1007/BF01685547. ISSN 0007-4861. PMID 66077. S2CID 13100142.
- ^ Барлоу, Сьюзан М.; Салливан, Фрэнк М.; Миллер, Ричард К. (2015-01-01), Шефер, Кристоф; Питерс, Пол; Миллер, Ричард К. (ред.), "2.23 - Профессиональные, промышленные и экологические агенты", Лекарственные препараты во время беременности и лактации (третье издание) , Сан-Диего: Academic Press, стр. 599–638, doi :10.1016/b978-0-12-408078-2.00024-x, ISBN 978-0-12-408078-2, получено 2023-03-18


