Тетраиодид теллура
 | |
| Имена | |
|---|---|
| Другие имена теллур(IV) иодид | |
| Идентификаторы | |
3D модель ( JSmol ) |
|
| ChemSpider |
|
| Информационная карта ECHA | 100.029.282 |
| Номер ЕС |
|
CID PubChem |
|
| УНИИ | |
Панель инструментов CompTox ( EPA ) |
|
| |
| |
| Характеристики | |
| ТеИ 4 | |
| Молярная масса | 635,218 г/моль |
| Появление | черные кристаллы |
| Плотность | 5,05 г/см 3 , твердый |
| Температура плавления | 280 °C (536 °F; 553 К) |
| Структура | |
| орторомбический | |
| Опасности | |
| Маркировка СГС : [1] | |
  | |
| Опасность | |
| Н302 , Н312 , Н314 , Н332 | |
| Р260 , Р261 , Р264 , Р270 , Р271 , Р280 , Р301+Р312 , Р301+Р330+Р331 , Р302+Р352 , Р303+Р361+Р353 , Р304+Р312 , Р304+Р340 , Р305+Р351+Р338 , Р310 , Р312 , Р322 , Р330 , Р363 , Р405 , Р501 | |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |
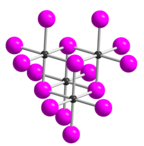
Тетраиодид теллура ( TeI4 ) — неорганическое химическое соединение . Он имеет тетрамерную структуру , которая отличается от тетрамерных твердых форм TeCl4 и TeBr4 . [2] В TeI4 атомы Te октаэдрически координированы, а ребра октаэдров являются общими. [ 2]
Подготовка
Тетраиодид теллура может быть получен путем взаимодействия Te и иодметана , CH3I . [ 2] В парах TeI4 диссоциирует : [3]
- ТеИ 4 → ТеИ 2 + И 2
Его также можно получить путем реакции теллуровой кислоты с иодистым водородом . [4]
- Te(OH) 6 + HI → TeI 4 + I 2 + 6 H 2 O
Его также можно получить путем реакции элементов, которые также могут давать дииодид теллура и моноиодид теллура , в зависимости от условий реакции: [5]
- Те + 2 И 2 → ТеИ 4
- ТеИ 4 → ТеИ 2 + И 2
Характеристики
Тетраиодид теллура — это железно-серое твердое вещество, которое медленно разлагается в холодной воде и быстро в теплой воде с образованием диоксида теллура и иодида водорода . [6] Он стабилен даже во влажном воздухе и разлагается при нагревании, выделяя иод. Он растворим в иодистоводородной кислоте с образованием H[TeI 5 ] и слабо растворим в ацетоне . [4]
Тетраиодид теллура является проводником в расплавленном состоянии, диссоциируя на ионы TeI 3 + и I − . В растворителях с донорными свойствами, таких как ацетонитрил , образуются ионные комплексы CH 3 CN, которые делают раствор проводящим: [3]
- TeI 4 + 2 CH 3 CN → (CH 3 CN) 2 TeI 3 + + I −
Известно пять модификаций тетраиодида теллура, все из которых состоят из тетрамерных молекул. [7] Форма δ является наиболее термодинамически стабильной формой. Она структурно получена (так же как и формы α, β и γ) из формы ε.
Ссылки
- ^ "Тетрайодид теллура". pubchem.ncbi.nlm.nih.gov . Получено 13 декабря 2021 г. .
- ^ abc Гринвуд, Норман Н .; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн . ISBN 978-0-08-037941-8.
- ^ ab Неорганическая химия , Эгон Виберг, Арнольд Фредерик Холлеман Elsevier 2001 ISBN 0-12-352651-5
- ^ ab Handbuch der Präparativen Organischen Chemie. 1 (3., umgearb. Aufl ed.). Штутгарт: Энке. 1975. с. 435. ИСБН 978-3-432-02328-1.
- ^ Хаген, AP (2009-09-17). Неорганические реакции и методы, Образование связей с галогенами (часть 1). John Wiley & Sons. ISBN 978-0-470-14538-8.
- ^ Иодид теллура (IV), 99% (в пересчете на металлы) в AlfaAesar, дата обращения 17.12.2013 (PDF) (требуется JavaScript). [ нерабочая ссылка ]
- ^ Ридель, Эрвин; Джаниак, Кристоф (2011). Anorganische Chemie: Zusatzmaterial онлайн . Студия (8-е изд.). Берлин: де Грюйтер. ISBN 978-3-11-022567-9.


