Гидросульфат рубидия
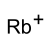 ион рубидия | |
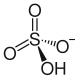 ион сульфата водорода | |
| Идентификаторы | |
|---|---|
| |
3D модель ( JSmol ) |
|
| ChemSpider |
|
| Информационная карта ECHA | 100.036.029 |
| Номер ЕС |
|
CID PubChem |
|
Панель инструментов CompTox ( EPA ) |
|
| |
| |
| Характеристики | |
| RbHSO4 | |
| Молярная масса | 182,54 г/моль −1 |
| Появление | Кристаллы без цвета [1] |
| Плотность | 2,89 г·см −3 |
| Температура плавления | 214 °C (417 °F; 487 К) [2] |
| Родственные соединения | |
Другие катионы | оксид рубидия гидроксид рубидия |
Родственные соединения | сульфат рубидия |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |
Гидросульфат рубидия , иногда называемый бисульфатом рубидия, является полунейтрализованной солью рубидия серной кислоты . Имеет формулу RbHSO4 .
Синтез
Его можно синтезировать с водой и стехиометрическим количеством дисульфата рубидия. Реакция происходит там, где нет влажности: [3]
Есть и другой метод создания. Он похож на синтез сульфата натрия и сульфата калия . Для этой реакции требуется хлорид рубидия и немного теплой серной кислоты. В ходе реакции также образуется некоторое количество хлористого водорода .
Характеристики
Это гигроскопичное соединение. Имеет моноклинную кристаллическую структуру, ее структура P2 1 /n. Размеры элементарной ячейки: a = 1440 пм, b = 462,2 пм, c = 1436 пм и β = 118,0°. Его кристаллы являются изоморфами с кристаллами гидросульфата аммония . [4]
Его стандартная энтальпия составляет −1166 кДж/моль. [5] При его растворении в воде выделяется 15,62 кДж/моль энергии. [6]
После нагревания разлагается на дисульфат рубидия и воду: [7]
Подобно калию и цезию , рубидий имеет еще одно соединение сульфата водорода: Rb 3 H(SO 4 ) 2 .
Ссылки
- ^ Жан Д'Анс, Эллен Лакс: Taschenbuch für Chemiker und Physiker. 3. Elemente, anorganische Verbindungen und Materialien, Minerale, Band 3. 4. Auflage, Springer, 1997, ISBN 978-3-5406-0035-0 , S. 692 ( Taschenbuch für Chemiker und Physiker , стр. 692, в Google Books ).
- ^ Р. Ферманн, С. Богосян, Х. Хамма-Кюни, Дж. Рогез: «Фазовые диаграммы, структурные и термодинамические свойства расплавленных солевых растворителей для промышленного катализатора окисления SO 2 » Аннотация
- ^ SB Rasmussen, H. Hamma, KM Eriksen, G. Hatem, M. Gaune-Escard, R. Fehrmann: "Физико-химические свойства и образование комплексов переходных металлов в расплавах щелочного пиросульфата и гидросульфата". VII Международная конференция по расплавленным шлакам, флюсам и солям, Южноафриканский институт горного дела и металлургии, 2004. Volltext (PDF; 661 кБ)
- ^ JP Ashmore, HE Petch: «Структура RbHSO 4 в параэлектрической фазе» в Can. J. Phys 1975 , 53 (24), S. 2694-2702. doi :10.1139/p75-328
- ^ LA Cowan, RM Morcos, N. Hatada, A. Navrotsky, SM Haile: "Высокотемпературные свойства Rb 3 H(SO 4 ) 2 при давлении окружающей среды: отсутствие полиморфного, суперпротонного перехода" в Solid State Ionics 2008 , 179 , S. 305-313. Volltext (PDF; 837 кБ)
- ^ М. де Форкран: «Sur les lorures et сульфаты рубидия и цезия» в Compt. Ренд. Hebd. 1906 , 143 , С. 98. Фоллтекст
- ^ Р. Абегг, Ф. Ауэрбах: «Справочник по неорганической химии». Верлаг С. Хирзель, Bd. 2, 1908. С. 432. Volltext.


