Римонабант
 | |
 | |
| Клинические данные | |
|---|---|
| AHFS / Drugs.com | Информация о лекарственных средствах для потребителей |
| Данные лицензии |
|
Категория беременности |
|
| Пути введения | Оральный |
| код АТС |
|
| Правовой статус | |
| Правовой статус |
|
| Фармакокинетические данные | |
| Биодоступность | Неопределенный |
| Связывание с белками | Почти 100% |
| Метаболизм | Печеночный , задействован CYP3A4 |
| Период полувыведения | Варьируется: от 6 до 9 дней при нормальном ИМТ, 16 дней, если ИМТ >30 |
| Выделение | Фекальный (86%) и почечный (3%) |
| Идентификаторы | |
| |
| Номер CAS | |
| CID PubChem |
|
| ИУФАР/БПС |
|
| DrugBank | |
| ChemSpider | |
| УНИИ | |
| КЕГГ | |
| ChEMBL | |
| Панель инструментов CompTox ( EPA ) |
|
| Информационная карта ECHA | 100.210.978 |
| Химические и физические данные | |
| Формула | С22Н21Cl3N4O |
| Молярная масса | 463,79 г·моль −1 |
| 3D модель ( JSmol ) |
|
| |
| (проверять) | |
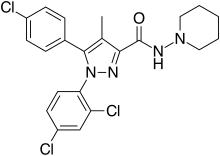
Римонабант (также известный как SR141716 ; торговые названия Acomplia , Zimulti ) [3] — аноректический препарат против ожирения, одобренный в Европе в 2006 году, но отозванный во всем мире в 2008 году из-за серьезных психиатрических побочных эффектов; он никогда не был одобрен в Соединенных Штатах. [1] [2] Римонабант — обратный агонист каннабиноидного рецептора CB 1 и был первым в своем классе для клинической разработки. [4] [5]
История
Римонабант — селективный блокатор рецепторов CB 1 , открытый и разработанный компанией Sanofi-Aventis . [6]
21 июня 2006 года Европейская комиссия одобрила продажу римонабанта в тогдашнем 25-членском Европейском союзе в качестве рецептурного препарата для использования в сочетании с диетой и физическими упражнениями для пациентов с индексом массы тела (ИМТ) более 30 кг/м 2 или пациентов с ИМТ более 27 кг/м 2 с сопутствующими факторами риска, такими как диабет 2 типа или дислипидемия . [7] Это был первый препарат в своем классе, одобренный где-либо в мире. [5]
Римонабант был подан в Управление по контролю за продуктами питания и лекарственными средствами (FDA) для одобрения в США в 2005 году; в 2007 году Консультативный комитет по эндокринным и метаболическим препаратам FDA (EMDAC) пришел к выводу, что Sanofi-Aventis не смогла продемонстрировать безопасность римонабанта, и проголосовал против рекомендации препарата против ожирения для одобрения. [8] Заявка была признана FDA не подлежащей одобрению , и компания отменила планы по повторной подаче. [9]
Препарат был одобрен в Бразилии в апреле 2007 года. [2]
В октябре 2008 года Европейское агентство по лекарственным средствам рекомендовало приостановить действие Acomplia после того, как Комитет по лекарственным средствам для человека (CHMP) определил, что риски Acomplia перевешивают его пользу из-за риска серьезных психиатрических проблем, включая самоубийство. [10] В ноябре 2008 года консультативный комитет в Бразилии также рекомендовал приостановить действие препарата, и в том же месяце Sanofi-Aventis приостановила продажу препарата по всему миру. [2] Одобрение EMA было отозвано в январе 2009 года . [11] [12] В 2009 году Индия запретила производство и продажу препарата. [13]
Побочные эффекты
Данные клинических испытаний, представленные в регулирующие органы, показали, что римонабант вызывал депрессивные расстройства или изменения настроения у 10% субъектов и суицидальные мысли примерно у 1%, а в Европе он был противопоказан людям с любыми психическими расстройствами, включая депрессивных или суицидальных людей. [7] Данные крупного рандомизированного клинического испытания (CRESCENDO) с участием > 9000 пациентов, получавших лечение римонабантом, продемонстрировали частоту психиатрических побочных эффектов (тревога, депрессия, подавленное настроение или бессонница) более 30%. [14]
Кроме того, тошнота и инфекции верхних дыхательных путей были очень распространенными побочными эффектами (встречались более чем у 10% людей); распространенные побочные эффекты (встречались у 1–10% людей) включали гастроэнтерит , беспокойство, раздражительность, бессонницу и другие нарушения сна, приливы, диарею, рвоту, сухость или зуд кожи, тендинит, мышечные спазмы и судороги, усталость, гриппоподобные симптомы и повышенный риск падений.
Консультативный комитет FDA согласился с опасениями, высказанными подразделениями по обзору. На основе данных, полученных от людей и животных, выяснилось, что терапевтическое окно в отношении токсичности для ЦНС, и в частности, судорог, было узким. [2] [15] [16]
Данные пострегистрационного наблюдения EMA показали, что риск психических расстройств у людей, принимающих римонабант, увеличился вдвое. [2]
Фармакология
Фармакодинамика
Римонабант является обратным агонистом каннабиноидного рецептора CB 1. Первоначально считалось, что он селективен для рецептора CB 1 , но впоследствии было обнаружено, что римонабант также действует как антагонист μ -опиоидного рецептора . [17]
Химия
Химический синтез римонабанта описывается следующим образом: [18] [ проверка не удалась ]
Исследовать
Наряду с клиническими испытаниями при ожирении, в ходе которых были получены данные, представленные в регулирующие органы, [19] римонабант также изучался в клинических испытаниях [2] при диабете, атеросклерозе и отказе от курения. [20] [21]
Смотрите также
- Дринабант — антагонист каннабиноидных рецепторов, разработанный для использования в рецептурных препаратах, вызывающих серьезные побочные эффекты со стороны психики.
Ссылки
- ^ ab Sam AH, Salem V, Ghatei MA (2011). «Римонабант: от RIO до запрета». Журнал ожирения . 2011 : 432607. doi : 10.1155/2011/432607 . PMC 3136184. PMID 21773005 .
- ^ abcdefg Морейра Ф.А., Криппа Дж.А. (июнь 2009 г.). «Психиатрические побочные эффекты римонабанта». Revista Brasileira de Psiquiatria . 31 (2): 145–153. дои : 10.1590/s1516-44462009000200012 . ПМИД 19578688.
- ^ "Римонабант". AdisInsight . Получено 21 февраля 2017 г. .
- ^ Fong TM, Heymsfield SB (сентябрь 2009 г.). «Обратные агонисты рецептора каннабиноида-1: современное понимание механизма действия и неотвеченные вопросы». International Journal of Obesity . 33 (9): 947–955. doi : 10.1038/ijo.2009.132 . PMID 19597516.
- ^ ab "Европейское одобрение препарата Санофи-Авентис Acomplia получено рано". IHS . 23 июня 2006 г.
- ^ Barth F, Rinaldi-Carmona M (август 1999). «Разработка антагонистов каннабиноидов». Current Medicinal Chemistry . 6 (8): 745–755. doi :10.2174/0929867306666220401143808. PMID 10469889. S2CID 247893317.
- ^ ab "Acomplia EPAR" (PDF) . EMA. 30 января 2009 г. Архивировано из оригинала (PDF) 22 февраля 2017 г. Получено 21 февраля 2017 г.Со страницы индекса EMA. Архивировано 22.02.2017 на Wayback Machine.
- ^ Saul S (14 июня 2007 г.). «FDA Panel Rejects Drug for Obesity» (Комитет FDA отклоняет препарат для лечения ожирения). The New York Times .
- ^ "Sanofi-Aventis Drops Application for Drug". The New York Times . 30 июня 2007 г.
- ^ "Европейское агентство по лекарственным средствам рекомендует приостановить действие разрешения на продажу препарата Acomplia". Европейское агентство по лекарственным средствам. 23 октября 2008 г. Получено 18 января 2016 г.
- ^ "Использование препаратов против ожирения приостановлено". BBC News . 23 октября 2008 г. Получено 4 марта 2010 г.
- ^ "Публичное заявление об отзыве разрешения на продажу препарата Acomplia (римонабант) в Европейском союзе" (PDF) . Европейское агентство по лекарственным средствам. 30 января 2009 г. Получено 18 января 2016 г.
- ^ "Лекарства, запрещенные в Индии". Центральная организация по контролю за стандартами лекарственных средств, Dte.GHS, Министерство здравоохранения и благополучия семьи, Правительство Индии. Архивировано из оригинала 22-02-2017 . Получено 17-09-2013 .
- ^ Topol EJ, Bousser MG, Fox KA, Creager MA, Despres JP, Easton JD и др. (август 2010 г.). «Римонабант для профилактики сердечно-сосудистых событий (CRESCENDO): рандомизированное, многоцентровое, плацебо-контролируемое исследование». Lancet . 376 (9740): 517–523. doi :10.1016/S0140-6736(10)60935-X. PMID 20709233. S2CID 36404292.
- ^ "Информационный документ FDA NDA 21-888 Таблетки Зимулти (римонабант), 20" (PDF) . FDA. 13 июня 2007 г.
- ^ Дэвис-Бруно К (13 июня 2007 г.). «Неклинический обзор: токсичность римонабанта для ЦНС». FDA, Отделение метаболизма и эндокринологии.
- ^ Seely KA, Brents LK, Franks LN, Rajasekaran M, Zimmerman SM, Fantegrossi WE, Prather PL (октябрь 2012 г.). «AM-251 и римонабант действуют как прямые антагонисты мю-опиоидных рецепторов: последствия для исследований взаимодействия опиоидов и каннабиноидов». Neuropharmacology . 63 (5): 905–915. doi :10.1016/j.neuropharm.2012.06.046. PMC 3408547 . PMID 22771770.
- ^ Yoshioka T, Fujita T, Kanai T, Aizawa Y, Kurumada T, Hasegawa K, Horikoshi H (февраль 1989). «Исследования затрудненных фенолов и аналогов. 1. Гиполипидемические и гипогликемические агенты со способностью ингибировать перекисное окисление липидов». Journal of Medicinal Chemistry . 32 (2): 421–428. doi :10.1021/jm00122a022. PMID 2913302.
- ^ Pi-Sunyer FX, Aronne LJ, Heshmati HM, Devin J, Rosenstock J (февраль 2006 г.). «Влияние римонабанта, блокатора рецепторов каннабиноида-1, на вес и кардиометаболические факторы риска у пациентов с избыточным весом или ожирением: Рио-Северная Америка: рандомизированное контролируемое исследование». JAMA . 295 (7): 761–775. doi : 10.1001/jama.295.7.761 . PMID 16478899.
- ^ Cahill K, Ussher MH (март 2011 г.). «Антагонисты рецепторов каннабиноидов типа 1 для прекращения курения». База данных систематических обзоров Cochrane . 2011 (3): CD005353. doi :10.1002/14651858.CD005353.pub4. PMC 6486173. PMID 21412887 .
- ^ Maldonado R, Valverde O, Berrendero F (апрель 2006 г.). «Участие эндоканнабиноидной системы в наркотической зависимости». Trends in Neurosciences . 29 (4): 225–232. doi :10.1016/j.tins.2006.01.008. PMID 16483675. S2CID 16125335.

