Комплекс переходных металлов-клещей

В химии комплекс переходного металла-пинцера представляет собой тип координационного комплекса с лигандом-пинцером. Лиганды-пинцеры представляют собой хелатирующие агенты , которые прочно связываются с тремя соседними копланарными участками в меридиональной конфигурации. [1] [2] Негибкость взаимодействия пинцера с металлом придает полученным комплексам высокую термическую стабильность. Эта стабильность отчасти объясняется ограниченной геометрией пинцера, которая ингибирует циклометаллирование органических заместителей на донорных участках на каждом конце. При отсутствии этого эффекта циклометаллирование часто является значительным процессом дезактивации для комплексов, в частности, ограничивая их способность влиять на активацию связи CH . Органические заместители также определяют гидрофобный карман вокруг реакционного координационного участка. Стехиометрические и каталитические применения комплексов-пинцеров изучаются ускоренными темпами с середины 1970-х годов. Большинство лигандов-пинцеров содержат фосфины . [3] Реакции комплексов металл-пинцет локализуются в трех местах, перпендикулярных плоскости лиганда-пинцет, хотя в некоторых случаях одна рука является полулабильной , а дополнительный координационный участок образуется временно. Ранние примеры лигандов-пинцет (первоначально так не называвшихся) были анионными с карбанионом в качестве центрального донорного участка и фланговыми донорами фосфина; эти соединения называются пинцетами PCP.
Область применения пинцетных лигандов
Хотя наиболее распространенный класс лигандов-пинцеров содержит наборы доноров PCP, были разработаны вариации, в которых фосфины заменены тиоэфирами и третичными аминами. Многие лиганды-пинцеры также содержат азотистые доноры в центральной координационной группе (см. рисунок), такие как пиридины . [4]

Легко приготовляемый пинцетный лиганд — POCOP . Многие типы тридентатных лигандов занимают три смежных копланарных координационных участка. Самый известный такой лиганд — терпиридин («терпи»). Терпи и его родственники не имеют стерической массы двух терминальных донорных участков, обнаруженных в традиционных пинцетных лигандах.
Металлические пинцетные комплексы часто получают путем активации связи CH . [5] [6]
Пинцерные комплексы Ni(II) N,N,N активны в реакциях сочетания Кумады , Соногаширы и Сузуки-Мияуры с неактивированными алкилгалогенидами. [7] [8]

Типы пинцетных лигандов
Пинцерный лиганд чаще всего является анионным, двухэлектронным донором металлического центра. Он состоит из жесткой плоской основной цепи, обычно состоящей из арильных каркасов, и имеет две нейтральные двухэлектронные донорные группы в мета-положениях. Общая формула для пинцерных лигандов - 2,6-(ER 2 ) 2 C 6 H 3 - сокращенно ECE - где E - двухэлектронный донор, а C - ипсо-углерод ароматической основной цепи (например, PCP - два фосфиновых донора). [9] Благодаря прочному тридентатному режиму координации он позволяет комплексам металлов проявлять высокую термическую стабильность, а также стабильность на воздухе. [5] Это также подразумевает, что для реакционной способности доступно уменьшенное количество координационных участков, что часто ограничивает количество нежелательных продуктов, образующихся в реакции из-за обмена лигандами, поскольку этот процесс подавляется.
Существуют различные типы пинцетных лигандов, которые используются в катализе переходных металлов . Часто они имеют тот же двухэлектронный донор, фланкирующий металлический центр, но это не является обязательным требованием.

Наиболее распространенные конструкции лигандов-пинцеров — PCP, NCN, PCN, SCS и PNO. Другие элементы, которые использовались в различных положениях в лиганде, — это бор , мышьяк , кремний и даже селен .
Изменяя свойства лигандов-пинцеров, можно значительно изменить химию в металлическом центре. Изменение твердости/мягкости донора, использование электроноакцепторных групп (EWG) в основной цепи и изменение стерических ограничений лигандов — все это методы, используемые для настройки реакционной способности в металлическом центре.
Синтез
Синтез лигандов часто включает реакцию между 1,3-дибромэтилбензолом и вторичным фосфином с последующей депротонизацией промежуточных соединений четвертичного фосфора для получения лиганда. [10]
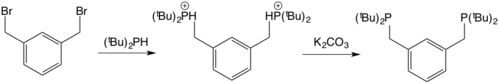
Для получения металлического комплекса используются два распространенных пути. Один из них — простое окислительное присоединение связи ipso-CX, где X = Br, I, к металлическому центру, часто M(0) (M = Pd, Mo, Fe, Ru, Ni, Pt), хотя могут быть использованы и другие доступные металлические комплексы с более высокими степенями окисления (например, Rh(COD)Cl 2 ). [11] [12]
Другим важным методом введения металла является активация связи CH . [5] Главное отличие заключается в том, что металл, используемый в этом методе, уже находится в более высокой степени окисления (например, виды PdCl2 – Pd(II)). Однако было обнаружено, что эти реакции протекают гораздо эффективнее при использовании комплексов металлов со слабосвязанными лигандами (например, Pd(BF4 ) 2 ( CH3CN ) 2 или Pd(OTf) 2 ( CH3CN ) 2 , где OTf = F3CO2SO− ) . [ 6 ]
Роль в катализе
Потенциальная ценность лигандов-пинцеров в катализе была исследована, хотя ни один процесс не был коммерциализирован. Желаемые приложения мотивированы высокой термической стабильностью и жесткостью. Недостатки включают стоимость лигандов.
Муфта Сузуки-Мияура

Было показано, что пинцетные комплексы катализируют реакции сочетания Сузуки-Мияуры — универсальную реакцию образования углерод-углеродной связи.
Типичное сочетание Сузуки использует катализаторы Pd(0) с монодентатными третичными фосфиновыми лигандами (например, Pd(PPh 3 ) 4 ). Это очень селективный метод соединения арильных заместителей вместе, но он требует повышенных температур. [13]
Используя катализаторы PCP pincer-palladium, арильные-арильные связи могут быть достигнуты с числами оборотов (TON) свыше 900 000 и высокими выходами. [5] Кроме того, другие группы обнаружили, что очень низкие загрузки катализатора могут быть достигнуты с асимметричными комплексами палладия pincer. Было обнаружено, что загрузки катализатора 0,0001 моль % имеют TON свыше 190 000, а верхний предел TON может достигать 1 100 000.
Соногашира соединение
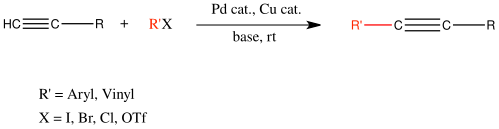
Сочетание Соногаширы нашло широкое применение в сочетании арилгалогенидов с алкинами. TONs свыше 2 000 000 и низкие загрузки катализатора 0,005 мол. % могут быть достигнуты с помощью катализаторов на основе PNP. [14]
Дегидрирование алканов
Алканы подвергаются дегидрированию при высоких температурах. Обычно это преобразование происходит гетерогенно, поскольку типично гомогенные катализаторы не выдерживают требуемых температур (~200 °C). Соответствующее преобразование может быть катализировано гомогенно пинцетными катализаторами, которые достаточно термически устойчивы. Доказательство концепции было установлено в 1996 году Йенсеном и его коллегами. Они сообщили, что пинцетный комплекс иридия и родия катализирует дегидрирование циклооктана с частотой оборота 12 мин −1 при 200 °C. Они обнаружили, что дегидрирование происходит со скоростью на два порядка выше, чем сообщалось ранее. [15] Было также обнаружено, что пинцетный комплекс иридия проявляет более высокую активность, чем родиевый комплекс. Эта разница в скорости может быть связана с доступностью степени окисления Ir(V), которая допускает более прочные связи Ir-C и Ir-H. [15]

Гомогенно катализируемый процесс может быть сопряжен с другими реакциями, такими как метатезис алкенов. Такие тандемные реакции не были продемонстрированы с гетерогенными катализаторами. [16] [17]
История
Первоначальная работа по лигандам PCP возникла из исследований комплексов Pt(II), полученных из длинноцепочечных дитретичных фосфинов, видов типа R 2 P(CH 2 ) n PR 2 , где n >4 и R = трет-бутил . Платина металлатирует одну метиленовую группу с высвобождением HCl, давая виды, такие как PtCl(R 2 P(CH 2 ) 2 CH(CH 2 ) 2 PR 2 ). [3]
Комплексы-пинцеры катализируют дегидрирование алканов. Ранние отчеты описывали дегидрирование циклооктана комплексом-пинцером Ir с частотой оборота 12 мин −1 при 200 °C. Комплексы термически стабильны при таких температурах в течение нескольких дней. [15]
Смотрите также
Ссылки
- ^ Химия пинцетных соединений; Моралес-Моралес, Д.; Йенсен, К., ред.; Elsevier Science: Амстердам, 2007. ISBN 0444531386
- ^ Дэвид Моралес-Моралес, Крейг Дженсен (2007). Химия пинцетных соединений . Elsevier. ISBN 978-0-444-53138-4.
- ^ ab Jensen, CM, «Иридиевые пинцетные комплексы PCP: высокоактивные и надежные катализаторы для новых гомогенных алифатических дегидрирований», Chemical Communications, 1999, 2443–2449. doi :10.1039/a903573g.
- ^ Гунанатан, К.; Бен-Дэвид, Ю. и Мильштейн, Д., «Прямой синтез амидов из спиртов и аминов с выделением H2 » , Science, 2007, 317, 790-792. doi :10.1126/science.1145295.
- ^ abcd Селандер, Никлас; Дж. Сабо, Кальман (2011). «Катализ комплексами палладиевых клещей». Химические обзоры . 111 (3): 2048–76. дои : 10.1021/cr1002112 . ПМИД 21087012.
- ^ ab Canty, AJ; Rodemann, T.; Skelton, BW; White, AH (2006). "Доступ к видам алкинилпалладия(IV) и -платины(IV), включая комплексы триоргано(дифосфин)металла(IV) и структурное исследование комплекса алкинил(пинцер)платины(IV), Pt(O2CArF)I(C⋮CSiMe3)(NCN) (ArF= 4-CF3C6H4, NCN = \2,6-(диметиламинометил)фенил-N,C,N]-)". Organometallics . 25 (16): 3996. doi :10.1021/om0601495.
- ^ Csok, Zsolt; Vechorkin, Олег; Harkins, Seth B.; Scopelliti, Rosario; Hu, Xile (2008-07-01). «Комплексы никеля лиганда Pincer NN2: множественная активация углерод-хлорида CH2Cl2 и CHCl3 приводит к селективному образованию связи углерод-углерод». Журнал Американского химического общества . 130 (26): 8156–8157. doi :10.1021/ja8025938. PMID 18528995.
- ^ Ди Франко, Томас; Стоянович, Марко; Келлер, Себастьен Карлос; Скопеллити, Росарио; Ху, Ксиле (2016-11-01). «Исследование структуры и активности пинцетных комплексов никеля NNN для реакций сочетания алкил-алкил Кумада и Сузуки-Мияура». Helvetica Chimica Acta . 99 (11): 830–847. doi :10.1002/hlca.201600165.
- ^ Далко, Петр I.; Мойсан, Лайонел (2001). «Энантиоселективный органокатализ». Angewandte Chemie, международное издание . 40 (20): 3726. doi :10.1002/1521-3773(20011015)40:20<3726::AID-ANIE3726>3.0.CO;2-D. ПМИД 11668532.
- ^ Джонсон, Магнус Т.; Йоханссон, Роджер; Кондрашов, Михаил В.; Стейл, Гидеон; Алквист, Мартен СГ; Рудт, Андреас; Вендт, Ола Ф. (2010). «Механизмы внедрения CO2 в аллиловые и метиловые σ-связи палладия (PCP). Кинетическое и вычислительное исследование». Organometallics . 29 (16): 3521. doi :10.1021/om100325v.
- ^ Бенито-Гарагорри, Д.; Киршнер, К. (2008). «Модульно спроектированные комплексы переходных металлов PNP и PCP Pincer на основе аминофосфинов: синтез и каталитическое применение». Accounts of Chemical Research . 41 (2): 201–213. doi :10.1021/ar700129q. PMID 18211031.
- ^ Weng, W.; Guo, C.; Çelenligil-Çetin, R.; Foxman, BM; Ozerov, OV (2006). «Изменение скелета в лиганде PNP-пинцета приводит к высокорегиоселективному катализатору димеризации алкинов». Chemical Communications (2): 197–199. doi :10.1039/B511148J. PMID 16372104.
- ^ Джон, Хартвиг (2010). Органопереходная металлическая химия: от связывания к катализу . Книги по университетской науке. ISBN 978-1-891389-53-5.
- ^ Bolliger, JL; Frech, CM (2009). «Очень удобные, чистые, быстрые и надежные реакции сочетания Соногаширы, стимулируемые пинцетными комплексами палладия на основе аминофосфина, выполненные в условиях реакции без добавок и аминов». Advanced Synthesis & Catalysis . 351 (6): 891. doi :10.1002/adsc.200900112.
- ^ abc Gupta, M.; Hagen, C.; Flesher, RJ; Kaska, WC; Jensen, CM (1996). «Высокоактивный катализатор дегидрирования алканов: стабилизация дигидридородиевых и иридиевых комплексов лигандом PCP pincer». Chemical Communications (17): 2083–2084. doi :10.1039/CC9960002083.
- ^ Хайбах, Майкл С.; Кунду, Сабудж; Брукхарт, Морис; Голдман, Алан С. (2012). «Метатезис алканов с помощью катализа тандемного дегидрирования алканов и метатезиса олефинов и родственной химии». Accounts of Chemical Research . 45 (6): 947–958. doi :10.1021/ar3000713. PMID 22584036.
- ^ Чой, Дж.; МакАртур, А. Р. Х.; Брукхарт, М.; Голдман, А. С. (2011). «Дегидрирование и родственные реакции, катализируемые комплексами иридиевого пинцета». Chemical Reviews . 111 (3): 1761–1779. doi : 10.1021/cr1003503. PMID 21391566.