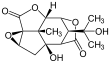
Пикротоксин
Пикротоксинин (слева) и пикротин (справа) | |||
| Клинические данные | |||
|---|---|---|---|
| код АТС |
| ||
| Идентификаторы | |||
| Номер CAS | |||
| CID PubChem |
| ||
| ИУФАР/БПС |
| ||
| DrugBank | |||
| ChemSpider | |||
| УНИИ |
| ||
| КЕГГ | |||
| ЧЭБИ | |||
| ChEMBL | |||
| Панель инструментов CompTox ( EPA ) |
| ||
| Информационная карта ECHA | 100.004.288 | ||
| Химические и физические данные | |||
| 3D модель ( JSmol ) |
| ||
| |||
 Н Н И (что это?) (проверить) И (что это?) (проверить) | |||
Пикротоксин , также известный как коккулин , является ядовитым кристаллическим растительным соединением. Впервые он был выделен французским фармацевтом и химиком Пьером Франсуа Гийомом Булле (1777–1869) в 1812 году. [1] Название «пикротоксин» представляет собой комбинацию греческих слов «picros» (горький) и «toxicon» (яд). [2] Смесь двух различных соединений, пикротоксин встречается в природе в плодах растения Anamirta cocculus , хотя его также можно синтезировать химическим путем.
Взаимодействуя с тормозным нейротрансмиттером ГАМК , пикротоксин действует как стимулятор и судорожное средство. Он в основном воздействует на центральную нервную систему, вызывая судороги и паралич дыхания в достаточно высоких дозах.
Химическая структура и синтез
Пикротоксин представляет собой эквимолярную смесь двух соединений: пикротоксинина (C 15 H 16 O 6 ; CAS# 17617-45-7) и пикротина (C 15 H 18 O 7 ; CAS# 21416-53-5). [3] Из двух соединений пикротин менее активен. [4]
Пикротоксин встречается в природе в плодах Anamirta cocculus , вьющегося растения из Индии и других частей Юго-Восточной Азии. Растение известно своими большими стеблями из белой древесины и душистыми цветами. Оно производит небольшие косточковые плоды, Cocculus indicus , которые обычно сушат. [ необходима цитата ]
В настоящее время существует целых пять синтезов пикротоксинина, один из которых был опубликован совсем недавно, в июне 2020 года. [5] В большинстве синтезов в качестве стереохимического шаблона используется карвон .
![Начните с метил (1S,4S,5R,7R,8S,9R,10R,11R)-10-(ацетилокси)-7-гидрокси-11-метил-3-оксо-9-(проп-1-ен-2-ил)-4,5-бис[(триметилсилил)окси]-2-оксатрицикло[5.3.1.04,11]ундекан-8-карбоксилата. (1) Внутримолекулярная переэтерификация, высвобождающая метилацетат; затем (2) снятие защиты с триметилсилил-защищенного вицинального диола, за которым следует (3) восстановительная дегидратация до олефина и (4) стереоспецифическое эпоксидирование до глицидного эфира](http://upload.wikimedia.org/wikipedia/commons/thumb/9/96/Picrotoxinin_Synthesis.png/500px-Picrotoxinin_Synthesis.png)
В 1988 году исследователи из Университета Тохоку в Японии завершили полный стереоселективный синтез как (‑)‑пикротоксинина, так и (-)-пикротина, начиная с (+)‑5β‑ гидроксикарвона . В этом синтезе восемь асимметричных центров были стереоселективно подготовлены на цис -конденсированной гидриндановой кольцевой системе с использованием нескольких различных реакций: перегруппировка Кляйзена для введения четвертичного центра, органоселен-опосредованное восстановление эпоксикетона и стереоспецифическое построение глицидного эфира. [ 7 ]
Вместо этого в синтезе, проведенном в июне 2020 года, использовалось быстрое формирование полициклического ядра с последующей манипуляцией степенями окисления ключевых атомов углерода для получения целевой молекулы. [5]
Некоторые исследования показывают, что пикритоксин может быть получен путем циклофункционализации циклоалкенильных систем. В кинетически контролируемых условиях этот процесс обычно приводит к экзоциклизации и образованию мостиковых кольцевых систем, подобных тем, что обнаружены в пикротоксине. [8]
Было разработано несколько методов для индивидуальной изоляции пикротоксинина и пикротина. Реакция с соседним цис- спиртом является ключевым препятствием и может быть ингибирована предварительной обработкой ( защитой ) трифторуксусным ангидридом в пиридине : [9]

Пикротоксин также использовался в качестве исходного материала в нескольких синтетических процессах, включая создание dl -пикротоксадиена, который сохраняет некоторые черты скелета пикротоксина. [10]
Механизм действия
Некоторые мышечные волокна ракообразных имеют возбуждающую и тормозную иннервацию. Пикротоксин блокирует торможение. [11] Были предложены две различные, но связанные теории относительно механизма, посредством которого пикротоксин действует на синапсы . Одна из теорий заключается в том, что он действует как неконкурентный блокатор каналов для хлоридных каналов рецептора ГАМК А , [12] в частности, хлоридного ионофора, активируемого гамма-аминомасляной кислотой. [13] Исследование 2006 года показало, что, хотя и не является структурно похожим на ГАМК, пикротоксин предотвращает поток ионов через хлоридные каналы, активируемые ГАМК. Он, вероятно, действует внутри самих ионных каналов, а не в местах распознавания ГАМК. Поскольку он ингибирует каналы, активируемые ГАМК, препараты, усиливающие ГАМК, такие как барбитураты и бензодиазепины, могут использоваться в качестве антидота. [14]
Другие исследования показывают, что токсин действует вместо этого как неконкурентный антагонист или ингибитор ГАМК-рецепторов. Исследование Ньюленда и Калл-Кэнди показало, что в достаточно высоких концентрациях пикротоксин снижает амплитуду токов ГАМК. Их данные показали, что маловероятно, что пикротоксин действует просто как блокатор потенциалзависимых каналов, хотя он и снижает частоту открытия каналов. Скорее, они обнаружили, что пикротоксин «связывается преимущественно с агонистически связанной формой рецептора». Это означает, что даже в присутствии низких концентраций пикротоксина реакция нейронов на ГАМК снижается. [15]
Токсичность
Пикротоксин действует как стимулятор центральной нервной системы и дыхания. Он чрезвычайно токсичен для рыб и людей, а также грызунов и других млекопитающих. Согласно Регистру токсического воздействия химических веществ, LDLo, или самая низкая зарегистрированная смертельная доза, составляет 0,357 мг/кг. Симптомы отравления пикротоксином включают кашель, затрудненное дыхание, головную боль, головокружение, спутанность сознания, желудочно-кишечные расстройства, тошноту или рвоту, а также изменения частоты сердечных сокращений и артериального давления. Хотя он особенно опасен при проглатывании, системные эффекты могут также возникнуть при вдыхании или всасывании в кровоток через повреждения на коже. [16] Пикротоксин также действует как судорожное средство. Было обнаружено, что в больших дозах он вызывает клонические судороги или сердечную аритмию, причем особенно высокие дозы в конечном итоге оказываются смертельными, как правило, из-за паралича дыхания. [17]
Клиническое применение и другие виды использования
Из-за своей токсичности пикротоксин в настоящее время чаще всего используется в качестве исследовательского инструмента. Однако из-за его антагонистического эффекта на ГАМК-рецепторы он использовался как стимулятор центральной нервной системы. Ранее он также использовался как противоядие при отравлении депрессантами ЦНС, особенно барбитуратами . [18]
Хотя пикротоксин не используется широко, он эффективен как пестицид и педикулицид . В 19 веке его использовали при приготовлении крепкого мультума , который добавляли в пиво, чтобы сделать его более опьяняющим. С тех пор этот препарат был объявлен вне закона. [19] [20]
Несмотря на свою потенциальную токсичность для млекопитающих в достаточно больших дозах, пикротоксин также иногда используется в качестве усилителя производительности у лошадей. Он классифицируется как нелегальное «вещество класса I» Американской ассоциацией лошадей четвертьфинальной породы . Вещества, которые классифицируются как «класс I», вероятно, влияют на производительность и не имеют терапевтического применения в медицине лошадей. [21] В 2010 году тренер лошадей четвертьфинальной породы Роберт Димитт был отстранен после того, как его лошадь, Stoli Signature, дала положительный результат на это вещество. Как и у людей, он используется для противодействия отравлению барбитуратами. [22]
Смотрите также
Ссылки
- ^ Булле П.Ф. (1812). «Анализ химического препарата де ла Кок дю Левант, Menispermum cocculus». Bulletin de Pharmacie (на французском языке). 4 : 5–34 .
Menispermum cocculus» переименован в «Anamirta cocculus».
- ^ (Буллей, 1812), стр. 31.
- ^ Ло В., Нокс С., Джумбу Ю., Джуисон Т., Го AC, Лю Ю. и др. «Пикротоксин». Наркобанк . Проверено 26 апреля 2017 г.
- ^ Гаммилл Р., Тулинский Дж. (1994). «Химия и фармакология ГАМКА и лигандов ГАМКАБ». Современная медицинская химия . 1 (3): 242 . Проверено 26 апреля 2017 г.
- ^ ab Crossley SW, Tong G, Lambrecht MJ, Burdge HE, Shenvi RA (июль 2020 г.). «Синтез (-)-пикротоксинина с помощью активации сильной связи на поздней стадии». Журнал Американского химического общества . 142 (26): 11376– 11381. doi :10.1021/jacs.0c05042. PMC 8011636. PMID 32573211 .
- ^ Trost B , Krische MJ (1996). "Пикротоксинин". Журнал Американского химического общества . 118 : 233. doi :10.1021/ja953060r . Получено 7 мая 2017 г.
- ^ Мияшита М., Сузуки Т., Йошикоши А. (май 1989 г.). «Стереоселективный полный синтез (-)-пикротоксинина и (-)-пикротина». Журнал Американского химического общества . 111 (10): 3728– 3734. Bibcode : 1989JAChS.111.3728M. doi : 10.1021/ja00192a035.
- ^ Trost B, Fleming I (1991). Comprehensive Organic Synthesis (том 4, изд.). Оксфорд, Великобритания: Pergamon Press. стр. 373. ISBN 9780080405957. Получено 7 мая 2017 г. .
- ^ Corey EJ, Pearce HL (1980). «Полный синтез пикротина». Tetrahedron Letters . 21 (19): 1823– 1824. doi :10.1016/s0040-4039(00)92789-8.
- ^ Conroy H (июнь 1952). «Пикротоксин. II. Скелет пикротоксинина. Полный синтез dl-пикротоксадиена». Журнал Американского химического общества . 74 (12): 3046–3051 . Bibcode : 1952JAChS..74.3046C. doi : 10.1021/ja01132a028.
- ^ Van Der Kloot WG, Robbins J, Cooke IM (март 1958). «Блокирование пикротоксином периферического торможения у раков». Science . 127 (3297): 521– 522. Bibcode :1958Sci...127..521V. doi :10.1126/science.127.3297.521. PMID 13529017.
- ^ Ро Дж.М., Доневан С.Д., Рогавски М.А. (декабрь 1996 г.). «Прямая активация рецепторов ГАМКА барбитуратами в культивируемых нейронах гиппокампа крысы». Журнал физиологии . 497 (2): 509–22 . doi :10.1113/jphysicalol.1996.sp021784. ПМК 1161000 . ПМИД 8961191.
- ^ Ло В., Нокс С., Джумбу Ю., Джуисон Т., Го AC, Лю Ю. и др. «Пикротоксин». Наркобанк . Проверено 26 апреля 2017 г.
- ^ Olsen RW (апрель 2006 г.). «Блокаторы пикротоксиноподобных каналов ГАМК-рецепторов». Труды Национальной академии наук Соединенных Штатов Америки . 103 (16): 6081– 2. Bibcode : 2006PNAS..103.6081O. doi : 10.1073/pnas.0601121103 . PMC 1458832. PMID 16606858 .
- ^ Newland CF, Cull-Candy SG (февраль 1992). «О механизме действия пикротоксина на каналы рецепторов ГАМК в диссоциированных симпатических нейронах крысы». Журнал физиологии . 447 : 191– 213. doi :10.1113/jphysiol.1992.sp018998. PMC 1176032. PMID 1317428 .
- ^ "Пикротоксин" (PDF) . Santa Cruz Biotechnology . Получено 26 апреля 2017 г.
- ^ "Пикротоксин". Toxnet . Национальная медицинская лаборатория США . Получено 26 апреля 2017 г. .
- ^ Нильссон Э., Эйрих Б. (2009). «О лечении отравления барбитуратами». Acta Medica Scandinavica . 137 (6): 381– 9. doi :10.1111/j.0954-6820.1950.tb12129.x. PMID 15432128.
- ^ Böttger A, Vothknecht U, Bolle C, Wolf A (2018). «Растительные препараты, влияющие на ионные каналы». Lessons on Caffeine, Cannabis & Co: Plant-derived Drugs and their Interaction with Human Receptors . Learning Materials in Biosciences. p. 129. doi :10.1007/978-3-319-99546-5_8. ISBN 978-3-319-99545-8.
- ^ Белл Дж. (1869). Отчет Комитета по отношениям алкоголя к медицине . Соединенные Штаты: Коллинз. стр. 32.
- ^ "Единые руководящие принципы классификации посторонних веществ и рекомендуемые штрафы и типовое правило" (PDF) . Association of Racing Commissioners International, Inc . Получено 26 апреля 2017 г. .
- ^ Lemoreaux P (2 сентября 2017 г.). «Два тренера Quarter Horse отстранены за нарушение правил употребления наркотиков в Prairie Meadows». Daily Racing Form. Daily Racing Form . Получено 26 апреля 2017 г.
Дальнейшее чтение
- Эренбергер К., Бенкое Э., Феликс Д. (1982). «Подавляющее действие пикротоксина, антагониста ГАМК, на лабиринтный спонтанный нистагм и головокружение у человека». Acta Oto-Laryngologica . 93 ( 1–6 ): 269–73 . doi :10.3109/00016488209130882. PMID 7064710.
- Дюпон Л., Дидеберг О., Ламотт-Брассёр Дж., Анжено Л. (1976). «Кристаллическая структура и молекула пикротоксина C 15 H 16 O 6 ·C 15 H 18 O 7 ». Acta Crystallographica B (на французском языке). 32 (11): 2987–2993 . Бибкод : 1976AcCrB..32.2987D. дои : 10.1107/S0567740876009424. hdl : 2268/31560 .
- Olsen RW, DeLorey TM (1999). "GABA Receptor Physiology and Pharmacology". В Siegel GJ, Agranoff BW, Albers RW, et al. (ред.). Basic Neurochemistry: Molecular, Cellular and Medical Aspects (6-е изд.). Филадельфия, Пенсильвания, США: Lippincott-Raven.