Органоактинидная химия

Химия актиноидорганических соединений — это наука, изучающая свойства, структуру и реакционную способность актиноидорганических соединений , представляющих собой металлоорганические соединения , содержащие химическую связь углерода с актиноидом .
Как и большинство металлоорганических соединений, органоактиниды чувствительны к воздуху и требуют обращения с ними с использованием соответствующих методов .
Металлоорганические комплексы с σ-связями
Наиболее распространенные органоактинидные комплексы включают π-связь с лигандами, такими как циклопентадиенил , но есть несколько исключений с σ-связью , а именно в химии тория и урана , поскольку они являются наиболее легко обрабатываемыми элементами этой группы.
Алкильные и арильные соединения

Попытки синтезировать алкилы урана были впервые предприняты во время Манхэттенского проекта Генри Гилманом , вдохновленным летучестью основных групп металлоорганических соединений. Однако он заметил, что эти соединения, как правило, крайне нестабильны. [1]
Маркс и Сейам попытались синтезировать их из UCl4 с использованием литийорганических реагентов , но они быстро разлагались.
В 1989 году группа наконец синтезировала гомолептический комплекс с триметилсилильными группами: U[CH(SiMe 3 ) 2 ] 3 . С тех пор также были синтезированы варианты с более высокими координационными числами , такие как [Li(TMEDA)] 2 [UMe 6 ] . [1]
С другой стороны, известен только один гомолептический алкил тория. [2] Семикоординированный анион гептаметилтората(IV) был синтезирован в 1984 году с использованием процедуры, аналогичной эквивалентному урановому комплексу.
Также были получены смешанные фосфинсодержащие комплексы тетраметилов тория и урана с использованием dmpe в качестве фосфорорганического лиганда, стабилизирующего структуру (амиды также могут выполнять эту роль) [3] .
Металлоциклы
Уран и торий образуют металлоциклы с разнообразной химией. [4] Эти комплексы очень лабильны, поэтому триметилсилильные группы снова присутствуют для защиты. Эти соединения образуются путем реакции более слабых алкилирующих агентов ( LiCH 3 и Mg(CH 3 ) 2 слишком сильны и приводят к образованию простых алкилов) с ClAn[N(Si(CH 3 ) 2 ] 3 (An = Th, U).

Металлоорганические комплексы с π-связями
Большинство органоактинидов включают в себя циклопентадиенил (ЦП) или циклооктатетраен (ЦОТ) и их производные в качестве лигандов. Они обычно принимают участие в η 5 - и η 8 -связывании , передавая электронную плотность через свои пи-орбитали.
Циклооктатетраеновые комплексы
Актиноцены

Актиниды образуют сэндвичевые комплексы с циклооктатетраеном аналогично тому, как переходные металлы реагируют с циклопентадиенильными лигандами. Ионы актинидов имеют атомные радиусы , которые слишком велики для образования соединений MCp 2 , поэтому они предпочитают реагировать с ионами C 8 H 8 2- .
Первый пример этого типа химических соединений был обнаружен в 1968 году Эндрю Штрейтвизером , который получил ураноцен путем реакции K(COT) 2 с UCl4 в тетрагидрофуране при 0 °C. [ 5] Само соединение представляет собой пирофорное зеленое твердое вещество, которое в остальном совершенно нереакционноспособно. [6]

Большинство четырехвалентных актинидов реагируют схожим образом, образуя актиноцены:
Бис(циклооктатетраен)протактиний был впервые получен в 1973 году путем превращения оксида протактиния(V) в пентахлорид и восстановления его алюминиевым порошком перед реакцией с циклооктатетраенидом калия . [7]
- :
Нептуноцен и тороцен были получены аналогичным образом с использованием тетрахлоридов. Плутоноцен является исключением: поскольку неизвестен стабильный хлорид плутония(IV), пришлось использовать (Hpy ) 2PuCl6 .
Более поздние актиниды также образуют комплексы с COT, но они обычно не принимают классическую нейтральную сэндвичевую структуру . Трехвалентные актиниды образуют ионные соединения с лигандами COT, это можно проиллюстрировать на примере реакции трииодида америция с K 2 COT.
Это соединение присутствует в растворе в виде аддукта ТГФ.
Комплексы замещенных циклооктатетраенов
Было синтезировано много замещенных ураноценов. [8] [9] Использовалась та же методология, что и для простого U(COT) 2 , но свойства некоторых соединений оказались другими.
Штрайтвизером было обнаружено, что тетрафенилциклооктатетраеновый комплекс полностью стабилен на воздухе. Эта высокая стабильность, вероятно, обусловлена тормозящим эффектом фенильных групп, защищающих центр U4 + от атаки кислорода . [9]
Все эти производные гораздо лучше растворимы в органических растворителях, таких как бензол , в котором они образуют зеленые растворы, более чувствительные к воздуху, чем кристаллические твердые вещества.

Плутоний также образует сэндвич-комплекс с 1,4-бис(триметилсилил)циклооктатетраенилом (1,4-COT'') и его 1,3-изомером. Это соединение получают окислением анионного зеленого комплекса Pu(III) Li(THF) 4 [Pu(1,4-COT'') 2 ] с хлоридом кобальта(II) , что приводит к образованию Pu(1,4-COT'')(1,3-COT''). Реакция легко заметна по изменению цвета раствора ТГФ на темно-красный, характерный для Pu(IV). [10]

Нептуниевый эквивалент с тризамещенным COT''' также был описан [11] , а комплексы как три-, так и дизамещенных лигандов с торием и ураном хорошо известны. [12] Они были синтезированы в соответствии со следующими схемами реакций:

Циклопентадиеновые комплексы
Комплексы трис(циклопентадиенил)актинида

Большинство трехвалентных f- элементов образуют соединения с циклопентадиеном с формулой M(Cp) 3 . Эти комплексы были выделены вплоть до калифорния , при этом эквивалент эйнштейния [ требуется цитата ] наблюдался в газовой фазе. [13]

Синтез AnCp 3 обычно следует схеме реакции, показанной выше [4] [14], с несколькими дополнительными шагами, которые иногда необходимы для синтеза трихлоридов из коммерчески поставляемых оксидов. [13] Тем не менее, некоторые авторы также используют другие синтезы: циклопентадиениды щелочных металлов могут быть использованы вместо комплекса бериллия, а комплексы An(IV) также могут быть использованы посредством реакции восстановительного элиминирования .
| Чт | У | Нп | Пу | Являюсь | См | Бк | Ср. |
|---|---|---|---|---|---|---|---|
| зеленый | коричневый | бледно-зеленый | зеленый | плоть | бесцветный | янтарь | красный |
Эти соединения известны с шестидесятых годов, однако до 2018 года структурно охарактеризовано было только соединение нептуния. Ковач и его коллеги смогли проанализировать комплексы плутония и урана, обнаружив, что все три структуры были похожи, с асимметричным распределением циклопентадиенидных лигандов и более высоким ковалентным характером связи углерод-актинид, чем в органолантаноидных соединениях. [16]
Комплексы тетракис(циклопентадиенил)актинидов
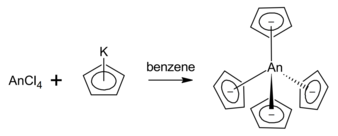
Четырехвалентный торий, уран и нептуний легко образуют соединения MCp 4 путем реакции метатезиса из циклопентадиенида калия с использованием бензола в качестве растворителя. [4]
Циклогептатриеновые комплексы
Хотя они и изучены меньше, было предсказано существование комплексов актинидов с ионом гептагаптоциклогептатриенила (Ch) и синтезирован урановый вид U(Ch) 2 − . Предполагается, что эти комплексы являются окислительными. Из-за сокращения 5f-орбитали ожидается, что комплексы актинидов и циклогептатриенов будут снижать стабильность с более высокими атомными номерами. [17]
Смотрите также
- Уранорганическая химия
- Химия органонептуния
- Актиноцены
- Ураноцен , U(C 8 H 8 ) 2
- Нептуноцен , Np(C 8 H 8 ) 2
- Плутоноцен , Pu(C 8 H 8 ) 2
Ссылки
- ^ ab Seaman LA, Walensky JR, Wu G, Hayton TW (апрель 2013 г.). «В поисках гомолептических актинидных алкильных комплексов». Неорганическая химия . 52 (7): 3556– 64. doi :10.1021/ic300867m. PMID 22716022.
- ^ Lauke H, Swepston PJ, Marks TJ (октябрь 1984 г.). «Синтез и характеристика гомолептического актинидного алкила. Ион гептаметилтората(IV): комплекс с семью металл-углеродными .сигма. связями». Журнал Американского химического общества . 106 (22): 6841– 6843. doi :10.1021/ja00334a062.
- ^ Edwards PG, Andersen RA, Zalkin A (февраль 1984). «Получение комплексов тетраалкилфосфина металлов f-блока. Кристаллическая структура Th(CH2Ph)4(Me2PCH2CH2PMe2) и U(CH2Ph)3Me(Me2PCH2CH2PMe2)». Organometallics . 3 (2): 293– 298. doi :10.1021/om00080a023.
- ^ abc Behrle AC, Walensky JR (2015), «Актиниды: металлоорганическая химия», Энциклопедия неорганической и бионеорганической химии , Американское онкологическое общество, стр. 1–41 , doi :10.1002/9781119951438.eibc0002.pub2, ISBN 9781119951438
- ^ Штрейтвизер-младший А., Мюллер-Вестерхофф У. (1968-12-01). "Бис(циклооктатетраенил)уран (ураноцен). Новый класс сэндвичевых комплексов, использующих атомные f-орбитали". Журнал Американского химического общества . 90 (26): 7364. doi :10.1021/ja01028a044.
- ^ Коттон, Саймон. (2013). Лантаноидная и актиноидная химия . John Wiley & Sons. ISBN 9781118681367. OCLC 897575995.
- ^ Starks DF, Parsons TC, Streitwieser A, Edelstein N (июнь 1974). "Бис(.пи.-циклооктатетраен)протактиний". Неорганическая химия . 13 (6): 1307– 1308. doi :10.1021/ic50136a011.
- ^ Streitwieser A, Harmon CA (1973-05-01). «Ураноцены с углеводородными заместителями». Неорганическая химия . 12 (5): 1102– 1104. doi :10.1021/ic50123a024.
- ^ ab Streitwieser A, Walker R (сентябрь 1975 г.). "Бис-π-(1,3,5,7-тетрафенилциклооктатетраен)уран, устойчивый на воздухе ураноцен". Журнал металлоорганической химии . 97 (3): C41 – C42 . doi :10.1016/S0022-328X(00)89316-X.
- ^ Apostolidis C, Walter O, Vogt J, Liebing P, Maron L, Edelmann FT (апрель 2017 г.). «Структурно охарактеризованный металлоорганический комплекс плутония (IV)». Angewandte Chemie . 56 (18): 5066– 5070. doi :10.1002/anie.201701858. PMC 5485009 . PMID 28371148.
- ^ Tassell MJ, Kaltsoyannis N (август 2010). «Ковалентность в AnCp4 (An = Th-Cm): сравнение молекулярных орбиталей, естественной популяции и анализов атомов в молекулах». Dalton Transactions . 39 (29): 6719– 25. doi :10.1039/c000704h. PMID 20631951.
- ^ Rausch J, Apostolidis C, Walter O, Lorenz V, Hrib CG, Hilfert L, Kühling M, Busse S, Edelmann FT (2015). «Один лиганд подходит всем: сэндвич-комплексы лантаноидов и актинидов, включающие лиганд 1, 4-бис (триметилсилил) циклооктатетраенил (= COT′′)». New Journal of Chemistry . 39 (10): 7656– 66. doi : 10.1039/c5nj00991j .
- ^ ab Laubereau PG, Burns JH (май 1970). «Микрохимическое получение трициклопентадиенильных соединений берклия, калифорния и некоторых лантаноидов». Неорганическая химия . 9 (5): 1091– 1095. doi :10.1021/ic50087a018.
- ^ Баумгартнер, Ф.; Фишер, Э.О.; Канеллакопулос, Б.; Лаберо, П. (7 января 1966 г.). «Трициклопентадиениламериций (III)». Angewandte Chemie (на немецком языке). 78 (1): 112–113 . doi :10.1002/ange.19660780113.
- ^ Marks TJ (сентябрь 1982 г.). «Актинидная металлоорганическая химия». Science . 217 (4564): 989– 97. Bibcode :1982Sci...217..989M. doi :10.1126/science.217.4564.989. PMID 17839316.
- ^ Apostolidis C, Dutkiewicz MS, Kovács A, Walter O (февраль 2018 г.). "Твердотельная структура трис-циклопентадиенида урана(III) и плутония(III)". Химия: европейский журнал . 24 (12): 2841– 2844. doi :10.1002/chem.201704845. PMC 5861669. PMID 29193373 .
- ^ Ли, Джун; Берстен, Брюс Э. (1 сентября 1997 г.). «Электронная структура циклогептатриенильных сэндвичевых соединений актинидов: An(η 7 -C 7 H 7 ) 2 (An = Th, Pa, U, Np, Pu, Am)». Журнал Американского химического общества . 119 (38): 9021– 9032. doi :10.1021/ja971149m.
- Маркс, Тобин Дж. (1982). «Актинидная металлоорганическая химия». Science . 217 (4564): 989–997 . doi :10.1126/science.217.4564.989.
![{\displaystyle {\ce {Pa2O5 + SOCl2 ->[400C] PaCl5}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/c49a38424502d636696eb5b77a0e618cf6990cab)


