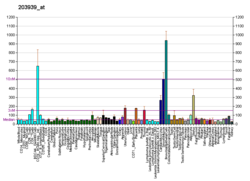
NT5E
| NT5E | |||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| Идентификаторы | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Псевдонимы | NT5E , CALJA, CD73, E5NT, NT, NT5, NTE, eN, eNT, экто 5'-нуклеотидазы | ||||||||||||||||||||||||||||||||||||||||||||||||||
| Внешние идентификаторы | ОМИМ : 129190; МГИ : 99782; Гомологен : 1895; Генные карты : NT5E; OMA :NT5E — ортологи | ||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| Викиданные | |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
5′-нуклеотидаза (5′-NT), также известная как экто-5′-нуклеотидаза или CD73 ( кластер дифференциации 73), представляет собой фермент , который у людей кодируется геном NT5E . [ 5] CD73 обычно служит для преобразования АМФ в аденозин . [6]
Сайты связывания факторов транскрипции
NT5E содержит сайты связывания для факторов транскрипции AP-2, белков SMAD , SP-1 и элементов, реагирующих на c-AMP , которые можно найти в частях промотора c-AMP. SMAD 2, 3, 4 и 5 и SP-1 связываются с промотором NT5E у крыс, что было доказано в анализах иммунопреципитации хроматина. В связи с тем, что транскрипты человеческого и крысиного NT5E на 89% идентичны, человеческий NT5E также может регулироваться белками SMAD. [7]
Функция
Экто-5-прим-нуклеотидаза (5-прим-рибонуклеотидфосфогидролаза; EC 3.1.3.5) катализирует превращение при нейтральном pH пуриновых 5-прим мононуклеотидов в нуклеозиды, предпочтительным субстратом является AMP . Фермент состоит из димера из 2 идентичных 70-кДа субъединиц, связанных гликозилфосфатидилинозитоловой связью с внешней поверхностью плазматической мембраны. Фермент используется в качестве маркера дифференциации лимфоцитов . Следовательно, дефицит NT5 возникает при различных иммунодефицитных заболеваниях (например, см. MIM 102700, MIM 300300). Другие формы 5-первичной нуклеотидазы существуют в цитоплазме и лизосомах и могут быть отличимы от экто-NT5 по их субстратному сродству, потребности в двухвалентном ионе магния, активации АТФ и ингибированию неорганическим фосфатом. [8] Редкие аллельные варианты связаны с синдромом кальцификации суставов и артерий у взрослых (CALJA), поражающим подвздошные , бедренные и большеберцовые артерии, снижая кровообращение в ногах и суставах рук и стоп, вызывая боль. [9] [10] [11]
Иммуносупрессия
NT5E (CD73) — это поверхностный фермент , который экспрессируется на нескольких клетках. Этот фермент опосредует постепенный гидролиз аутокринных и паракринных сигналов опасности АТФ и АДФ до противовоспалительного аденозина . Иммуносупрессия, опосредованная аденозинэргическими путями, очень важна для поддержания гомеостаза иммунной системы. Иммуносупрессивные функции регуляторных Т-клеток также зависят от экспрессии CD73. Treg обычно подавляют иммунный ответ. Они влияют на пролиферацию и функцию Т-клеток. [12] CD73 также встречается на анергических CD4 + Т-клетках, тем самым поддерживая собственную толерантность к здоровым тканям, а также защищая плод от иммунной системы матери во время беременности. Также был описан аденозин, генерируемый NT5E, который ограничивает воспалительный иммунный ответ посредством отрицательной обратной связи в нейтрофилах , которые экспрессируют аденозиновый рецептор . [13]
Как мишень для наркотиков
В некоторых опухолях наблюдается повышенная регуляция и сверхэкспрессия CD73, поэтому он был предложен в качестве лекарственной мишени для терапии рака. [14] [15] [16]
Антитело CPI-006 против CD73 уже находится на ранней стадии клинических испытаний в качестве средства для лечения запущенных форм рака. [17]
Системная красная волчанка
Специализированные иммунные клетки, такие как миелоидные супрессорные клетки и регуляторные Т-клетки, также опосредуют свои эффекты через аденозин, генерируемый локальной эктонуклеотидазой. В некоторых случаях у пациентов с волчанкой отсутствует адекватная экспрессия CD73 Т-клетками, что свидетельствует о нарушенной регуляторной функции Т-клеток. [18]
Рак
NT5E может действовать как иммуноингибиторная контрольная молекула. Свободный аденозин, генерируемый NT5E, ингибирует клеточные иммунные реакции и тем самым способствует иммунному ускользанию опухолевых клеток. [13] Благодаря ферментативным и неферментативным свойствам CD73 участвует в процессах, связанных с раком, и его уровень повышается при многих видах рака, таких как лейкемия , глиобластома , меланома , рак пищевода , простаты , яичников и молочной железы . Это важная ключевая молекула в регуляции и развитии рака и участвует в прогрессировании опухоли. Кроме того, NT5E функционирует как адгезионная и сигнальная молекула и может регулировать клеточную сигнализацию с компонентами внеклеточного матрикса, такими как фибронектин и ламинин . Это может опосредовать метастатические и инвазивные свойства рака. [19] В мышиных моделях опухолей молочной железы и рака простаты, а также в модели ксенотрансплантата молочной железы было подтверждено, что NT5E поддерживает ангиогенез опухоли . Его экспрессия способствует инвазии и метастазированию клеток меланомы мышей и человека и клеток рака молочной железы человека. Инфильтрация опухоли клетками, которые экспрессируют NT5E, такими как миелоидные супрессорные клетки (MDSC), Treg, дендритные клетки (DC), приводит к накоплению аденозина. Впоследствии сигнализация цАМФ запускается в Т-клетках , которые экспрессируют аденозиновый рецептор A2A . [20] Аденозиновые рецепторы также экспрессируются на макрофагах , DC, MDSC и естественных клетках-киллерах (NK). Таким образом, аденозин может ингибировать функцию этих иммунных клеток. Кроме того, опухолевые клетки могут также экспрессировать аденозиновые рецепторы A1 и A3 , связанные с белками Gαi, что способствует как миграции, так и пролиферации опухолевых клеток. [13] [19] [21] Особенно из-за его полезных эффектов в мышиной модели опухоли, анти-CD73-терапия в настоящее время является многообещающим подходом к лечению рака в будущем. Ингибиторы CD73 в настоящее время проходят клинические испытания для лечения рака. [19]
миРНК
МикроРНК — это небольшие некодирующие молекулы РНК , которые регулируют экспрессию генов на посттранскрипционном уровне посредством связывания с мРНК. Это приводит к деградации целевой молекулы мРНК или трансляционной репрессии. В опухолевых клетках паттерн экспрессии miRNA часто меняется и, следовательно, влияет на поверхностный NT5E, что в результате мешает противоопухолевому иммунному ответу. [22] [23] Например, исследования подтверждают роль семейства miR30 в регуляции NT5E. При экспрессии miR-30a-5p экспрессия NT5E снижалась. [13]
Смотрите также
Ссылки
- ^ abc GRCh38: Ensembl выпуск 89: ENSG00000135318 – Ensembl , май 2017 г.
- ^ abc GRCm38: Ensembl выпуск 89: ENSMUSG00000032420 – Ensembl , май 2017 г.
- ^ "Human PubMed Reference:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США .
- ^ "Mouse PubMed Reference:". Национальный центр биотехнологической информации, Национальная медицинская библиотека США .
- ^ Misumi Y, Ogata S, Ohkubo K и др. (август 1990 г.). «Первичная структура человеческой плацентарной 5'-нуклеотидазы и идентификация гликолипидного якоря в зрелой форме». European Journal of Biochemistry . 191 (3): 563– 9. doi :10.1111/j.1432-1033.1990.tb19158.x. PMID 2129526.
- ^ Allard B, Cousineau I, Spring K и др. (2019-01-01), «Глава пятнадцатая — Измерение ферментативной активности CD73 с использованием люминесцентных и колориметрических анализов», в Galluzzi L, Rudqvist NP (ред.), Tumor Immunology and Immunotherapy — Molecular Methods, Methods in Enzymology, т. 629, Academic Press, стр. 269–289 , doi :10.1016/bs.mie.2019.10.007, ISBN 978-0-12-818671-8, PMID 31727245, S2CID 208035622 , получено 28.11.2020
- ^ Kordaß T, Osen W, Eichmüller SB (2018). «Управление иммуносупрессором: факторы транскрипции и микроРНК, регулирующие CD73/NT5E». Frontiers in Immunology . 9 : 813. doi : 10.3389 /fimmu.2018.00813 . PMC 5915482. PMID 29720980.
- ^ "Ген Entrez: 5′-нуклеотидаза NT5E, экто (CD73)".
- ^ St Hilaire C, Ziegler SG, Markello TC и др. (февраль 2011 г.). «NT5E мутации и артериальные кальцификации». The New England Journal of Medicine . 364 (5): 432– 42. doi :10.1056/NEJMoa0912923. PMC 3049958. PMID 21288095 .
- ^ Sharp J (март 1954). «Наследственная сосудистая и суставная кальцификация». Annals of the Rheumatic Diseases . 13 (1): 15–27 . doi :10.1136/ard.13.1.15. PMC 1030367. PMID 13149051 .
- ^ Интернет-менделевское наследование у человека (OMIM): 211800
- ^ Dong K, Gao ZW, Zhang HZ (декабрь 2016 г.). «Роль аденозинэргического пути при аутоиммунных заболеваниях человека». Immunologic Research . 64 ( 5– 6): 1133– 1141. doi :10.1007/s12026-016-8870-2. PMC 5126201. PMID 27665459 .
- ^ abcd Kordaß T, Osen W, Eichmüller SB (2018-04-18). "Управление иммуносупрессором: факторы транскрипции и микроРНК, регулирующие CD73/NT5E". Frontiers in Immunology . 9 : 813. doi : 10.3389/fimmu.2018.00813 . PMC 5915482. PMID 29720980 .
- ^ Нацеливание аденозина для иммунотерапии рака 2018
- ^ Анти-CD73 в иммунотерапии рака: пробуждение новых возможностей 2016
- ^ Ghalamfarsa G, Kazemi MH, Raoofi Mohseni S, et al. (2019). «CD73 как потенциальная возможность для иммунотерапии рака». Expert Opin Ther Targets . 23 (2): 127– 142. doi :10.1080/14728222.2019.1559829. PMID 30556751. S2CID 58767911.
- ^ Антитело к CD73 кажется безопасным и показывает многообещающие результаты при лечении рака на поздних стадиях
- ^ Knight JS, Mazza LF, Yalavarthi S, et al. (2018). «Эктонуклеотидазоопосредованное подавление аутоиммунитета при волчанке и сосудистой дисфункции». Frontiers in Immunology . 9 : 1322. doi : 10.3389/fimmu.2018.01322 . PMC 6004379. PMID 29942314 .
- ^ abc Zhu J, Zeng Y, Li W, et al. (февраль 2017 г.). "CD73/NT5E является мишенью miR-30a-5p и играет важную роль в патогенезе немелкоклеточного рака легких". Molecular Cancer . 16 (1): 34. doi : 10.1186/s12943-017-0591-1 . PMC 5291990 . PMID 28158983.
- ^ Yu M, Guo G, Huang L и др. (январь 2020 г.). «2B-опосредованная прямая связь усиливает иммунную контрольную точку». Nature Communications . 11 (1): 515. doi :10.1038/s41467-019-14060-x. PMC 6981126 . PMID 31980601.
- ^ Трипати А., Лин Э., Нуссенцвейг Р. и др. (2019-05-20). «Экспрессия NT5E и иммунный ландшафт рака простаты (РПЖ): анализ из базы данных Атласа генома рака». Журнал клинической онкологии . 37 (15_suppl): e16591. doi :10.1200/JCO.2019.37.15_suppl.e16591. ISSN 0732-183X. S2CID 190909472.
- ^ Бажин А.В., Амедей А., Караханова С. (2018). «Редакционная статья: Молекулы иммунных контрольных точек и иммунотерапия рака». Границы в иммунологии . 9 : 2878. дои : 10.3389/fimmu.2018.02878 . ПМК 6290335 . ПМИД 30568661.
- ^ Zhang F, Luo Y, Shao Z и др. (апрель 2016 г.). «МикроРНК-187, нисходящий эффектор пути TGFβ, подавляет опосредованный Smad эпителиально-мезенхимальный переход при колоректальном раке». Cancer Letters . 373 (2): 203– 13. doi :10.1016/j.canlet.2016.01.037. PMID 26820227.
Дальнейшее чтение
- Resta R, Thompson LF (февраль 1997). "Сигнализация Т-клеток через CD73". Cellular Signalling . 9 (2): 131– 9. doi :10.1016/S0898-6568(96)00132-5. PMID 9113412.
- Кирхгофф К, Хейл Г (март 1996). «Перенос мембранных белков, закрепленных на гликозилфосфатидилинозитоле, из клетки в клетку во время созревания сперматозоидов». Молекулярная репродукция человека . 2 (3): 177–84 . doi : 10.1093/molehr/2.3.177 . PMID 9238677.
- Resta R, Yamashita Y, Thompson LF (февраль 1998 г.). "Эктоферментные и сигнальные функции лимфоцита CD73". Immunological Reviews . 161 : 95–109 . doi :10.1111/j.1600-065X.1998.tb01574.x. PMID 9553767. S2CID 29930691.
- Рози Ф., Карлуччи Ф., Маринелло Э. и др. (март 2002 г.). «Экто-5'-нуклеотидаза при В-клеточном хроническом лимфоцитарном лейкозе». Биомедицина и фармакотерапия . 56 (2): 100–4 . doi :10.1016/S0753-3322(01)00072-5. ПМИД 12000134.
- Бабийчук ЭБ, Дрэгер А (июнь 2006 г.). «Регуляция активности экто-5'-нуклеотидазы посредством Ca2+-зависимой, опосредованной аннексином 2 мембранной перестройки?». Труды биохимического общества . 34 (ч. 3): 374– 6. doi :10.1042/BST0340374. PMID 16709165. S2CID 8728207.
- Стефанович В., Мандель П., Розенберг А. (июль 1976 г.). «Экто-5'-нуклеотидаза интактных культивируемых клеток глиомы крысы C6». Журнал биологической химии . 251 (13): 3900– 5. doi : 10.1016/S0021-9258(17)33333-1 . PMID 819433.
- Thomson LF, Ruedi JM, Glass A и др. (январь 1990 г.). «Производство и характеристика моноклональных антител к гликозилфосфатидилинозитол-закрепленному антигену дифференцировки лимфоцитов экто-5'-нуклеотидазе (CD73)». Tissue Antigens . 35 (1): 9– 19. doi :10.1111/j.1399-0039.1990.tb01750.x. PMID 2137649.
- Клеменс MR, Шерман WR, Холмберг NJ и др. (ноябрь 1990 г.). «Характеристика растворимой и связанной с мембраной человеческой плацентарной 5'-нуклеотидазы». Biochemical and Biophysical Research Communications . 172 (3): 1371– 7. doi :10.1016/0006-291X(90)91601-N. PMID 2173922.
- Boyle JM, Hey Y, Guerts van Kessel A и др. (декабрь 1988 г.). «Присвоение экто-5'-нуклеотидазы человеческой хромосоме 6». Human Genetics . 81 (1): 88– 92. doi :10.1007/BF00283737. PMID 2848759. S2CID 22488106.
- Влахович П., Стефанович В. (1995). «Влияние дофамина на экспрессию экто-5'-нуклеотидазы в клубочковых мезангиальных клетках человека». Международные архивы физиологии, биохимии и биофизики . 102 (3): 171–3 . дои : 10.3109/13813459409007533. ПМИД 8000038.
- Hansen KR, Resta R, Webb CF и др. (декабрь 1995 г.). «Выделение и характеристика промотора гена, кодирующего 5'-нуклеотидазу (CD73) человека». Gene . 167 ( 1– 2): 307– 12. doi :10.1016/0378-1119(95)00574-9. PMID 8566797.
- Airas L, Jalkanen S (сентябрь 1996 г.). "CD73 опосредует адгезию В-клеток к фолликулярным дендритным клеткам". Blood . 88 (5): 1755– 64. doi : 10.1182/blood.V88.5.1755.1755 . PMID 8781432.
- Airas L, Niemelä J, Salmi M и др. (январь 1997 г.). «Дифференциальная регуляция и функция CD73, гликозил-фосфатидилинозитол-связанной 70-кДа адгезионной молекулы, на лимфоцитах и эндотелиальных клетках». Журнал клеточной биологии . 136 (2): 421– 31. doi :10.1083/jcb.136.2.421. PMC 2134816. PMID 9015312 .
- Strohmeier GR, Lencer WI, Patapoff TW и др. (июнь 1997 г.). «Поверхностная экспрессия, поляризация и функциональное значение CD73 в эпителии кишечника человека». Журнал клинических исследований . 99 (11): 2588– 601. doi :10.1172/JCI119447. PMC 508104. PMID 9169488 .
- Аумюллер Г., Реннеберг Х., Шиманн П.Дж. и др. (1997). «Роль апокриновых высвобожденных белков в посттестикулярной регуляции функции спермы человека». Судьба мужской половой клетки . Достижения экспериментальной медицины и биологии. Т. 424. С. 193–219 . doi :10.1007/978-1-4615-5913-9_39. ISBN 978-1-4613-7711-5. PMID 9361795.
- Rosi F, Agostinho AB, Carlucci F и др. (1998). «Поведение человеческих лимфоцитарных изоферментов 5'-нуклеотидазы». Life Sciences . 62 (25): 2257– 66. doi :10.1016/S0024-3205(98)00206-9. PMID 9651114.
Внешние ссылки
- NT5E+белок,+человек в рубриках медицинских предметов Национальной медицинской библиотеки США (MeSH)
- Обзор всей структурной информации, доступной в PDB для UniProt : P21589 (5′-нуклеотидаза) на сайте PDBe-KB .
В данной статье использован текст из Национальной медицинской библиотеки США , являющийся общественным достоянием .