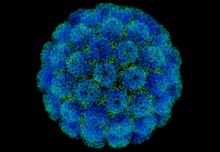
СВ40
| Вирус обезьян 40 | |
|---|---|
 | |
| Классификация вирусов | |
| (без рейтинга): | Вирус |
| Область : | Моноднавирия |
| Королевство: | Шотокувиры |
| Тип: | Коссавирикота |
| Сорт: | Паповавирицеты |
| Заказ: | Сеполивирусы |
| Семья: | Полиомавирусы |
| Род: | бетаполиомавирус |
| Разновидность: | |
| Вирус: | Вирус обезьян 40 |
| Синонимы | |
обезьяний вакуолизирующий вирус 40, SV40 | |
SV40 — это аббревиатура для simian vacuolating virus 40 или simian virus 40 , полиомавируса , который встречается как у обезьян , так и у людей . Как и другие полиомавирусы, SV40 — это ДНК-вирус , который, как установлено, вызывает опухоли у людей и животных, но чаще всего сохраняется в виде латентной инфекции. SV40 широко изучался как модельный эукариотический вирус, что привело ко многим ранним открытиям в области репликации эукариотической ДНК [1] и транскрипции . [2]
После заражения партий вакцины от полиомиелита в 1950-х и 1960-х годах, SV40 попал под подозрение как возможный риск рака, но последующего увеличения заболеваемости раком не наблюдалось, что делает такой риск маловероятным. Тем не менее, SV40 стал причиной скандала для активистов антивакцинального движения , которые обвиняли его во многих болезнях, включая рак и ВИЧ/СПИД . [3]
Болезнь человека
Гипотеза о том, что SV40 может вызывать рак у людей, была особенно спорной областью исследований, подогреваемой историческим загрязнением некоторых партий вакцины против полиомиелита SV40 в 1950-х и 1960-х годах. [4] «Убедительные доказательства теперь указывают на то, что SV40 вызывает инфекции у людей сегодня и представляет собой новый патоген». [5] Однако «маловероятно, что одного только заражения SV40 достаточно, чтобы вызвать злокачественное новообразование у человека...» [6]
повреждение p53 и канцерогенность
Было высказано предположение, что SV40 может действовать как сопутствующий канцероген вместе с крокидолитовым асбестом, вызывая мезотелиому . [7] [8]
Загрязнение вакцины от полиомиелита
Некоторые вакцины, произведенные в США между 1955 и 1961 годами, были загрязнены SV40 из питательной среды и исходного посевного штамма. Исследования на уровне популяции не показали обширных доказательств увеличения заболеваемости раком в результате воздействия, [9] хотя SV40 был широко изучен. [10] Тридцатипятилетнее последующее наблюдение не обнаружило избыточного числа раковых заболеваний, связанных с SV40. [11]
генная терапия
Из-за его высокой тканевости биотехнологические компании стремятся использовать модифицированные векторы на основе SV40 в качестве вирусного вектора для генной терапии . В этих векторах, полученных с помощью вируса-помощника или упаковочной клеточной линии, удаляются большой антиген T SV40 и малый антиген T SV40. [12] [13] [14]
Вирусология
SV40 состоит из безоболочечного икосаэдрического вириона с замкнутым кольцевым двухцепочечным ДНК-геномом [15] размером 5,2 кб. [16] Вирион прикрепляется к рецепторам клеточной поверхности MHC класса I с помощью вирионного гликопротеина VP1. Проникновение в клетку происходит через кавеолиновую везикулу . Внутри клеточного ядра клеточная РНК-полимераза II действует, способствуя ранней экспрессии генов. Это приводит к образованию мРНК , которая разделяется на два сегмента. В результате образуются малый и большой антигены T. Большой антиген T выполняет две функции: 5% направляется в плазматическую клеточную мембрану , а 95% возвращается в ядро. Попав в ядро, большой антиген T связывается с тремя вирусными сайтами ДНК, I, II и III. Связывание сайтов I и II саморегулирует ранний синтез РНК . Связывание с сайтом II происходит в каждом клеточном цикле. Сайт связывания I инициирует репликацию ДНК в точке начала репликации . Ранняя транскрипция дает две сплайсированные РНК, которые обе являются 19s. Поздняя транскрипция дает как более длинную 16s, которая синтезирует основной вирусный капсидный белок VP1; и меньшую 19s, которая дает VP2 и VP3 через утечку сканирования . Все белки, кроме 5% большого T, возвращаются в ядро, поскольку сборка вирусной частицы происходит там. Сообщалось, что предполагаемый поздний белок VP4 действует как виропорин, облегчая высвобождение вирусных частиц и приводя к цитолизу ; [17] [18] однако наличие и роль VP4 были оспорены. [19] [20]
Реактивация множественности
SV40 способен к множественной реактивации (МР). [21] [22] МР — это процесс, при котором два или более вирусных генома, содержащие в противном случае летальные повреждения, взаимодействуют внутри инфицированной клетки, образуя жизнеспособный вирусный геном. Ямамато и Шимоджо наблюдали МР, когда вирионы SV40 облучались УФ-светом и подвергались множественному заражению клеток-хозяев. [21] Холл изучал МР, когда вирионы SV 40 подвергались воздействию сшивающего агента ДНК 4, 5', 8-триметилпсоралена. [22] В условиях, когда в каждую клетку-хозяина проникала только одна вирусная частица, приблизительно одна сшивка ДНК была летальной для вируса и не могла быть восстановлена. Напротив, когда несколько вирусных геномов инфицировали клетку-хозяина, сшивки ДНК, вызванные псораленом , восстанавливались; то есть происходила МР. Холл предположил, что вирионы со сшитой ДНК были восстановлены путем рекомбинационной репарации. [22] Мишод и др. рассмотрели многочисленные примеры MR у различных вирусов и предположили, что MR является распространенной формой сексуального взаимодействия, которая обеспечивает преимущество рекомбинационного восстановления повреждений генома. [23]
Транскрипция
Ранний промотор для SV40 содержит три элемента. TATA-бокс расположен примерно на 20 пар оснований выше места начала транскрипции . 21 повтор пары оснований содержит шесть GC-боксов и является сайтом, который определяет направление транскрипции. Кроме того, 72 повтора пар оснований являются транскрипционными усилителями . Когда белок SP1 взаимодействует с 21 повтором пар оснований, он связывает либо первые, либо последние три GC-бокса. Связывание первых трех инициирует раннюю экспрессию , связывание последних трех инициирует позднюю экспрессию. Функция 72 повторов пар оснований заключается в увеличении количества стабильной РНК и увеличении скорости синтеза. Это делается путем связывания ( димеризации ) с фактором транскрипции AP-1, чтобы получить первичный транскрипт, который 3'- полиаденилирован и 5'-кэпирован. [ необходима цитата ]
Другие животные
SV40 находится в состоянии покоя и бессимптомен у макак-резусов . Вирус был обнаружен во многих популяциях макак в дикой природе, где он редко вызывает заболевания. Однако у обезьян с иммунодефицитом — например, из-за заражения вирусом иммунодефицита обезьян — SV40 действует во многом подобно человеческим полиомавирусам JC и BK , вызывая заболевание почек и иногда демиелинизирующее заболевание, похожее на прогрессирующую мультифокальную лейкоэнцефалопатию . У других видов, в частности хомяков , SV40 вызывает различные опухоли, в основном саркомы. У крыс онкогенный большой антиген T SV40 использовался для создания модели опухоли мозга для примитивной нейроэктодермальной опухоли и медуллобластомы . [24]
Молекулярные механизмы, посредством которых вирус воспроизводится и изменяет функции клеток, ранее были неизвестны, а исследования SV40 значительно расширили понимание биологами экспрессии генов и регуляции роста клеток. [ необходима цитата ]
История
SV40 был впервые идентифицирован Беном Свитом и Морисом Хиллеманом в 1960 году, когда они обнаружили, что от 10 до 30% вакцин против полиомиелита в США были загрязнены SV40. [25] В 1962 году Бернис Эдди описала онкогенную функцию SV40 , вызывающую саркому и эпендимомы у хомяков, инокулированных клетками обезьян, инфицированными SV40. [26] Полный вирусный геном был секвенирован Вайсманом в Йельском университете (США) [27] в 1978 году, а также Фирсом и его командой в Гентском университете ( Бельгия ). [28]
Культура и общество
SV40 стал культовой темой среди активистов антивакцинального движения , которые обвиняют его присутствие в зараженной вакцине в том, что оно является причиной «эпидемии» рака и ответственно за ВИЧ/СПИД . [3]
Смотрите также
Ссылки
- ^ Фаннинг, Э.; Чжао, К. (февраль 2009 г.). «Репликация ДНК SV40: от гена А до наномашины». Вирусология . 384 (2): 352–359 . doi :10.1016/j.virol.2008.11.038. PMC 2718763. PMID 19101707 .
- ^ Банерджи, Дж.; Рускони, С.; Шаффнер, В. (декабрь 1981 г.). «Экспрессия гена β-глобина усиливается удаленными последовательностями ДНК SV40». Cell . 27 (2): 299– 308. doi :10.1016/0092-8674(81)90413-X. PMID 6277502. S2CID 54234674.
- ^ ab Gorski DH (9 сентября 2013 г.). «Еще один мем о зомби-антивакцинистах: вакцина от полиомиелита, SV40 и рак, о, боже!». Science-Based Medicine .
- ^ Poulin, DL; Decaprio, JA (2006). «Имеет ли SV40 роль в развитии рака у человека?». Журнал клинической онкологии . 24 (26): 4356– 65. doi :10.1200/JCO.2005.03.7101. PMID 16963733.
- ^ Vilchez, Regis A.; Butel, Janet S. (июль 2004 г.). «Возникший человеческий патогенный вирус обезьян 40 и его роль в раке». Clinical Microbiology Reviews . 17 (3): 495– 508. doi : 10.1128/CMR.17.3.495-508.2004 . ISSN 0893-8512. PMC 452549. PMID 15258090. S2CID 10372679 .
- ^ Qi F, Carbone M, Yang H, Gaudino G (октябрь 2011 г.). «Трансформация вируса обезьян 40, злокачественная мезотелиома и опухоли мозга». Expert Rev Respir Med (обзор). 5 (5): 683–97 . doi :10.1586/ers.11.51. PMC 3241931 . PMID 21955238.
- ^ Kroczynska, Barbara; Cutrone, Rochelle; Bocchetta, Maurizio; Yang, Haining; Elmishad, Amira G.; Vacek, Pamela; Ramos-Nino, Maria; Mossman, Brooke T.; Pass, Harvey I.; Carbone, Michele (19 сентября 2006 г.). "Асбест Crocidolite и SV40 являются коканцерогенами в мезотелиальных клетках человека и вызывают мезотелиому у хомяков". Труды Национальной академии наук . 103 (38): 14128– 14133. Bibcode : 2006PNAS..10314128K. doi : 10.1073/pnas.0604544103 . PMC 1599923 . PMID 16966607.
- ^ Pershouse, Mark A.; Heivly, Shane; Girtsman, Teri (январь 2006 г.). «Роль SV40 в злокачественной мезотелиоме и других злокачественных новообразованиях человека». Inhalation Toxicology . 18 (12): 995–1000 . Bibcode : 2006InhTx..18..995P. doi : 10.1080/08958370600835377. PMID 16920674. S2CID 30590705.
- ^ «Исследования не обнаружили никаких доказательств того, что вирус обезьян 40 связан с раком человека». Science Daily (пресс-релиз). NIH/National Cancer Institute. 25 августа 2004 г.
- ^ Hilleman MR (1998). «Открытие вируса обезьян 40 (SV40) и его связь с вакцинами против вируса полиомиелита». Dev Biol Stand . 94 : 183–90 . PMID 9776239.
- ^ Кэрролл-Панкхерст, К.; Энгельс, Е.А.; Стриклер, Х.Д.; Годерт, Дж.Дж.; Вагнер, Дж.; Мортимер Е.А.-мл. (ноябрь 2001 г.). «Смертность в течение тридцати пяти лет после получения полиовакцины, загрязненной SV40, в неонатальный период». Br J Cancer . 85 (9): 1295–7 . doi :10.1054/bjoc.2001.2065. PMC 2375249. PMID 11720463 .
- ^ Mueller, C.; Strayer, MS; Sirninger, J.; Braag, S.; Branco, F.; Louboutin, J.-P.; Flotte, TR; Strayer, DS (февраль 2010 г.). "In vitro и in vivo функциональная характеристика векторов CFTR, полученных из рекомбинантного SV40 без рецепторов". Gene Therapy . 17 (2): 227– 237. doi :10.1038/gt.2009.137. PMC 2820588 . PMID 19890354.
- ^ Тоскано, Мигель Г.; ван дер Фельден, Йерун; ван дер Верф, Сибранд; Одейк, Махтелд; Роке, Ана; Камачо-Гарсия, Рафаэль Х.; Эррера-Гомес, Ирен Г.; Манчини, Ирен; де Хаан, Питер (15 сентября 2017 г.). «Создание линии упаковочных клеток на основе Vero для производства векторов доставки гена SV40 для использования в клинических исследованиях генной терапии». Молекулярная терапия. Методы и клинические разработки . 6 : 124–134 . doi :10.1016/j.omtm.2017.06.007. ПМК 5537168 . ПМИД 28791314.
- ^ Вера, Мария; Фортес, Пури (май 2004 г.). «Обезьяний вирус-40 как вектор генной терапии». ДНК и клеточная биология . 23 (5): 271– 282. doi :10.1089/104454904323090903. PMID 15169607.
- ^ Фаннинг, Э.; Чжао, К. (2009). «Репликация ДНК SV40: от гена А до наномашины». Вирусология . 384 (2): 352–359 . doi :10.1016/j.virol.2008.11.038. PMC 2718763. PMID 19101707 .
- ^ Sowd, GA; Fanning, E (2012). «Волк в овечьей шкуре: SV40 использует белки поддержания генома хозяина для репликации вирусной ДНК». PLOS Pathogens . 8 (11): e1002994. doi : 10.1371/journal.ppat.1002994 . PMC 3493471. PMID 23144614 .
- ^ Рагхава, Смита; Джорда, Кристина М.; Романо, Фабиан Б.; Хек, Алехандро П.; Хеберт, Дэниел Н. (30 июня 2011 г.). «Поздний белок VP4 вируса SV40 — это виропорин, который образует поры для разрушения мембран для высвобождения вирусов». Патогены PLOS . 7 (6): e1002116. doi : 10.1371/journal.ppat.1002116 . PMC 3128117. PMID 21738474 .
- ^ Декаприо, Джеймс А.; Гарсеа, Роберт Л. (апрель 2013 г.). «Рог изобилия человеческих полиомавирусов». Nature Reviews Microbiology . 11 (4): 264– 276. doi :10.1038/nrmicro2992. PMC 3928796. PMID 23474680.
- ^ Хенриксен, Стиан; Ринальдо, Кристин Ханссен (29 апреля 2020 г.). «Подтверждают ли доказательства существование виропорина полиомавируса обезьян SV40 Vp4?». mSphere . 5 (2): e00019-20. doi :10.1128/mSphere.00019-20. PMC 7082134 . PMID 32188744.
- ^ Дэниелс, Роберт; Хеберт, Дэниел Н. (29 апреля 2020 г.). «В поддержку полиомавируса обезьян 40 VP4 как позднее экспрессируемого виропорина». mSphere . 5 (2): e00187-20. doi :10.1128/mSphere.00187-20. PMC 7082142 . PMID 32188752.
- ^ ab Ямамото, Хироси; Симодзё, Х (август 1971 г.). «Множественная реактивация человеческого аденовируса типа 12 и обезьяньего вируса 40, облученного ультрафиолетовым светом». Вирусология . 45 (2): 529–31 . doi :10.1016/0042-6822(71)90355-2. PMID 4328814.
- ^ abc Hall, JD (1982). «Репарация псорален-индуцированных сшивок в клетках, многократно инфицированных SV40». Molecular & General Genetics . 188 (1): 135– 8. doi :10.1007/bf00333007. PMID 6294477. S2CID 5843939.
- ^ Michod, Richard E.; Bernstein, Harris; Nedelcu, Aurora M. (2008). «Адаптивное значение пола у микробных патогенов». Инфекция, генетика и эволюция . 8 (3): 267–85 . Bibcode :2008InfGE...8..267M. doi :10.1016/j.meegid.2008.01.002. PMID 18295550.
- ^ Eibl, RH; Kleihues, P; Jat, PS; Wiestler, OD (1994). «Модель примитивных нейроэктодермальных опухолей в трансгенных нейральных трансплантатах, содержащих большой антиген T SV40». The American Journal of Pathology . 144 (3): 556–64 . PMC 1887088. PMID 8129041 .
- ^ Sweet, BH; Hilleman, MR (ноябрь 1960). «Вакуолизирующий вирус, SV 40». Труды Общества экспериментальной биологии и медицины . 105 (2): 420– 427. doi :10.3181/00379727-105-26128. PMID 13774265. S2CID 38744505.
- ^ Эдди, BE; Борман, GS; Граббс, GE; Янг, RD (май 1962). «Идентификация онкогенного вещества в культуре клеток почек макаки-резуса как обезьяньего вируса 40». Вирусология . 17 : 65–75 . doi :10.1016/0042-6822(62)90082-x. PMID 13889129.
- ^ Reddy, VB; Weissman, SM (май 1978). «Геном вируса обезьян 40». Science . 200 (4341): 494– 502. Bibcode :1978Sci...200..494R. doi :10.1126/science.205947. PMID 205947.
- ^ Фирс, В; Контрерас, Р; Хагеманн, Г; Роджерс, Р; Ван Де Вурде, А; Ван Хеуверсвин, Х; Ван Херревеге, Дж; Волкарт, Г; Изеберт, М. (май 1978 г.). «Полная нуклеотидная последовательность ДНК SV40». Природа . 273 (5658): 113–20 . Бибкод : 1978Natur.273..113F. дои : 10.1038/273113a0. PMID 205802. S2CID 1634424.
Внешние ссылки
Часто задаваемые вопросы о CDC
- «Simian Virus 40 (SV40) - 1955 – 1963» в «Исторических проблемах безопасности». Безопасность вакцин . CDC. 30 марта 2022 г.
Другой
- Simian+virus+40 в рубриках медицинских предметов Национальной медицинской библиотеки США (MeSH)
- Запись SV40 в базе данных NCBI Taxonomy
- Запись SV40 в базе данных генома NCBI

