Молибденовая кислота
 | |
 | |
| Имена | |
|---|---|
| Другие имена Молибденовая(VI) кислота | |
| Идентификаторы | |
3D модель ( JSmol ) |
|
| ЧЭБИ |
|
| ChemSpider |
|
| Информационная карта ECHA | 100.029.063 |
| Номер ЕС |
|
| КЕГГ |
|
CID PubChem |
|
| УНИИ | |
Панель инструментов CompTox ( EPA ) |
|
| |
| |
| Характеристики | |
| MoO3 · H2O | |
| Молярная масса | 161,95 г моль −1 [1] |
| Появление | белые кристаллы (безводные) желтые кристаллы (моногидрат) |
| Плотность | 3,112 г/см 3 (безводный) 3,124 г/см 3 (моногидрат) |
| Температура плавления | 300 °C (572 °F; 573 К) [1] |
| 1510 мг дм −3 Растворим в 10% аммиаке 35 г/л | |
| Структура | |
| гексагональная (безводная) моноклинная (моногидрат) | |
| Опасности | |
| Маркировка СГС : [2] | |
  | |
| Предупреждение | |
| Н319 , Н335 , Н373 | |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |
Молибденовая кислота относится к гидратированным формам триоксида молибдена и родственным видам. Моногидрат (MoO 3 ·H 2 O) и дигидрат (MoO 3 ·2H 2 O) хорошо охарактеризованы. Это желтые диамагнитные твердые вещества.
Структура твердых тел

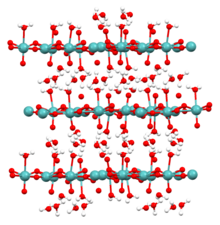
Твердые формы молибденовой кислоты являются координационными полимерами . Моногидрат MoO 3 ·H 2 O состоит из слоев октаэдрически координированных единиц MoO 5 ·(H 2 O), где 4 вершины являются общими. [3] Дигидрат (изображение показано выше) имеет ту же слоистую структуру с «дополнительной» молекулой H 2 O, вставленной между слоями. [4]
Структура молибденовой кислоты в растворе
В подкисленных водных растворах молибденовой кислоты наблюдается комплекс MoO 3 (H 2 O) 3. Молибден снова принимает октаэдрическую молекулярную геометрию , вероятно, с тремя оксолигандами и тремя акволигандами . [5]
Соли молибденовой кислоты называются молибдатами . Они возникают при добавлении основания к растворам молибденовой кислоты.
Приложения
Многие оксиды молибдена используются в качестве гетерогенных катализаторов , например, для окисления . Молибденовая кислота и ее соли используются для изготовления реактива Фреде для предположительной идентификации алкалоидов.
Ссылки
- ^ ab "Молибденовая кислота | 7782-91-4". Chemicalbook.com . Получено 2012-08-23 .
- ^ "C&L Inventory". echa.europa.eu .
- ^ Уэллс А.Ф. (1984) Структурная неорганическая химия 5-е издание Oxford Science Publications ISBN 0-19-855370-6
- ^ Кребс, Б. (1972). "Кристаллическая структура MoO3(H2O)2". Acta Crystallographica B. 28 ( 7): 2222– 2231. Bibcode :1972AcCrB..28.2222K. doi : 10.1107/S0567740872005849 .
- ^ Структура раствора молибденовой кислоты по данным Рамановской спектроскопии и анализа DFT, Oyerindea OF, Week CL, Anbarb AD, Spiro TG Inorganica Chimica Acta, 361, 4, (2008), 1000-1007, doi :10.1016/j.ica.2007.06.025
