Гемоглобин Хопкинс-2
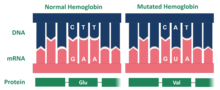
Гемоглобин Хопкинса-2 (Hb Hop-2) — это мутация белка гемоглобина , который отвечает за транспортировку кислорода через кровь от легких к мускулатуре тела у позвоночных. Специфическая мутация в гемоглобине Хопкинса-2 приводит к появлению двух аномальных α-цепей (человеческий гемоглобин состоит из 2 α- и 2 β-полипептидов, обычно называемых цепями). [1] Мутация является результатом замены гистидина 112 на аспарагиновую кислоту в полипептидной последовательности белка. [1] Кроме того, в одной из мутировавших альфа-цепей имеются замены в 114 и 118, двух точках на аминокислотной цепи. [2] Эта мутация может вызвать серповидноклеточную анемию . [3]
После первоначального открытия гемоглобина два исследователя, работавшие в больнице Джона Хопкинса в середине двадцатого века, Эрнест В. Смит и Дж. В. Торберт, обнаружили мутацию гемоглобина Хопкинса-2. [4] Работа Харви А. Итано и Элизабет А. Робинсон в 1960 году подтвердила открытие Смита и Торберта и подчеркнула важность альфа-локусов в мутации. [5] Позже в двадцатом веке Сэмюэль Шараш, другой ученый и врач, работавший в больнице Хопкинса, изучал физиологическое воздействие этого варианта на здоровье. [6] Его выводы свидетельствуют о том, что этот вариант не оказывает никакого клинического эффекта. [7]
История
В середине 1900-х годов многие факторы побудили исследования гемоглобина в Балтиморе, штат Мэриленд , и в конечном итоге привели к открытию гемоглобина Хопкинса-2. Во-первых, разработка новых технологий, включая рентгеновскую кристаллографию и химию белков, которые могли быть использованы в исследованиях молекулярной биологии, катализировала исследования. [8] Кроме того, широкое распространение талассемии (Hb H), заболевания, при котором ген альфа дисфункционален, в Юго-Восточной Азии и Южном Китае еще больше обеспокоило исследователей, поскольку, если ее не лечить, мутация может привести к деформации костей, отеку селезенки , замедлению темпов роста или сердечной дисфункции . [9] [10] Кроме того, открытие Максом Перуцем , исследователем из Кембриджа, основной третичной структуры гемоглобина в 1962 году катализировало исследования в области гематологии. [11] Исследования Вернона Ингрэма, посвященные серповидноклеточной анемии , в 1956 году показали, что варианты или мутации в РНК гемоглобина приводят к серповидноклеточной анемии . [8] [3]

Эрнест В. Смит и Дж. В. Норберт исследовали открытие Ингрэма и в 1958 году обнаружили мутацию гемоглобина Хопкинса-2. Смит и Торберт, научные сотрудники, работающие в исследовательском отделе гематологии Локкарда Конли в Университете Джонса Хопкинса, доказали, что рекомбинация неаллельных генов приводит к двум вариантам гена, который производит гемоглобин. Варианты «нормального» гена гемоглобина приводят к мутации в производимых гемоглобинах. [4] Другими словами, исследователи обнаружили две версии гемоглобина : [Hb-Hop2] и S варианты . [8]
Выводы Смита и Торберта были подтверждены и развиты Харви А. Итано и Элизабет А. Робинсон в 1960 году. В своей статье « Генетический контроль a- и B-цепей гемоглобина» Итано и Робинсон объяснили, что как альфа-, так и бета- локусы участвуют в регуляции гемоглобина. Рекомбинация альфа-локусов в гене, кодирующем гемоглобин, приводит к мутации белка гемоглобина. Исследователи называют этот мутировавший белок вариацией гемоглобина Хопкинса-2. [5]
Дальнейшие исследования, связанные с генетической мутацией Хопкинса-2, проводились врачами Университета Джонса Хопкинса, которые продолжали заниматься исследованиями в области гематологии, несмотря на общее изменение фокуса в медицинском сообществе от гематологии. Известный исследователь Хопкинса Сэмюэль Шараш был одним из многих ученых Хопкинса, которые исследовали кровь и ее компоненты в конце двадцатого века. [8] В частности, Шараш хорошо известен своей работой с Джорджем Довером, другим исследователем Хопкинса; вместе они открыли вариант лечения серповидноклеточной анемии . Однако Шараш также занимался исследованиями гемоглобина Хопкинса-2. В своей статье в журнале Nature под названием « Клинические исследования и физиологические свойства гемоглобина Хопкинса-2» Шараш объявил о своих открытиях, связанных с вариантом гемоглобина. Шараш сосредоточился на физических последствиях варианта, а не на самой генетике. В конечном счете, Шараш утверждает в своей статье, что вариант не является заметным фенотипически и оказывает незаметное или никакое влияние на здоровье человека. [ необходима ссылка ]
Гемоглобин и гематология в больнице Хопкинса

Гематологические исследования были заметны в больнице Джона Хопкинса до открытия варианта гемоглобина Хопкинса-2. После наблюдения за клетками под микроскопом сэр Уильям Ослер связал концепцию дисфункциональных тромбоцитов с развитием язвенного эндокардита и тромбоза . Первоначальные наблюдения Ослера за тромбоцитами послужили толчком к изучению крови и гематологии в больнице Хопкинса и в других исследовательских учреждениях. [12] Тромбоциты были открыты независимо Максом Шульце в 1865 году [13] и Г. Биццозеро в 1882 году. [14]
Начиная с 1920 года врачи больницы Джонса Хопкинса проводили исследования серповидноклеточной анемии или серповидноклеточной болезни. Хотя их выводы относительно этой болезни устарели, доктора Талиаферро и Хак обнаружили скрытую форму серповидноклеточной анемии. Их исследование серповидноклеточной анемии было первым из многих, проведенных в больнице Хопкинса. В 1940 году Ирвинг Шерман, студент-медик больницы Джонса Хопкинса, правильно определил дезоксигенацию гемоглобина у пациентов с серповидноклеточной болезнью после того, как он заметил характерные для дезоксигенации паттерны преломления при прохождении света через белок. [15] Дезоксигенация гемоглобина у пациентов с серповидноклеточной болезнью имеет серьезные последствия для тех, кто несет мутацию. Белки гемоглобина, присутствующие у людей с серповидноклеточной болезнью, не могут переносить кислород к органам и другим тканям человеческого тела. Это приводит к болевым кризисам , а болезнь приводит к сокращению продолжительности жизни на 40–60 лет. [16]
Эрнест В. Смит и Торберт сыграли важную роль в открытии гемоглобина Хопкинса-2, а также многих других гематологических мутаций и состояний. [4] Двое ученых работали вместе в Хопкинсе, чтобы идентифицировать мутацию N-Baltimore гемоглобина в 1958 году. [17] Также известная как мутация Хопкинса-I, Дженкинса, N-Мемфиса или Кенвуда, мутация N-Baltimore представляет собой точечную мутацию, в которой кодон глицина заменяется кодоном аденозина . Мутация N-Baltimore связана с мутациями C и S гемоглобина. [18]
Смит провел обширные исследования совместно с Локлардом Конли, одним из начальников Смита во время открытия варианта гемоглобина-2 Хопкинса. Локкард Конли, обычно называемый «Локом», был студентом университета Джонса Хопкинса и врачом, получившим образование в Колумбийском университете . В 1947 году Конли стал первым директором отделения гематологии в Хопкинсе и оставался на этой должности в течение 33 лет. Там он изучал заболевания, связанные с кровью, такие как свертывание крови и серповидноклеточная анемия , и изобрел оборудование для анализа молекулярных видов. [19] В частности, он и Смит создали устройство, которое позволило отделить варианты гемоглобина от стандартных молекул гемоглобина. Таким образом, влияние Конли на гематологию было не только научным открытием, но и технологическим открытием, которое позволило расширить область гематологии. [20] Конли оставался врачом и профессором в больнице Джона Хопкинса до своей смерти в 2010 году. [19]
Хотя значительное количество гематологических исследований было завершено в 1950-х и 1960-х годах, ученые задавались вопросом, можно ли провести больше исследований без разработки более передовых технологий. В конечном итоге, это сомнение привело к тому, что в середине двадцатого века меньше ученых занимались исследованиями в области гематологии. [8] Несмотря на нехватку исследователей, были сделаны новые открытия, связанные с генетикой и гемоглобином. Однако исследования продолжались в крупных медицинских лабораториях, таких как Хопкинс. [21]
В середине и конце двадцатого века оба доктора Джордж Дж. Довер и Сэмюэль Шараш изучали патологию серповидноклеточной анемии в больнице Джона Хопкинса. [7] Вместе они внедрили лечение заболевания с помощью противоракового препарата гидроксимочевины ; препарат успешно смягчил некоторые болезненные приступы, связанные с серповидноклеточной анемией , в дополнение к легочным симптомам, связанным с этим заболеванием. Довер, детский гематолог и эксперт по фетальному гемоглобину , инициировал использование белка в качестве способа лечения серповидноклеточной анемии у взрослых. [ необходима цитата ]
Медицинские последствия
Вариант гемоглобина Хопкинса-2 имеет сродство к кислороду в организме, что означает, что происходит увеличение распространения кислорода по организму из-за того, что Ho-2 переносит большее количество кислорода. [22] Нет эффекта эритроцитов с Ho-2 по сравнению с гемоглобином S , который изменяет форму клетки, становясь серповидной. Вариант гемоглобина Хопкинса-2 не участвует в формировании серповидных клеток . Отсутствует фенотипическое выражение Ho-2 в терминах серповидных клеток, поэтому человек с серповидными клетками и гемоглобином Хопкинса-2 будет бессимптомным. [ необходима цитата ]
Генетическая основа
Вариант гемоглобина Хопкинса 2 является результатом мутации. В частности, мутировавший белок состоит из двух альфа-цепей. Мутация для варианта гемоглобина Хопкинса-2 расположена на поверхности молекулы. В варианте Ho-2 аспарагиновая кислота заменяет гистидин в позиции 112 на альфа-цепи. [2] Доктор Макс Перуц исследовал аспарагиновую кислоту в альфа-112, утверждая, что карбоксильная группа аминокислоты образует водородную связь с фенольным гидроксилом, что, в свою очередь, стабилизирует структуру молекулы и увеличивает сродство к кислороду. Гемоглобин Ho-2 имеет высокий уровень кислорода, который восполняет недостаток кислорода в эритроцитах. Ho-2 похож на гемоглобин А , который является нормальным гемоглобином и также содержит две α-цепи. Это дает объяснение того, как вариант гемоглобина Хопкинса-2 связан с симптомами серповидноклеточной анемии . [ необходима ссылка ]
Hopkins-2 также может специфически взаимодействовать с гемоглобином S. Гемоглобин S является наиболее распространенным аномальным вариантом гемоглобина. Гемоглобин S является вариантом, который вызывает серповидноклеточную анемию , которая является заболеванием, при котором красные кровяные клетки разрушаются и приобретают аномальную форму. Гемоглобин S имеет две бета-цепи, тогда как гемоглобин Hopkins-2 имеет две альфа-цепи. Hopkins-2 составляет 22% гемолизатов у одиночных гетерозигот; следовательно, у этих пациентов наблюдается нормальная версия гена. Гемолизаты являются продуктами разрушения красных кровяных клеток. Ho-2 также составляет 11% гемолизатов у «двойных» гетерозигот, которые возникают, когда ген содержит как Hopkins-2, так и гемоглобин S. [23]
В настоящее время существует несколько возможных объяснений того, как работает вариант гемоглобина Хопкинс-2. Одно из объяснений, которое придумали ученые, заключается в том, что Ho-2 создается из-за точечной мутации, вызывающей замену гистидина аспарагиновой кислотой. [23] Другое объяснение заключается в том, что существует неравный кроссинговер между двумя генами α, который объясняет замену гистидина аспарагиновой кислотой. [23] Это затем привело к делеции, происходящей в хромосоме, содержащей Ho-2. Эта делеция удаляет область, где N-конец расположен в основной α-цепи, и где C-конец расположен в второстепенной α-цепи. [23] Делеция N-конца инактивирует ферменты и прекращает их способность разрезать цепи в определенных областях, что неизбежно повреждает цепь. [ необходима цитата ]
Примеры исследований
Исследования случаев были завершены на некоторых пациентах, которые были носителями генетической мутации гемоглобина Хопкинса-2 Сэмюэлем Шарачем и другими. Исследователи пришли к выводу после завершения исследований, что многие из носителей мутации были бессимптомны к серповидноклеточной анемии и были в целом вполне здоровы. Любые возникшие медицинские проблемы не имели никакой связи с серповидноклеточной анемией. Эти исследования проводились в 1970-х годах. [8]
Семья Фуллер-Карр
В семье Фуллера-Карра было пять носителей гемоглобина Хопкинса 2 и десять двойных гетерозигот Ho-2 и гемоглобина S. [24] Все носители были здоровы и имели нормальные результаты гематологических тестов. Из тех, кто имел гемоглобин S и Ho-2, никто не страдал анемией ; но у некоторых из обследованных наблюдалось повышенное количество ретикулоцитов. [24] Это измеряется с помощью анализа крови, который анализирует скорость выработки эритроцитов костным мозгом и их выброс в кровь. Не было никаких предположений о симптоматической серповидноклеточной анемии в семье. [ необходима цитата ]
Неизвестный ребенок
Было проведено исследование трехлетнего ребенка, который был носителем варианта гемоглобина Хопкинса-2. У ребенка была легкая анемия и ретикулоцитоз, что часто наблюдается при анемии. [25] Однако в крови не было обнаружено серповидных клеток, и у них не было симптомов, связанных с серповидноклеточной анемией. Также был снижен средний корпускулярный объем (MCV), который является средним объемом количества эритроцитов . [25]
Ссылки
- ^ ab Clegg JB, Charache S (1978). "Структура гемоглобина Хопкинса-2". Гемоглобин . 2 (1): 85– 8. doi :10.3109/03630267808999194. PMID 646867.
- ^ ab Rucknagel DL, Winter WP (ноябрь 1974). «Дупликация структурных генов для цепей альфа и бета гемоглобина у человека». Annals of the New York Academy of Sciences . 241 (1): 80– 92. Bibcode : 1974NYASA.241...80R. doi : 10.1111/j.1749-6632.1974.tb21868.x. hdl : 2027.42/73379 . PMID 4611311. S2CID 83499229.
- ^ ab Bloom M (1995). Понимание серповидноклеточной анемии . Соединенные Штаты: University Press of Mississippi. С. 3–6. ISBN 978-0878057450.
- ^ abc Hill RL, Swenson RT, Schwartz HC (ноябрь 1960). «Характеристика химической аномалии в гемоглобине G». Журнал биологической химии . 235 (11): 3182– 7. doi : 10.1016/S0021-9258(20)81333-7 . PMID 13714317.
- ^ ab Itano HA, Robinson EA (ноябрь 1960 г.). "ГЕНЕТИЧЕСКИЙ КОНТРОЛЬ АЛЬФА- И БЕТА-ЦЕПЕЙ ГЕМОГЛОБИНА". Труды Национальной академии наук Соединенных Штатов Америки . 46 (11): 1492– 501. Bibcode :1960PNAS...46.1492I. doi : 10.1073/pnas.46.11.1492 . PMC 223072 . PMID 16590776.
- ^ Sugg DK (31 января 1995 г.). «Хопкинс находит лечение серповидноклеточной анемии». The Baltimore Sun. Архивировано из оригинала 18 мая 2017 г. Получено 8 марта 2017 г.
- ^ ab Charache S, Ostertag W, von Ehrenstein G (декабрь 1971 г.). «Клинические исследования и физиологические свойства гемоглобина Хопкинса-2». Nature . 234 (51): 248– 51. doi :10.1038/newbio234248a0. PMID 5288820.
- ^ abcdef Weatherall, DJ (2001). «К молекулярной медицине; воспоминания о гемоглобиновой области, 1960-2000». British Journal of Haematology . 115 (4): 729–738 . doi : 10.1046/j.1365-2141.2001.03227.x . PMID 11843803.
- ^ "Что такое талассемия?". Детская больница UCSF Benioff . Получено 8 марта 2017 г.
- ^ "Симптомы и причины - Клиника Майо". Клиника Майо . Получено 15.04.2017 .
- ^ Стинсма Д.П., Шампо М.А., Кайл Р.А. (август 2015 г.). «Макс Перуц и структура гемоглобина». Труды клиники Майо . 90 (8): e89. doi : 10.1016/j.mayocp.2015.04.026 . PMID 26250737.
- ^ Stone MJ (октябрь 2003 г.). «Наследие Уильяма Ослера и его вклад в гематологию». British Journal of Haematology . 123 (1): 3– 18. doi : 10.1046/j.1365-2141.2003.04615.x . PMID 14510937. S2CID 211024.
- ^ Brewer DB (май 2006). «Макс Шульце (1865), Г. Биццозеро (1882) и открытие тромбоцитов». British Journal of Haematology . 133 (3): 251– 8. doi : 10.1111/j.1365-2141.2006.06036.x . PMID 16643426.
- ^ Рибатти Д., Кривеллато Э. (октябрь 2007 г.). «Джулио Биццозеро и открытие тромбоцитов». Исследования лейкемии . 31 (10): 1339–41 . doi :10.1016/j.leukres.2007.02.008. ПМИД 17383722.
- ^ "Открытие и биологическая основа". www.nslc.wustl.edu . Получено 2017-04-15 .
- ^ "Что такое серповидноклеточная анемия? - NHLBI, NIH". www.nhlbi.nih.gov . Получено 20 апреля 2017 г.
- ^ Лоренцо-Медина М., Де-Ла-Иглесия С., Роперо П., Ногейра-Салгейро П., Сантана-Бенитес Дж. (ноябрь 2014 г.). «Влияние вариантов гемоглобина на значения гемоглобина a1c, измеренные с использованием метода высокоэффективной жидкостной хроматографии». Журнал диабетической науки и технологии . 8 (6): 1168– 76. doi :10.1177/1932296814538774. PMC 4455477. PMID 25355712 .
- ^ "N-Baltimore.html". globin.bx.psu.edu . Получено 2017-03-30 .
- ^ ab "Медицинские архивы - Личные коллекции документов: Коллекция К. Локкарда Конли". www.medicalarchives.jhmi.edu . Получено 30.03.2017 .
- ^ "C. Lockard Lock Conley, MD (1915-2010)". www.hematology.org . 2010-04-27 . Получено 2017-03-30 .
- ^ Макканн С. (2016). История гематологии: от Геродота до ВИЧ . Oxford University Press. ISBN 978-0-19-102713-0.[ нужна страница ]
- ^ Хейсман, Титус Х. Дж., Марианна Ф. Х. Карвер и Георгий Ефремов. Программа вариантов человеческого гемоглобина (1996) . Огаста, Джорджия, США: Фонд серповидноклеточной анемии, 1996. Печать. [ нужна страница ]
- ^ abcd Ostertag W, von Ehrenstein G, Charache S (май 1972). «Дублированные гены альфа-цепи в гемоглобине Хопкинса-2 человека и доказательства неравного кроссинговера между ними». Nature . 237 (72): 90– 4. doi :10.1038/newbio237090a0. PMID 4503919.
- ^ ab Charache S, Ostertag W, von Ehrenstein G (май 1972). "Клинические исследования и физиологические свойства гемоглобина Хопкинса-2". Nature . 237 (72): 88– 90. doi :10.1038/newbio237088a0. PMID 4503918.
- ^ ab Steinberg, Martin H., et al. Нарушения гемоглобина: генетика, патофизиология и клиническое ведение . Cambridge University Press, 2009. [ нужна страница ]