Флуноксапрофен
 | |
 | |
| Клинические данные | |
|---|---|
| код АТС | |
| Идентификаторы | |
| |
| Номер CAS | |
| CID PubChem |
|
| ChemSpider | |
| УНИИ |
|
| КЕГГ | |
| ЧЭБИ | |
| ChEMBL | |
| Панель инструментов CompTox ( EPA ) |
|
| Химические и физические данные | |
| Формула | С 16 Н 12 Ф Н О 3 |
| Молярная масса | 285,274 г·моль −1 |
| 3D модель ( JSmol ) |
|
| |
 Н Н И (что это?) (проверить) И (что это?) (проверить) | |
Флуноксапрофен , также известный как Приаксим, является хиральным нестероидным противовоспалительным препаратом (НПВП). Он тесно связан с напроксеном , который также является НПВП. Было показано, что флуноксапрофен значительно улучшает симптомы остеоартрита и ревматоидного артрита . Клиническое использование флуноксапрофена прекращено из-за опасений потенциальной гепатотоксичности .
Структура
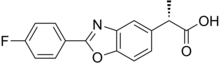
Флуноксапрофен — это двухкольцевое гетероциклическое соединение, полученное из бензоксазола . Он также содержит атом фтора и пропаноильную группу.
Синтез
Общий синтез аналогичен синтезу беноксапрофена ; в этом случае при формировании бензоксазольного кольца используется парафторбензоилхлорид.
Реакция Зандмейера путем диазотирования 2-(4-аминофенил)пропаннитрила (1) с последующим кислотным гидролизом приводит к фенолу (2), который нитруется и восстанавливается с использованием хлорида олова или каталитического гидрирования с получением аминофенола (4). Гидролиз нитрила дает карбоновую кислоту (5), которая преобразуется в рацемический флуноксапрофен путем ацилирования с помощью п- фторбензоилхлорида с последующей циклизацией . [1] [2] [3] [4]
Препараты
Поскольку флуноксапрофен имеет ограниченную растворимость в воде, необходимо предпринять дополнительные шаги для приготовления сиропов, кремов, суппозиториев и т. д. Чтобы сделать флуноксапрофен водорастворимым, но все еще активным и эффективным, его необходимо смешать с лизином , а затем суспендировать в органическом растворителе, который растворим в воде. Соль кристаллизуется при охлаждении. Затем соль необходимо отфильтровать и высушить. Фармакологическое тестирование этого теперь водорастворимого соединения показало, что оно обладает противовоспалительными свойствами, равными самому флуктапрофену. [5]
Фармакокинетика
Эффективность и безопасность флуноксапрофена сравнивались с эффективностью и безопасностью напроксена у пациентов с ревматоидным артритом , чтобы показать, что оба препарата имеют эквивалентные терапевтические эффекты. Оба препарата значительно облегчают спонтанную боль, которая возникает как днем, так и ночью. Оба препарата также значительно облегчают боль, связанную с активным и пассивным движением, и помогают облегчить утреннюю скованность. Исследование также показало, что оба препарата одинаково эффективны в улучшении силы захвата . [6]
Флуноксапрофен вводят в виде рацемата. Всасывание и распределение обоих энантиомеров были изучены в 1988 году. Не было обнаружено существенных различий между стереоизомерами в отношении их абсорбции и периода полувыведения. [7] Однако дальнейшие исследования показали, что S-энантиомер является фармакологически активной формой препарата и не подвергается стереоинверсии, в то время как R-флуноксапрофен фармакологически активируется посредством биотрансформации в S-энантиомер. [8] Эта стереоспецифическая хиральная инверсия опосредуется тиоэфиром FLX-S-Acyl-CoA. [9] Фармакокинетические исследования со стереоселективными биопробами были проведены на разных видах после дозировки рацемата (и производные энантиомера флуноксапрофена также использовались в качестве хиральных флуоресцентных дериватизирующих агентов для определения энантиомеров других энантиомеров препарата в плазме). [10]
Было показано, что правовращающая форма особенно активна и имеет гораздо более высокий терапевтический индекс , чем некоторые другие противовоспалительные средства, включая индометацин и диклофенак . [5] Также было показано, что флуноксапрофен ингибирует синтез лейкотриенов , а не простагландинов . Это похоже на беноксапрофен . Было показано, что флуноксапрофен и беноксапрофен имеют схожие характеристики абсорбции. Однако было показано, что распределение и выведение флукноксапрофена происходят намного быстрее, чем у беноксапрофена . [11]
Побочные эффекты
Структурным аналогом флуноксапрофена является беноксапрофен . Оба препарата являются аналогами карбоновых кислот, которые образуют реактивные ацилглюкурониды. Было показано, что беноксапрофен участвует в редких случаях гепатотоксичности. Из-за этого беноксапрофен был удален с рынка. В ответ на это клиническое использование флуноксапрофена также прекратилось, хотя исследования показали, что флуноксапрофен менее токсичен, чем беноксапрофен.
Токсичность этих нестероидных противовоспалительных препаратов может быть связана с ковалентной модификацией белков в ответ на реактивные ацилглюкурониды препаратов. Реактивность ацилглюкуронидов, по-видимому, совместно определяет степень связывания с белками [12] , как первоначально предполагалось исследовательской группой Бенета и др. в 1993 году.
Ссылки
- ^ DE 2324443, Эванс, Дельм; Данвелл, Дэвид Уильям и Хикс, Теренс Алан, «Производные бензоксазола и процессы их производства» [Производные бензоксазола и процессы их производства]», опубликовано 29 ноября 1973 г., передано Lilly Industries Ltd.
- ^ Д. Эванс и др., патент США 3,912,748 (1975, Eli Lilly ).
- ^ Данвелл Д.В., Эванс Д., Хикс ТА (январь 1975 г.). «Производные 2-арил-5-бензоксазолалкановой кислоты с заметной противовоспалительной активностью». Журнал медицинской химии . 18 (1): 53–58 . doi :10.1021/jm00235a012. PMID 1109576.
- ^ "Флуноксапрофен". Thieme . Получено 2024-07-09 .
- ^ ab "Процесс приготовления водорастворимых солей лизина (+)2-(4-фторфенил)-альфа-метил-5-бензоксазол уксусной кислоты" Патент США 5,120,851
- ^ Fioravanti A, Giordano N, Megale F, Jovane D, Franci A, Marcolongo R (1989). "[Эффективность и переносимость флуноксапрофена при лечении ревматоидного артрита. Перекрестное клиническое исследование с использованием напроксена]". La Clinica Terapeutica (на итальянском языке). 131 (2): 83–91 . PMID 2533024.
- ^ Palatini P, Montanari G, Perosa A, Forgione A, Pedrazzini S, Furlanut M (1988). «Стереоспецифическое распределение энантиомеров флуноксапрофена у людей». Международный журнал исследований клинической фармакологии . 8 (3): 161– 7. PMID 3403103.
- ^ Pedrazzini S, De Angelis M, Muciaccia WZ, Sacchi C, Forgione A (1988). «Стереохимическая фармакокинетика 2-арилпропионовой кислоты нестероидного противовоспалительного препарата флуноксапрофена у крыс и человека». Arzneimittel-Forschung . 38 (8): 1170– 5. PMID 3196413.
- ^ Grillo MP, Wait JC, Tadano Lohr M, Khera S, Benet LZ (2010). «Стереоселективное образование тиоэфира флукоксапрофена-S-ацил-глутатиона, опосредованное образованием ацил-КоА в гепатоцитах крыс». Drug Metabolism and Disposition . 38 (1): 133– 42. doi :10.1124/dmd.109.029371. PMC 2802421. PMID 19786506 .
- ^ Martin E, Quinke K, Spahn H, Mutschler E (1989). "(−)-(S)-флуноксапрофен и (−)-(S)-напроксен изоцианат: два новых флуоресцентных хиральных дериватизирующих агента для энантиоспецифического определения первичных и вторичных аминов". Хиральность . 1 (3): 223– 34. doi :10.1002/chir.530010308. PMID 2642051.
- ^ Furlanut M, Montanari G, Perosa A, Velussi C, Forgione A, Palatini P (1985). «Кинетика абсорбции и распределения флуноксапрофена и беноксапрофена у здоровых добровольцев». Международный журнал исследований клинической фармакологии . 5 (3): 165–70 . PMID 4018949.
- ^ Dong JQ, Liu J, Smith PC (2005). «Роль ацилглюкуронидов беноксапрофена и флуноксапрофена в ковалентном связывании с белками плазмы и печени крысы in vivo». Биохимическая фармакология . 70 (6): 937–48 . doi :10.1016/j.bcp.2005.05.026. PMID 16046212.
