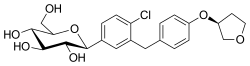
Эмпаглифлозин
 | |
| Клинические данные | |
|---|---|
| Торговые наименования | Джардинс, другие |
| Другие имена | БИ-10773 |
| AHFS / Drugs.com | Монография |
| МедлайнПлюс | а614043 |
| Данные лицензии |
|
Категория беременности |
|
| Пути введения | Через рот |
| Класс наркотиков | Ингибитор натрий-глюкозного котранспортера-2 (SGLT2) [2] |
| код АТС | |
| Правовой статус | |
| Правовой статус | |
| Идентификаторы | |
| |
| Номер CAS |
|
| CID PubChem |
|
| ИУФАР/БПС |
|
| DrugBank |
|
| ChemSpider |
|
| УНИИ |
|
| КЕГГ | |
| ХЭБИ | |
| ChEMBL |
|
| Панель инструментов CompTox ( EPA ) |
|
| Информационная карта ECHA | 100.122.058 |
| Химические и физические данные | |
| Формула | С23Н27ClО7 |
| Молярная масса | 450,91 г·моль −1 |
| 3D модель ( JSmol ) |
|
| |
| |
Эмпаглифлозин , продаваемый под торговой маркой Jardiance , среди прочего, является противодиабетическим препаратом, используемым для улучшения контроля уровня глюкозы у людей с диабетом 2 типа . [12] [2] [14] Он принимается внутрь . [2]
Распространенные побочные эффекты включают гипервентиляцию, анорексию, боли в животе, тошноту, рвоту, летаргию, изменения психического состояния, гипотонию, острое повреждение почек и вагинальные дрожжевые инфекции. [2] Более редкие, но более серьезные побочные эффекты включают инфекцию кожи паха, называемую гангреной Фурнье , и форму диабетического кетоацидоза с нормальным уровнем сахара в крови. [2] [15] Использование во время беременности или кормления грудью не рекомендуется. [16] Эмпаглифлозин иногда вызывает временное снижение функции почек, а в редких случаях вызывает острое повреждение почек , поэтому его использование следует контролировать у лиц с нарушением функции почек. Но некоторые испытания показали, что эмпаглифлозин можно использовать у людей с СКФ всего лишь 20 мл/мин/1,73 м², без увеличения неблагоприятных исходов для почек. [17] [18]
Было показано, что использование эмпаглифлозина улучшает результаты у людей с установленным сердечно-сосудистым заболеванием. [19] [17] Имеются данные высококачественных исследований о том, что эмпаглифлозин также может помочь замедлить скорость снижения функции почек. Независимо от статуса диабета, польза наблюдалась у людей с легкой, умеренной или тяжелой потерей функции почек. [20] [21] Люди, начавшие принимать эмпаглифлозин, могут сначала заметить снижение функции почек, прежде чем их скорость клубочковой фильтрации стабилизируется. [22] Наибольшая польза была продемонстрирована у тех, у кого была тяжелая потеря функции почек, более высокий риск ухудшения функции почек и фон диабета. [20]
Эмпаглифлозин является ингибитором натрий-глюкозного котранспортера-2 (SGLT-2) и действует за счет увеличения потери сахара с мочой . [2]
Эмпаглифлозин был одобрен для медицинского применения в Соединенных Штатах и Европейском союзе в 2014 году. [13] [23] [24] Он входит в Список основных лекарственных средств Всемирной организации здравоохранения . [25] В 2022 году он был 56-м наиболее часто назначаемым лекарством в Соединенных Штатах, с более чем 12 миллионами рецептов. [26] [27] Он получил одобрение в качестве дженерика от Управления по контролю за продуктами и лекарствами США (FDA). [28]
Медицинское применение
В Соединенных Штатах эмпаглифлозин показан для снижения риска сердечно-сосудистой смерти и госпитализации по поводу сердечной недостаточности у взрослых с сердечной недостаточностью; [12] для снижения риска устойчивого снижения СКФ, терминальной стадии заболевания почек, сердечно-сосудистой смерти и госпитализации у взрослых с хроническим заболеванием почек с риском прогрессирования; [12] для снижения риска сердечно-сосудистой смерти у взрослых с диабетом 2 типа и установленным сердечно-сосудистым заболеванием; [12] и в качестве дополнения к диете и физическим упражнениям для улучшения гликемического контроля у людей в возрасте десяти лет и старше с диабетом 2 типа. [12]
В Европейском союзе эмпаглифлозин показан людям в возрасте от десяти лет и старше для лечения недостаточно контролируемого диабета 2 типа в качестве дополнения к диете и физическим упражнениям; [13] в качестве монотерапии, когда метформин считается неподходящим из-за непереносимости; [13] в дополнение к другим лекарственным средствам для лечения диабета. [13] Он показан взрослым для лечения симптоматической хронической сердечной недостаточности; [13] и он показан взрослым для лечения хронической болезни почек. [13]
Эмпаглифлозин снижает риск госпитализации и смерти у людей со сниженной функцией сердца при добавлении к стандартному лечению сердечной недостаточности с диабетом 2 типа или без него. [29] [30] [31] Он показан взрослым с диабетом 2 типа и установленным сердечно-сосудистым заболеванием для снижения риска сердечно-сосудистой смерти; а также в качестве дополнения к диете и физическим упражнениям для улучшения гликемического контроля у взрослых с диабетом 2 типа. [12] [32] [33]
В июне 2023 года Управление по контролю за продуктами и лекарствами США (FDA) расширило показания к применению препарата в качестве дополнения к диете и физическим упражнениям для улучшения контроля уровня сахара в крови у детей в возрасте 10 лет и старше с диабетом 2 типа. [34]
Противопоказания
- История тяжелой аллергической реакции на эмпаглифлозин [12]
- Терминальная стадия заболевания почек [12]
- Диабетический кетоацидоз [12]
Побочные эффекты
Общий
- Эмпаглифлозин увеличивает риск генитальных грибковых инфекций. Риск наиболее высок у людей с предшествующей историей генитальных грибковых инфекций. [35]
- Считалось, что эмпаглифлозин связан с повышенным риском инфекций мочевыводящих путей . Обзоры клинических испытаний показали, что нет значительного риска развития инфекций мочевыводящих путей при приеме эмпаглифлозина по сравнению с плацебо или другими диабетическими препаратами. [36] [37]
- Эмпаглифлозин снижает систолическое и диастолическое артериальное давление и может увеличить риск низкого артериального давления , что может привести к обморокам и/или падениям. [35] Риск выше у пожилых людей, людей, принимающих диуретики , и людей со сниженной функцией почек. [35]
- Небольшое повышение уровня холестерина липопротеинов низкой плотности (ЛПНП) может наблюдаться при приеме эмпаглифлозина в диапазоне 2–4% от исходного уровня. [35]
Серьезный
- Диабетический кетоацидоз , редкое, но потенциально опасное для жизни состояние, может чаще возникать при приеме эмпаглифлозина и других ингибиторов SGLT-2. [38] [39] Хотя диабетический кетоацидоз обычно связан с повышенным уровнем глюкозы в крови, у людей, принимающих ингибиторы SGLT-2, диабетический кетоацидоз может наблюдаться при нехарактерно нормальном уровне глюкозы в крови, явление, называемое эугликемическим диабетическим кетоацидозом. [38] Отсутствие повышенного уровня глюкозы в крови у людей, принимающих ингибиторы SGLT-2, может затруднить диагностику диабетического кетоацидоза. Риск эугликемического диабетического кетоацидоза, связанного с эмпаглифлозином, может быть выше в условиях болезни, обезвоживания, хирургического вмешательства и/или употребления алкоголя. [38] Это также наблюдается у больных диабетом 1 типа, принимающих эмпаглифлозин, что, в частности, является неодобренным или «не по назначению» применением препарата. [39] Чтобы снизить риск развития кетоацидоза (серьезного состояния, при котором организм вырабатывает высокие уровни кислот крови, называемых кетонами) после операции, FDA одобрило изменения в инструкции по назначению лекарств от диабета с ингибиторами SGLT2, чтобы рекомендовать временное прекращение их приема перед запланированной операцией. Прием эмпаглифлозина следует прекратить как минимум за три дня до запланированной операции. [40] Симптомы диабетического кетоацидоза включают тошноту, рвоту, боли в животе, усталость и затрудненное дыхание. [40]
- Гангрена Фурнье , редкая, но серьезная инфекция паха, чаще встречается у людей, принимающих эмпаглифлозин и другие ингибиторы SGLT-2. [2] [15] Симптомы включают лихорадку, общее недомогание и боль или отек вокруг гениталий или кожи позади них. Инфекция быстро прогрессирует, и рекомендуется срочная медицинская помощь. [15]
- Эмпаглифлозин может увеличить риск низкого уровня сахара в крови при использовании вместе с сульфонилмочевиной или инсулином. [41] При использовании отдельно или в сочетании с метформином он, по-видимому, не увеличивает риск гипогликемии. [42]
Механизм действия
Эмпаглифлозин является ингибитором натрийглюкозного котранспортера-2 (SGLT-2), который обнаруживается почти исключительно в проксимальных канальцах нефронных компонентов почек. SGLT-2 отвечает примерно за 90 процентов реабсорбции глюкозы в кровь. Блокирование SGLT-2 снижает уровень глюкозы в крови, блокируя реабсорбцию глюкозы в почках и тем самым выводя глюкозу (т. е. сахар крови) через мочу. [43] [44] [45] Из всех доступных в настоящее время ингибиторов SGLT-2 эмпаглифлозин имеет самую высокую степень селективности к SGLT-2 по сравнению с SGLT-1, SGLT-4, SGLT-5 и SGLT-6. [46]
История
Он был разработан компанией Boehringer Ingelheim и продается совместно с Eli Lilly and Company . Он также доступен в виде фиксированных комбинаций эмпаглифлозин/линаглиптин , [47] эмпаглифлозин/метформин , [48] и эмпаглифлозин/линаглиптин/метформин . [49]
В отношении сердечно-сосудистой смерти FDA основывало свое решение на пострегистрационном исследовании, которое оно потребовало, когда одобрило эмпаглифлозин в 2014 году в качестве дополнения к диете и физическим упражнениям для улучшения гликемического контроля у взрослых с диабетом 2 типа. [23] [32] Эмпаглифлозин изучался в пострегистрационном клиническом исследовании с участием более 7000 участников с диабетом 2 типа и сердечно-сосудистыми заболеваниями. [32] В ходе исследования было показано, что эмпаглифлозин снижает риск сердечно-сосудистой смерти по сравнению с плацебо при добавлении к стандартной терапии диабета и атеросклеротических сердечно-сосудистых заболеваний. [32]
При сердечной недостаточности безопасность и эффективность эмпаглифлозина были оценены FDA в качестве дополнения к стандартной терапии в рандомизированном двойном слепом международном исследовании, сравнивающем 2997 участников, получавших эмпаглифлозин в дозе 10 мг один раз в день, с 2991 участником, получавшим плацебо. [33] Основным измерением эффективности было время до смерти от сердечно-сосудистых причин или необходимости госпитализации из-за сердечной недостаточности. [33] Из лиц, получавших эмпаглифлозин в среднем около двух лет, 14% умерли от сердечно-сосудистых причин или были госпитализированы из-за сердечной недостаточности, по сравнению с 17% участников, получавших плацебо. [33] Это преимущество было в основном связано с меньшим количеством участников, госпитализированных из-за сердечной недостаточности. [33]
FDA удовлетворило заявку на приоритетное рассмотрение эмпаглифлозина и предоставило одобрение Jardiance компании Boehringer Ingelheim. [33]
Правовой статус
По состоянию на май 2013 года компании Boehringer и Lilly подали заявки на получение разрешения на продажу в Европейское агентство по лекарственным средствам (EMA) и Управление по контролю за продуктами и лекарствами США (FDA). [50] Эмпаглифлозин был одобрен в Европейском союзе в мае 2014 года, [13] а в Соединенных Штатах — в августе 2014 года. [23] [24] [51] FDA потребовало четыре пострегистрационных исследования: исследование сердечно-сосудистых исходов, два исследования на детях и исследование токсичности на животных, связанных с испытаниями на детях. [23] [51] [ требуется обновление ]
Исследовать
Метаанализ краткосрочных рандомизированных контролируемых испытаний показал схожую эффективность в отношении гликемического контроля между эмпаглифлозином 10 мг и 25 мг у людей с диабетом 2 типа. Хотя может быть более сильное снижение HbA1c при более высоких дозах, эта разница более клинически значима, когда исходный уровень HbA1c у пациентов составляет ≥ 8,5%. [52] [53]
Вес и артериальное давление
Эмпаглифлозин вызывает умеренное снижение артериального давления и массы тела. Эти эффекты, вероятно, обусловлены выделением глюкозы с мочой и небольшим увеличением выделения натрия с мочой . [35] [54]
В клинических испытаниях участники с диабетом 2 типа, принимавшие эмпаглифлозин с другими диабетическими препаратами, потеряли в среднем 2% от своего исходного веса . [55] [56] Более высокий процент людей, принимавших эмпаглифлозин, достигал потери веса более чем на 5% от своего исходного уровня, что было связано с улучшением контроля уровня глюкозы. [55] [56] [35] Такая же степень потери веса наблюдалась и в исследовании с участием пациентов с сердечной недостаточностью, принимавших эмпаглифлозин. [57]
Было показано, что эмпаглифлозин снижает систолическое артериальное давление на 3–5 миллиметров ртутного столба (мм рт. ст.) без изменения частоты пульса. [55] [56] [35] Больший процент людей с неконтролируемым артериальным давлением на исходном уровне достиг контролируемого артериального давления (т. е. систолического артериального давления <130 мм рт. ст. и диастолического артериального давления <80 мм рт. ст.) после приема эмпаглифлозина в течение 24 недель. [56] Влияние на артериальное давление и массу тела в целом рассматривается как благоприятное, поскольку многие люди с диабетом 2 типа имеют высокое артериальное давление или избыточный вес или ожирение. [42] [58]
Ссылки
- ^ "Использование Эмпаглифлозина (Джардианс) во время беременности". Drugs.com . 30 августа 2018 г. Архивировано из оригинала 5 августа 2019 г. Получено 10 февраля 2020 г.
- ^ abcdefg "Empagliflozin Monograph for Professionals". Drugs.com . AHFS. Архивировано из оригинала 6 апреля 2019 г. Получено 21 декабря 2018 г.
- ^ "AusPAR: Empagliflozin". Therapeutic Goods Administration (TGA), Commonwealth of Australia . 8 ноября 2017 г. Получено 24 марта 2022 г.
- ^ "Jardiance". Boehringer Ingelheim Pty Ltd. Управление по контролю за товарами терапевтического назначения (TGA), Австралийское Содружество. Архивировано из оригинала 18 марта 2023 г.
- ^ "Рецептурные лекарства: регистрация новых химических веществ в Австралии, 2014". Therapeutic Goods Administration (TGA), Commonwealth of Australia . 21 июня 2022 г. Архивировано из оригинала 10 апреля 2023 г. Получено 10 апреля 2023 г.
- ^ "Рецептурные лекарства и биологические препараты: ежегодный отчет TGA за 2017 год". Управление по контролю за товарами терапевтического назначения (TGA), Австралийское содружество . 21 июня 2022 г. Получено 31 марта 2024 г.
- ^ "Health Canada New Drug Authorizations: 2015 Highlights". Health Canada . 4 мая 2016 г. Получено 7 апреля 2024 г.
- ^ "Информация о продукте Jardiance". Health Canada . 11 августа 2015 г. Получено 8 сентября 2024 г.
- ^ "Информация о продукте Jardiance". Health Canada . 11 августа 2015 г. Получено 8 сентября 2024 г.
- ^ "Jardiance 10 мг таблетки, покрытые пленочной оболочкой – Краткое описание характеристик продукта (SmPC)". (emc) . Архивировано из оригинала 20 сентября 2020 г. . Получено 10 февраля 2020 г. .
- ^ "Jardiance 25 мг таблетки, покрытые пленочной оболочкой – Краткое описание характеристик продукта (SmPC)". (emc) . 23 октября 2019 г. Архивировано из оригинала 22 сентября 2020 г. Получено 10 февраля 2020 г.
- ^ abcdefghij "Jardiance- empagliflozin tablet, film coated". DailyMed . 22 января 2020 г. Архивировано из оригинала 11 февраля 2020 г. Получено 10 февраля 2020 г.
- ^ abcdefgh "Jardiance EPAR". Европейское агентство по лекарственным средствам (EMA) . 16 июня 2014 г. Архивировано из оригинала 28 августа 2021 г. Получено 10 февраля 2020 г.Текст был скопирован из этого источника, авторские права на который принадлежат Европейскому агентству по лекарственным средствам. Воспроизведение разрешено при условии указания источника.
- ^ Davies MJ, D'Alessio DA, Fradkin J, Kernan WN, Mathieu C, Mingrone G и др. (декабрь 2018 г.). «Управление гипергликемией при диабете 2 типа, 2018 г. Консенсусный отчет Американской диабетической ассоциации (ADA) и Европейской ассоциации по изучению диабета (EASD)». Diabetologia . 61 (12): 2461–2498. doi : 10.1007/s00125-018-4729-5 . PMID 30288571.
- ^ abc "FDA предупреждает о редких случаях серьезной инфекции половой области при приеме ингибиторов SGLT2 при диабете". Управление по контролю за продуктами и лекарствами США (FDA) . 9 февраля 2019 г. Архивировано из оригинала 13 декабря 2019 г. Получено 18 марта 2019 г.
- ^ Британский национальный формуляр: BNF 76 (76-е изд.). Pharmaceutical Press. 2018. стр. 691. ISBN 9780857113382.
- ^ ab Заннад Ф., Батлер Дж., Филиппатос Г.С., Покок С., Джамал В., Шни Дж. и др. (май 2021 г.). «Исходы сердечно-сосудистой системы и почек при применении эмпаглифлозина при сердечной недостаточности». Präzisionsmedizin – Eine Reise in die Zukunft der Diabetologie www.diabeteskongress.de . 16 . Георг Тиме Верлаг КГ. дои : 10.1055/s-0041-1727471.
- ^ Herrington WG, Staplin N, Wanner C, Green JB, Hauske SJ, Emberson JR и др. (январь 2023 г.). «Эмпаглифлозин у пациентов с хронической болезнью почек». The New England Journal of Medicine . 388 (2): 117–127 . doi :10.1056/NEJMoa2204233. PMC 7614055. PMID 36331190.
- ^ Zinman B, Wanner C, Lachin JM, Fitchett D, Bluhmki E, Hantel S и др. (ноябрь 2015 г.). «Эмпаглифлозин, сердечно-сосудистые исходы и смертность при диабете 2 типа». The New England Journal of Medicine . 373 (22): 2117–2128. doi :10.1056/NEJMoa1504720. PMID 26378978.
- ^ ab Herrington WG, Preiss D, Haynes R, von Eynatten M, Staplin N, Hauske SJ и др. (август 2020 г.). «Erratum: Потенциал улучшения кардиоренальных исходов путем ингибирования натрий-глюкозного котранспортера-2 у людей с хронической болезнью почек: обоснование исследования EMPA-KIDNEY». Clinical Kidney Journal . 13 (4): 722. doi :10.1056/NEJMoa2204233. hdl : 20.500.13003/18576 . PMC 7467589 . PMID 32905262.
- ^ Ваннер С., Инзукки С.Е., Лачин Дж.М., Фитчетт Д., фон Эйнаттен М., Маттеус М. и др. (июль 2016 г.). «Эмпаглифлозин и прогрессирование заболевания почек при диабете 2 типа». Медицинский журнал Новой Англии . 375 (4): 323–334. дои : 10.1056/nejmoa1515920. ПМИД 27299675.
- ^ Ваннер С., Инзукки С.Е., Лачин Дж.М., Фитчетт Д., фон Эйнаттен М., Маттеус М. и др. (июль 2016 г.). «Эмпаглифлозин и прогрессирование заболевания почек при диабете 2 типа». Медицинский журнал Новой Англии . 375 (4): 323–334. doi : 10.1056/NEJMoa1515920. ПМИД 27299675.
- ^ abcd "FDA одобряет препарат Jardiance для лечения диабета 2 типа" (пресс-релиз). Управление по контролю за продуктами и лекарствами США (FDA). 1 августа 2014 г. Архивировано из оригинала 22 октября 2016 г. Получено 5 февраля 2023 г.
 В данной статье использован текст из этого источника, находящегося в общественном достоянии .
В данной статье использован текст из этого источника, находящегося в общественном достоянии . - ^ ab "Пакет одобрения препарата: таблетки Jardiance (эмпаглифлозин) NDA #204629". Управление по контролю за продуктами и лекарствами США (FDA) . 8 сентября 2014 г. Архивировано из оригинала 11 февраля 2020 г. Получено 10 февраля 2020 г.
- ^ Всемирная организация здравоохранения (2023). Выбор и использование основных лекарственных средств 2023: веб-приложение A: Модельный список основных лекарственных средств Всемирной организации здравоохранения: 23-й список (2023) . Женева: Всемирная организация здравоохранения. hdl : 10665/371090 . WHO/MHP/HPS/EML/2023.02.
- ^ "Топ-300 2022 года". ClinCalc . Архивировано из оригинала 30 августа 2024 года . Получено 30 августа 2024 года .
- ^ "Статистика использования препарата Эмпаглифлозин, США, 2013–2022 гг.". ClinCalc . Получено 30 августа 2024 г. .
- ^ "2022 First Generic Drug Approvals". Управление по контролю за продуктами и лекарствами США (FDA). 3 марта 2023 г. Архивировано из оригинала 14 января 2024 г. Получено 14 января 2024 г.
- ^ Packer M, Anker SD, Butler J, Filippatos G, Pocock SJ, Carson P и др. (октябрь 2020 г.). «Сердечно-сосудистые и почечные исходы при применении эмпаглифлозина при сердечной недостаточности». The New England Journal of Medicine . 383 (15): 1413–1424. doi : 10.1056/NEJMoa2022190. hdl : 2066/230126 . PMID 32865377.
- ^ Anker SD, Butler J, Filippatos G, Ferreira JP, Bocchi E, Böhm M и др. (октябрь 2021 г.). «Эмпаглифлозин при сердечной недостаточности с сохраненной фракцией выброса». The New England Journal of Medicine . 385 (16): 1451–1461. doi : 10.1056/NEJMoa2107038. PMID 34449189.
- ^ Zannad F, Ferreira JP, Pocock SJ, Anker SD, Butler J, Filippatos G и др. (сентябрь 2020 г.). «Ингибиторы SGLT2 у пациентов с сердечной недостаточностью со сниженной фракцией выброса: метаанализ исследований EMPEROR-Reduced и DAPA-HF». Lancet . 396 (10254): 819–829. doi :10.1016/s0140-6736(20)31824-9. PMID 32877652.
- ^ abcd "FDA одобряет препарат Jardiance для снижения сердечно-сосудистой смертности у взрослых с диабетом 2 типа" (пресс-релиз). Управление по контролю за продуктами и лекарствами США (FDA). 6 декабря 2016 г. Архивировано из оригинала 11 февраля 2020 г. Получено 12 декабря 2016 г.
 В данной статье использован текст из этого источника, находящегося в общественном достоянии .
В данной статье использован текст из этого источника, находящегося в общественном достоянии . - ^ abcdef "FDA одобряет лечение более широкого круга пациентов с сердечной недостаточностью" (пресс-релиз). Управление по контролю за продуктами и лекарствами США (FDA). 24 февраля 2022 г. Архивировано из оригинала 27 февраля 2022 г. Получено 27 февраля 2022 г.
 В данной статье использован текст из этого источника, находящегося в общественном достоянии .
В данной статье использован текст из этого источника, находящегося в общественном достоянии . - ^ "FDA одобряет новый класс лекарств для лечения детского диабета 2 типа". Управление по контролю за продуктами и лекарствами США (FDA) (пресс-релиз). 20 июня 2023 г. Архивировано из оригинала 21 июня 2023 г. Получено 20 июня 2023 г.
- ^ abcdefg "Empagliflozin (Jardiance) National Drug Monograph" (PDF) . Министерство по делам ветеранов США . Октябрь 2015 г. Архивировано из оригинала (PDF) 18 марта 2021 г.
- ^ Donnan JR, Grandy CA, Chibrikov E, Marra CA, Aubrey-Bassler K, Johnston K и др. (февраль 2019 г.). «Сравнительная безопасность ингибиторов натрий-глюкозного котранспортера 2 (SGLT2): систематический обзор и метаанализ». BMJ Open . 9 (1): e022577. doi :10.1136/bmjopen-2018-022577. PMC 6361337 . PMID 30813108.
- ^ Kinduryte Schorling O, Clark D, Zwiener I, Kaspers S, Lee J, Iliev H (август 2020 г.). «Объединенный анализ безопасности и переносимости эмпаглифлозина у пациентов с сахарным диабетом 2 типа». Advances in Therapy . 37 (8): 3463–3484. doi :10.1007/s12325-020-01329-7. PMC 7370973. PMID 32372290 .
- ^ abc Rosenstock J, Ferrannini E (сентябрь 2015 г.). «Эугликемический диабетический кетоацидоз: предсказуемая, обнаруживаемая и предотвратимая проблема безопасности с ингибиторами SGLT2». Diabetes Care . 38 (9): 1638–1642. doi : 10.2337/dc15-1380 . PMID 26294774.
- ^ ab Handelsman Y, Henry RR, Bloomgarden ZT, Dagogo-Jack S, DeFronzo RA, Einhorn D, et al. (Июнь 2016 г.). «Заявление о позиции Американской ассоциации клинических эндокринологов и Американского колледжа эндокринологии по поводу связи ингибиторов Sglt-2 и диабетического кетоацидоза». Endocrine Practice . 22 (6): 753–762. doi : 10.4158/EP161292.PS . PMID 27082665.
- ^ ab "FDA пересматривает этикетки ингибиторов SGLT2 для лечения диабета, чтобы включить предупреждение". Управление по контролю за продуктами и лекарствами США (FDA). 19 марта 2020 г. Архивировано из оригинала 7 июня 2020 г. Получено 6 июня 2020 г.
 В данной статье использован текст из этого источника, находящегося в общественном достоянии .
В данной статье использован текст из этого источника, находящегося в общественном достоянии . - ^ "Эмпаглифлозин в комбинированной терапии для лечения диабета 2 типа". NICE . 25 марта 2015 г. Архивировано из оригинала 21 декабря 2018 г. Получено 21 декабря 2018 г.
- ^ ab Anderson JE, Wright EE, Shaefer CF (февраль 2017 г.). «Эмпаглифлозин: роль в вариантах лечения пациентов с сахарным диабетом 2 типа». Терапия диабета . 8 (1): 33–53. doi :10.1007/s13300-016-0211-x. PMC 5306110. PMID 27837465 .
- ^ Абдул-Гани МА, ДеФронзо РА (сентябрь 2008 г.). «Ингибирование реабсорбции глюкозы в почках: новая стратегия достижения контроля глюкозы при сахарном диабете 2 типа». Эндокринная практика . 14 (6): 782–790. doi :10.4158/ep.14.6.782. PMID 18996802.
- ^ Nair S, Wilding JP (январь 2010 г.). «Ингибиторы натрий-глюкозного котранспортера 2 как новое лечение сахарного диабета». Журнал клинической эндокринологии и метаболизма . 95 (1): 34–42. doi : 10.1210/jc.2009-0473 . PMID 19892839.
- ^ Bays H (март 2009). «От жертвы к союзнику: почка как новая цель для лечения сахарного диабета». Current Medical Research and Opinion . 25 (3): 671–681. doi :10.1185/03007990802710422. PMID 19232040. S2CID 73341491.
- ^ Tentolouris A, Vlachakis P, Tzeravini E, Eleftheriadou I, Tentolouris N (август 2019 г.). «Ингибиторы SGLT2: обзор их антидиабетических и кардиопротекторных эффектов». Международный журнал исследований окружающей среды и общественного здравоохранения . 16 (16): 2965. doi : 10.3390/ijerph16162965 . PMC 6720282. PMID 31426529.
- ^ "Glyxambi-эмпаглифлозин и линаглиптин таблетки, покрытые пленочной оболочкой". DailyMed . 22 января 2020 г. Получено 3 апреля 2020 г.
- ^ "Synjardy XR- эмпаглифлозин, таблетка метформина гидрохлорида, пролонгированного действия". DailyMed .
- ^ "Trijardy XR- эмпаглифлозин, линаглиптин, метформина гидрохлорид таблетка, пролонгированного действия". DailyMed . Архивировано из оригинала 25 декабря 2021 г. Получено 24 декабря 2021 г.
- ^ Tucker ME (7 мая 2013 г.). «Первые подробности испытаний эмпаглифлозина следуют за заявками в США и ЕС». Медицинские новости Medscape . Архивировано из оригинала 18 июня 2013 г. Получено 18 января 2014 г.
- ^ ab Mechatie E (1 августа 2014 г.). «FDA одобряет эмпаглифлозин для взрослых с диабетом 2 типа». Clinical Endocrinology News Digital Network . Архивировано из оригинала 28 августа 2021 г. Получено 23 августа 2014 г.
- ^ Liakos A, Karagiannis T, Athanasiadou E, Sarigianni M, Mainou M, Papatheodorou K и др. (октябрь 2014 г.). «Эффективность и безопасность эмпаглифлозина при диабете 2 типа: систематический обзор и метаанализ». Диабет, ожирение и метаболизм . 16 (10): 984–993. doi :10.1111/dom.12307. PMID 24766495.
- ^ Inzucchi SE, Davies MJ, Khunti K, Trivedi P, George JT, Zwiener I и др. (февраль 2021 г.). «Эффекты лечения эмпаглифлозином в зависимости от категорий исходного уровня HbA1c, массы тела и артериального давления в качестве дополнения к метформину у пациентов с диабетом 2 типа». Диабет, ожирение и метаболизм . 23 (2): 425–433. doi :10.1111/dom.14234. PMC 7839733. PMID 33084149 .
- ^ Verma S, McMurray JJ (октябрь 2018 г.). «Ингибиторы SGLT2 и механизмы сердечно-сосудистой пользы: современный обзор». Diabetologia . 61 (10): 2108–2117. doi : 10.1007/s00125-018-4670-7 . PMID 30132036.
- ^ abc Kovacs CS, Seshiah V, Swallow R, Jones R, Rattunde H, Woerle HJ и др. (февраль 2014 г.). «Эмпаглифлозин улучшает гликемию и контроль веса в качестве дополнительной терапии к пиоглитазону или пиоглитазону плюс метформин у пациентов с диабетом 2 типа: 24-недельное рандомизированное плацебо-контролируемое исследование». Диабет, ожирение и метаболизм . 16 (2): 147–158. doi :10.1111/dom.12188. PMID 23906415.
- ^ abcd Häring HU, Merker L, Seewaldt-Becker E, Weimer M, Meinicke T, Broedl UC и др. (июнь 2014 г.). «Эмпаглифлозин как дополнение к метформину у пациентов с диабетом 2 типа: 24-недельное рандомизированное двойное слепое плацебо-контролируемое исследование». Diabetes Care . 37 (6): 1650–1659. doi : 10.2337/dc13-2105 . PMID 24722494.
- ^ Anker SD, Khan MS, Butler J, Ofstad AP, Peil B, Pfarr E и др. (январь 2023 г.). «Изменение веса и клинические исходы при сердечной недостаточности со сниженной фракцией выброса: выводы EMPEROR-Reduced». European Journal of Heart Failure . 25 (1): 117–127. doi :10.1002/ejhf.2728. PMC 10098519 . PMID 36325584.
- ^ "Информационный бюллетень об ожирении и избыточном весе" (PDF) . Всемирная организация здравоохранения. Архивировано (PDF) из оригинала 23 января 2019 года . Получено 23 марта 2019 года .

