Дофетилид
 | |
| Клинические данные | |
|---|---|
| Торговые наименования | Тикосин |
| AHFS / Drugs.com | Монография |
| МедлайнПлюс | а601235 |
| код АТС |
|
| Правовой статус | |
| Правовой статус |
|
| Фармакокинетические данные | |
| Биодоступность | 96% (перорально) |
| Связывание с белками | 60% -70% |
| Период полувыведения | 10 часов |
| Идентификаторы | |
| |
| Номер CAS | |
| CID PubChem |
|
| ИУФАР/БПС |
|
| DrugBank | |
| ChemSpider | |
| УНИИ |
|
| КЕГГ | |
| ЧЭБИ | |
| ChEMBL | |
| Панель инструментов CompTox ( EPA ) |
|
| Информационная карта ECHA | 100.166.441 |
| Химические и физические данные | |
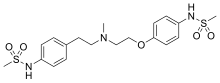
| Формула | С19Н27Н3О5С2 |
| Молярная масса | 441,56 г·моль −1 |
| 3D модель ( JSmol ) |
|
| |
| (проверять) | |
Дофетилид — антиаритмическое средство класса III . [2] Он продается под торговым названием Tikosyn компанией Pfizer и доступен в Соединенных Штатах в капсулах, содержащих 125, 250 и 500 мкг дофетилида. Он недоступен в Европе [3] или Австралии. [4]
Медицинское применение
Дофетилид используется для поддержания синусового ритма у лиц, склонных к возникновению мерцательной аритмии и трепетания предсердий, а также для химической кардиоверсии синусового ритма при мерцательной аритмии и трепетании предсердий . [5] [6]
На основании результатов датского исследования аритмий и смертности при применении дофетилида («DIAMOND») [7] дофетилид не влияет на смертность при лечении пациентов, перенесших инфаркт миокарда с дисфункцией левого желудочка , однако было показано, что он снижает повторные госпитализации по любой причине, а также повторные госпитализации, связанные с ХСН . [7] В связи с результатами исследования DIAMOND некоторые врачи используют дофетилид для подавления фибрилляции предсердий у лиц с дисфункцией ЛЖ, однако его применение, по-видимому, ограничено: после первоначального получения разрешения на продажу в Европе в 1999 году компания Pfizer добровольно отозвала это разрешение в 2004 году по коммерческим причинам [3] , и он не зарегистрирован в других странах первого мира.
Он имеет клинические преимущества перед другими антиаритмическими средствами III класса при химической кардиоверсии мерцательной аритмии и поддержании синусового ритма и не обладает легочной или гепатотоксичностью амиодарона, однако мерцательная аритмия обычно не считается опасной для жизни, а дофетилид вызывает повышенную частоту потенциально опасных для жизни аритмий по сравнению с другими методами лечения. [8]
Противопоказания
Перед введением первой дозы необходимо определить скорректированный интервал QT (QTc). Если QTc больше 440 мсек (или 500 мсек у пациентов с нарушениями желудочковой проводимости ), дофетилид противопоказан. Если частота сердечных сокращений меньше 60 уд/мин, следует использовать нескорректированный интервал QT . После каждой последующей дозы дофетилида следует определить QTc и скорректировать дозировку.
Если в любой момент после приема второй дозы дофетилида QTc превышает 500 мсек (550 мсек у пациентов с нарушениями желудочковой проводимости), прием дофетилида следует прекратить. [9]
Побочные эффекты
Torsades de pointes является наиболее серьезным побочным эффектом терапии дофетилидом. Частота возникновения torsades de pointes составляет 0,3–10,5% и зависит от дозы, при этом частота возникновения увеличивается с увеличением дозы. Большинство эпизодов torsades de pointes произошло в течение первых трех дней после начала приема дофетилида. Пациентов следует госпитализировать и наблюдать в течение первых трех дней после начала приема дофетилида. [7]
Риск возникновения желудочковой тахикардии типа «пируэт» можно снизить, приняв меры предосторожности на начальном этапе терапии, например, госпитализировав пациентов минимум на три дня для проведения серийного измерения уровня креатинина , обеспечив постоянный телеметрический мониторинг и наличие возможности проведения сердечной реанимации.
Фармакология
Механизм действия
Дофетилид действует путем селективного блокирования быстрого компонента выпрямляющего тока калия (I Kr ). [10]
Это приводит к увеличению рефрактерного периода ткани предсердий, что обусловливает его эффективность в лечении мерцательной аритмии и трепетания предсердий.
Дофетилид не влияет на dV/dT max ( наклон восходящей линии деполяризации фазы 0), скорость проводимости или мембранный потенциал покоя.

Наблюдается дозозависимое увеличение интервала QT и скорректированного интервала QT (QTc). По этой причине многие практикующие врачи начинают терапию дофетилидом только у лиц, находящихся под телеметрическим контролем или если могут быть выполнены серийные измерения ЭКГ QT и QTc.
Фармакокинетика
Пиковые концентрации в плазме наблюдаются через два-три часа после перорального приема натощак . Дофетилид хорошо всасывается в пероральной форме, с биодоступностью >90%. Внутривенное введение дофетилида недоступно в Соединенных Штатах. [11]
Период полувыведения дофетилида составляет примерно 10 часов; однако он варьируется в зависимости от многих физиологических факторов (наиболее существенного — клиренса креатинина ) и колеблется от 4,8 до 13,5 часов. В связи со значительным уровнем почечной элиминации (80% в неизмененном виде, 20% в виде метаболитов) дозу дофетилида необходимо корректировать, чтобы предотвратить токсичность из-за нарушения функции почек. [12]
Дофетилид метаболизируется преимущественно ферментами CYP3A4, в основном в печени и желудочно-кишечном тракте . Это означает, что он, вероятно, будет взаимодействовать с препаратами, которые ингибируют CYP3A4, такими как эритромицин , кларитромицин или кетоконазол , что приведет к более высоким и потенциально токсичным уровням дофетилида. [13]
Метаболизм
Устойчивый уровень дофетилида в плазме достигается через 2–3 дня.
80% дофетилида выводится почками , поэтому у лиц с хроническим заболеванием почек дозу дофетилида следует корректировать на основе клиренса креатинина .
В почках дофетилид выводится посредством катионного обмена (секреции). Препараты, которые нарушают работу системы катионного обмена почек, такие как верапамил , циметидин , гидрохлоротиазид , итраконазол , кетоконазол , прохлорперазин и триметоприм, не следует назначать лицам, принимающим дофетилид.
Около 20 процентов дофетилида метаболизируется в печени через изофермент CYP3A4 ферментной системы цитохрома P450 . Лекарственные препараты, которые влияют на активность изофермента CYP3A4, могут повышать уровень дофетилида в сыворотке. Если нарушена система катионного обмена почек (как в случае с перечисленными выше препаратами), больший процент дофетилида выводится через изоферментную систему CYP3A4 .
История
После первоначального одобрения FDA США, из-за проаритмического потенциала, препарат был доступен только больницам и врачам, которые получили образование и прошли специальную подготовку по рискам лечения дофетилидом; однако это ограничение было впоследствии снято в 2016 году. [14]
Смотрите также
Ссылки
- ^ «Список всех препаратов с предупреждениями в черном ящике, составленный FDA (используйте ссылки «Загрузить полные результаты» и «Просмотреть запрос»). nctr-crs.fda.gov . FDA . Получено 22 октября 2023 г. .
- ^ Lenz TL, Hilleman DE (июль 2000 г.). «Дофетилид, новый антиаритмический препарат III класса». Фармакотерапия . 20 (7): 776–786. doi :10.1592/phco.20.9.776.35208. PMID 10907968. S2CID 19897963.
- ^ ab Wathion N (2004-04-13). "Публичное заявление о тикосине (дофетилиде): добровольный отзыв разрешения на продажу в Европейском союзе" (PDF) . Европейское агентство по оценке лекарственных средств . Архивировано из оригинала (PDF) 2017-10-13 . Получено 2015-01-03 .
- ^ Австралийский справочник по лекарственным средствам 2014 г.
- ^ Banchs JE, Wolbrette DL, Samii SM, Penny-Peterson ED, Patel PP, Young SK и др. (ноябрь 2008 г.). «Эффективность и безопасность дофетилида у пациентов с фибрилляцией и трепетанием предсердий». Журнал интервенционной кардиоэлектрофизиологии . 23 (2): 111–115. doi :10.1007/s10840-008-9290-6. PMID 18688699. S2CID 25162347.
- ^ Lenz TL, Hilleman DE (ноябрь 2000 г.). «Дофетилид: новый антиаритмический препарат, одобренный для лечения и/или поддержания фибрилляции/трепетания предсердий». Drugs of Today . 36 (11): 759–771. doi :10.1358/dot.2000.36.11.601530. PMID 12845335.
- ^ abc Торп-Педерсен С., Мёллер М., Блох-Томсен П.Е., Кобер Л., Сандё Э., Эгструп К. и др. (сентябрь 1999 г.). «Дофетилид у пациентов с застойной сердечной недостаточностью и дисфункцией левого желудочка. Датские исследования аритмии и смертности в исследовательской группе дофетилида». Медицинский журнал Новой Англии . 341 (12): 857–865. дои : 10.1056/NEJM199909163411201 . ПМИД 10486417.
- ^ Micromedex Drugdex оценки лекарств micromedex.com
- ^ «ТИКОСИН® (дофетилид)» . Пфайзер.
- ^ Roukoz H, Saliba W (январь 2007 г.). «Дофетилид: новый антиаритмический агент III класса». Expert Review of Cardiovascular Therapy . 5 (1): 9–19. doi :10.1586/14779072.5.1.9. PMID 17187453. S2CID 11255636.
- ^ Rasmussen HS, Allen MJ, Blackburn KJ, Butrous GS, Dalrymple HW (1992). «Дофетилид, новый антиаритмический агент III класса». Журнал кардиоваскулярной фармакологии . 20 (Suppl 2): S96–105. doi :10.1097/00005344-199220002-00015. PMID 1279316.
- ^ «Дофетилид». Lexicomp. Wulters Kluwer Health, nd Web. <online.lexi.com>.
- ^ Walker DK, Alabaster CT, Congrave GS, Hargreaves MB, Hyland R, Jones BC и др. (апрель 1996 г.). «Значение метаболизма в распределении и действии антиаритмического препарата дофетилида. Исследования in vitro и корреляция с данными in vivo». Drug Metabolism and Disposition . 24 (4): 447–455. PMID 8801060.
- ^ "Информация о Тикосине (дофетилиде)". Управление по контролю за продуктами и лекарствами США . 2016-03-09.
