Дитионовая кислота
 | |
 | |
| Имена | |
|---|---|
| Название ИЮПАК дитионовая кислота [1] | |
| Другие имена гиподисерная кислота | |
| Идентификаторы | |
3D модель ( JSmol ) |
|
| ЧЭБИ | |
| ChemSpider | |
CID PubChem |
|
| УНИИ | |
Панель инструментов CompTox ( EPA ) |
|
| |
| |
| Характеристики | |
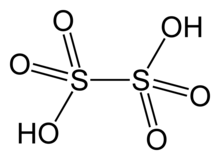
| H2S2O6 | |
| Молярная масса | 162,14 г моль −1 |
| Кислотность ( pK a ) | −3,4 (оценочно) [2] |
| Сопряженное основание | Дитионат |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |
Дитионовая кислота , H 2 S 2 O 6 , является неорганическим соединением с формулой H 2 S 2 O 6 . Это дважды протонированное производное дитионата, хорошо охарактеризованного дианиона. Дитионовая кислота в основном наблюдается и охарактеризована как водный раствор . [3]
Синтез
Дитионаты можно получить путем окисления сульфита (со степени окисления +4 до +5 ), но в более крупных масштабах их получают путем окисления охлажденного водного раствора диоксида серы диоксидом марганца :
- 2MnO2 + 3SO2 → MnS2O6 + MnSO4
Образовавшийся раствор дитионата марганца затем может быть преобразован в дитионаты других металлов посредством реакций метатезиса :
- Ba 2+ (вод) + MnS 2 O 6 (вод) + MnSO 4 (вод) → BaSO 4 (т)↓ + BaS 2 O 6 · 2 H 2 O (вод)
Концентрированные растворы дитионовой кислоты впоследствии можно получить, обрабатывая раствор дитионата бария серной кислотой:
- BaS 2 O 6 (водн.) + H 2 SO 4 (водн.) → H 2 S 2 O 6 (водн.) + BaSO 4 (тв)↓
Смотрите также
- Дитионит натрия
- Гипофосфорная кислота , эквивалент фосфора.
Ссылки
- ^ Международный союз теоретической и прикладной химии (2005). Номенклатура неорганической химии (Рекомендации ИЮПАК 2005). Кембридж (Великобритания): RSC – IUPAC . ISBN 0-85404-438-8 . стр. 130. Электронная версия.
- ^ Perrin, D. D., ред. (1982) [1969]. Константы ионизации неорганических кислот и оснований в водных растворах . Химические данные ИЮПАК (2 -е изд.). Oxford: Pergamon (опубликовано в 1984 г.). Запись 63. ISBN 0-08-029214-3. LCCN 82-16524.
- ^ Гринвуд, Норман Н.; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн . ISBN 978-0-08-037941-8.стр. 715-716


