Ротамер
В химии ротамеры — это химические виды, которые отличаются друг от друга в первую очередь вращениями вокруг одной или нескольких одинарных связей . Различные расположения атомов в молекуле , которые отличаются вращением вокруг одинарных связей, также можно назвать различными конформациями . Конформеры/ротамеры мало отличаются по своим энергиям, поэтому их почти никогда нельзя разделить в практическом смысле. Вращения вокруг одинарных связей подвержены небольшим энергетическим барьерам. [1] Когда временной масштаб для взаимопревращения достаточно велик для изоляции отдельных ротамеров (обычно произвольно определяемый как период полураспада взаимопревращения 1000 секунд или дольше), виды называются атропоизомерами ( см.: атропоизомерия ). [2] [3] [4] Переворот кольца замещенных циклогексанов представляет собой распространенную форму конформеров. [5]
Изучение энергетики вращения связей называется конформационным анализом . [6] В некоторых случаях конформационный анализ может быть использован для прогнозирования и объяснения селективности продукта, механизмов и скоростей реакций. [7] Конформационный анализ также играет важную роль в рациональном, структурно-ориентированном проектировании лекарств .
Типы
Ротамер : один из набора конформеров, возникающих в результате ограниченного вращения вокруг одной одинарной связи. [8]
Вращая свои углерод-углеродные связи, молекулы этана и пропана имеют три локальных энергетических минимума. Они структурно и энергетически эквивалентны и называются шахматными конформерами . Для каждой молекулы три заместителя, исходящие из каждой углерод-углеродной связи, являются шахматными, причем каждый двугранный угол H–C–C–H (и двугранный угол H–C–C–CH 3 в случае пропана) равен 60° (или приблизительно равен 60° в случае пропана). Три заслоненные конформации, в которых двугранные углы равны нулю, являются переходными состояниями (максимумами энергии), соединяющими два эквивалентных энергетических минимума, шахматные конформеры. [ необходима цитата ]
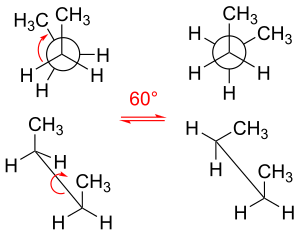
Молекула бутана является простейшей молекулой, в которой вращения одинарных связей приводят к двум типам неэквивалентных структур, известных как анти- и гош- конформеры (см. рисунок).
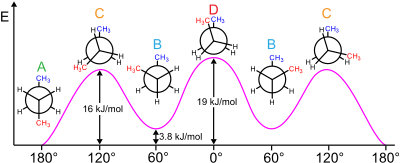
Например, бутан имеет три конформера, связанных с его двумя метильными (CH 3 ) группами: два гош -конформера, в которых метильные группы находятся на расстоянии ±60° друг от друга и которые являются энантиомерами , и анти -конформер, в котором четыре углеродных центра копланарны, а заместители находятся на расстоянии 180° друг от друга (см. диаграмму свободной энергии бутана). Разница энергий между гош и анти составляет 0,9 ккал/моль, что связано с энергией деформации гош-конформера. Таким образом, анти-конформер является наиболее стабильным (≈ 0 ккал/моль). Три заслоненные конформации с двугранными углами 0°, 120° и 240° являются переходными состояниями между конформерами. [6] Обратите внимание, что две заслоненные конформации имеют разные энергии: при 0° заслонены две метильные группы, что приводит к более высокой энергии (≈ 5 ккал/моль), чем при 120°, где метильные группы заслонены водородами (≈ 3,5 ккал/моль). [10]
В то время как простые молекулы можно описать этими типами конформаций, более сложные молекулы требуют использования системы Клайна-Прелога для описания различных конформеров. [6]
Более конкретные примеры конформаций подробно описаны в другом месте:
- Кольцевая конформация
- Конформации циклогексана , включая конформации кресла и лодки.
- Конформации циклоалканов , включая средние кольца и макроциклы
- Конформация углеводов , которая включает конформации циклогексана, а также другие детали.
- Аллильная деформация – энергетика, связанная с вращением вокруг одинарной связи между углеродом sp2 и углеродом sp3 .
- Атропоизомерия – из-за ограниченного вращения вокруг связи.
- Сворачивание , включая вторичную и третичную структуру биополимеров (нуклеиновых кислот и белков). [11]
- Акамптизомерия – обусловлена ограниченной инверсией угла связи.
Равновесие конформеров

Конформеры обычно существуют в динамическом равновесии [12]
На диаграмме, изображающей равновесное распределение двух конформеров при разных температурах, приведены три изотермы. При разнице свободной энергии 0 ккал/моль это дает константу равновесия 1, что означает, что два конформера существуют в соотношении 1:1. У них одинаковая свободная энергия; ни один из них не более стабилен, поэтому ни один из них не преобладает по сравнению с другим. Отрицательная разница в свободной энергии означает, что конформер взаимопревращается в термодинамически более стабильную конформацию, поэтому константа равновесия всегда будет больше 1. Например, Δ G° для превращения бутана из гош -конформера в анти -конформер составляет −0,47 ккал/моль при 298 К. [13] Это дает константу равновесия около 2,2 в пользу анти -конформера или смеси гош : анти -конформеров в соотношении 31:69 в равновесии. Наоборот, положительная разница в свободной энергии означает, что конформер уже более стабилен, поэтому взаимопревращение представляет собой неблагоприятное равновесие ( K < 1).
Распределение популяции конформеров
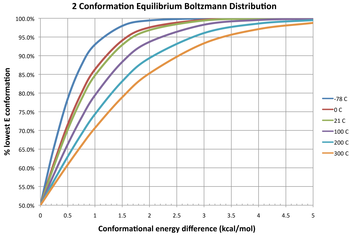
Распределение дробной популяции различных конформеров следует распределению Больцмана : [14]
Левая часть — доля конформера i в равновесной смеси M конформеров в термодинамическом равновесии. С правой стороны E k ( k = 1, 2, ..., M ) — энергия конформера k , R — молярная постоянная идеального газа (приблизительно равная 8,314 Дж/(моль·К) или 1,987 кал/(моль·К)), а T — абсолютная температура . Знаменатель правой части — это функция распределения.
Факторы, влияющие на свободную энергию конформеров
Эффекты электростатических и стерических взаимодействий заместителей, а также орбитальные взаимодействия, такие как гиперконъюгация, отвечают за относительную стабильность конформеров и их переходных состояний. Вклад этих факторов варьируется в зависимости от природы заместителей и может вносить как положительный, так и отрицательный вклад в энергетический барьер. Вычислительные исследования малых молекул, таких как этан, показывают, что электростатические эффекты вносят наибольший вклад в энергетический барьер; однако барьер традиционно приписывается в первую очередь стерическим взаимодействиям. [15] [16]
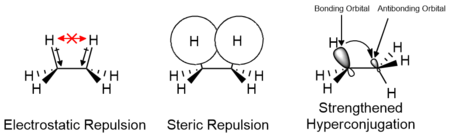
В случае циклических систем стерический эффект и вклад в свободную энергию можно аппроксимировать значениями A , которые измеряют разницу энергий, когда заместитель на циклогексане находится в аксиальном по сравнению с экваториальным положением. В больших (>14 атомов) кольцах существует много доступных низкоэнергетических конформаций, которые соответствуют свободной от напряжений алмазной решетке. [17]
Наблюдение за конформерами
Короткий временной масштаб взаимопревращения исключает разделение конформера в большинстве случаев. Атропоизомеры являются конформационными изомерами, которые могут быть разделены из-за ограниченного вращения. [18] Равновесие между конформационными изомерами можно наблюдать с помощью различных спектроскопических методов . [19]
Сворачивание белка также генерирует конформеры, которые можно наблюдать. Уравнение Карплуса связывает двугранный угол вицинальных протонов с их константами J-связывания , измеренными с помощью ЯМР. Уравнение помогает в выяснении сворачивания белка, а также конформаций других жестких алифатических молекул. [20] Боковые цепи белка демонстрируют ротамеры, распределение которых определяется их стерическим взаимодействием с различными конформациями остова. Этот эффект очевиден из статистического анализа конформаций боковых цепей белка в библиотеке ротамеров, зависящих от остова . [21]
Спектроскопия
Конформационную динамику можно отслеживать с помощью ЯМР- спектроскопии при переменной температуре. Метод применяется к барьерам 8–14 ккал/моль, и виды, демонстрирующие такую динамику, часто называются « флюксионными ». Например, в производных циклогексана два конформера кресла быстро взаимопревращаются при комнатной температуре. Переворот кольца происходит со скоростью приблизительно 10 5 переворотов кольца/сек, с общим энергетическим барьером 10 ккал/моль (42 кДж/моль). Этот барьер исключает разделение при температурах окружающей среды. [22] Однако при низких температурах ниже точки коалесценции можно напрямую отслеживать равновесие с помощью ЯМР-спектроскопии и с помощью динамической, зависящей от температуры ЯМР-спектроскопии — взаимопревращение барьера. [23]
Помимо ЯМР-спектроскопии, для измерения конформерных соотношений используется ИК-спектроскопия . Для аксиального и экваториального конформера бромциклогексана ν CBr отличается почти на 50 см −1 . [22]
Конформационно-зависимые реакции
Скорости реакции сильно зависят от конформации реагентов. Во многих случаях доминирующий продукт возникает в результате реакции менее распространенного конформера в силу принципа Кертина-Хаммета . Это типично для ситуаций, когда конформационное равновесие происходит намного быстрее, чем реакция с образованием продукта. Зависимость реакции от стереохимической ориентации, таким образом, обычно видна только в конфигурационном анализе , в котором конкретная конформация блокируется заместителями. Прогнозирование скоростей многих реакций, включающих переход между состояниями sp2 и sp3, такими как восстановление кетона, окисление спирта или нуклеофильное замещение, возможно, если учитывать все конформеры и их относительную стабильность, определяемую их напряжением . [24]
Одним из примеров, где ротамеры становятся значимыми, являются реакции элиминирования , которые включают одновременное удаление протона и уходящей группы из вицинальных или антиперипланарных положений под влиянием основания.
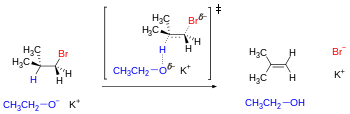
Механизм требует, чтобы отходящие атомы или группы следовали антипараллельным траекториям. Для субстратов с открытой цепью это геометрическое предварительное условие выполняется по крайней мере одним из трех смещенных конформеров. Однако для некоторых циклических субстратов, таких как циклогексан, антипараллельное расположение может быть недостижимо в зависимости от заместителей, которые могут устанавливать конформационный замок. [25] Соседние заместители на циклогексановом кольце могут достигать антиперипланарности только тогда, когда они занимают трансдиаксиальные положения (то есть оба находятся в аксиальном положении, один идет вверх, а другой идет вниз). [ необходима цитата ]
Одним из следствий этого анализа является то, что транс- 4- трет -бутилциклогексилхлорид не может легко элиминироваться, а вместо этого подвергается замещению (см. диаграмму ниже), поскольку наиболее стабильная конформация имеет объемную группу t -Bu в экваториальном положении, поэтому хлоридная группа не является антиперипланарной ни с одним вицинальным водородом (она гош по отношению ко всем четырем). Термодинамически невыгодная конформация имеет группу t -Bu в аксиальном положении, что выше по энергии более чем на 5 ккал/моль (см. значение A ). [26] В результате группа t -Bu «запирает» кольцо в конформации, где она находится в экваториальном положении, и наблюдается реакция замещения. С другой стороны, цис -4- трет -бутилциклогексилхлорид подвергается элиминированию, поскольку антиперипланарность Cl и H может быть достигнута, когда группа t -Bu находится в благоприятном экваториальном положении.
Отталкивание между аксиальной t -бутильной группой и атомами водорода в 1,3-диаксиальном положении настолько сильно, что циклогексановое кольцо вернется к конформации скрученной лодки . Напряжение в циклических структурах обычно характеризуется отклонениями от идеальных углов связи ( напряжение Байера ), идеальных углов кручения ( напряжение Питцера ) или трансаннулярных (Прелог) взаимодействий.
Стереохимия алканов
Конформеры алканов возникают из вращения вокруг sp 3 гибридизированных углерод-углеродных сигма-связей . Наименьший алкан с такой химической связью, этан , существует в виде бесконечного числа конформаций относительно вращения вокруг связи C–C. Две из них признаны формами с минимальным энергетическим значением ( затерянная конформация ) и максимальным энергетическим значением ( затменная конформация ). Существование определенных конформаций обусловлено затрудненным вращением вокруг сигма-связей, хотя роль гиперконъюгации предлагается конкурирующей теорией. [ необходима цитата ]
Важность энергетических минимумов и энергетических максимумов видна при расширении этих концепций на более сложные молекулы, для которых стабильные конформации могут быть предсказаны как формы с минимальной энергией. Определение стабильных конформаций также сыграло большую роль в установлении концепции асимметричной индукции и способности предсказывать стереохимию реакций, контролируемых стерическими эффектами. [ необходима цитата ]
В примере с заторможенным этаном в проекции Ньюмена атом водорода на одном атоме углерода имеет 60° торсионный угол или угол кручения [27] относительно ближайшего атома водорода на другом углероде, так что стерические помехи сведены к минимуму. Заторможенная конформация более стабильна на 12,5 кДж / моль , чем заслоненная конформация, которая является максимумом энергии для этана. В заслоненной конформации торсионный угол минимизирован.

В бутане две смещенные конформации больше не эквивалентны и представляют собой два различных конформера: анти-конформацию (крайняя левая, внизу) и гош-конформацию (крайняя правая, внизу).

Обе конформации свободны от торсионной деформации, но в гош-конформации две метильные группы находятся ближе друг к другу, чем сумма их радиусов Ван-дер-Ваальса. Взаимодействие между двумя метильными группами является отталкивающим ( деформация Ван-дер-Ваальса ), и возникает энергетический барьер .
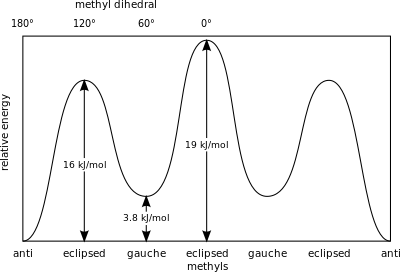
Мера потенциальной энергии, запасенной в конформерах бутана с большими стерическими препятствиями, чем основное состояние «анти»-конформера, определяется следующими значениями: [28]
- Гош, конформер – 3,8 кДж/моль
- Затменные H и CH 3 – 16 кДж/моль
- Затменные CH 3 и CH 3 – 19 кДж/моль.
Затененные метильные группы создают большее стерическое напряжение из-за большей электронной плотности по сравнению с отдельными атомами водорода .
Учебное объяснение существования максимума энергии для заслоненной конформации в этане — стерическое препятствие , но при длине связи CC 154 пм и радиусе Ван-дер-Ваальса для водорода 120 пм атомы водорода в этане никогда не мешают друг другу. Вопрос о том, ответственны ли стерические препятствия за заслоненный максимум энергии, является предметом дебатов и по сей день. Одна из альтернатив объяснению стерических препятствий основана на гиперконъюгации , проанализированной в рамках естественной орбитальной связи. [29] [30] [31] В заторможенной конформации одна сигма- связывающая орбиталь CH отдает электронную плотность антисвязывающей орбитали другой связи CH. Энергетическая стабилизация этого эффекта максимальна, когда две орбитали имеют максимальное перекрытие, происходящее в заторможенной конформации. В заторможенной конформации перекрытия нет, что приводит к неблагоприятному максимуму энергии. С другой стороны, анализ в рамках количественной теории молекулярных орбиталей показывает, что 2-орбитальные-4-электронные (стерические) отталкивания доминируют над гиперконъюгацией. [32] Исследование теории валентных связей также подчеркивает важность стерических эффектов. [33]
Номенклатура
Наименование алканов согласно стандартам, перечисленным в Золотой книге ИЮПАК, осуществляется в соответствии с системой Клайна-Прелога для указания углов (называемых либо торсионными, либо двугранными углами ) между заместителями вокруг одинарной связи: [27]
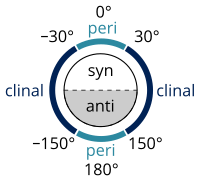
- угол кручения между 0° и ±90° называется син (s)
- угол кручения между ±90° и 180° называется анти (а)
- угол кручения между 30° и 150° или между −30° и −150° называется клинальным (c)
- угол кручения между 0° и ±30° или ±150° и 180° называется перипланарным (p)
- угол скручивания от 0° до ±30° называется синперипланарной (sp), также называемой син- или цис- конформацией
- угол кручения от 30° до 90° и от −30° до −90° называется синклинальным (sc), также называемым гошем или перекосом [34]
- угол кручения между 90° и 150° или от −90° до −150° называется антиклинальным (ac)
- угол кручения между ±150° и 180° называется антиперипланарным (ap), также называемым анти- или транс- конформацией
Деформация кручения или «деформация Питцера» относится к сопротивлению скручиванию вокруг связи.
Особые случаи
В н -пентане концевые метильные группы испытывают дополнительную интерференцию пентана . [ необходима ссылка ]
Замена водорода на фтор в политетрафторэтилене изменяет стереохимию с зигзагообразной геометрии на спиральную из -за электростатического отталкивания атомов фтора в позициях 1,3. Доказательства спиральной структуры в кристаллическом состоянии получены из рентгеновской кристаллографии и из ЯМР-спектроскопии и кругового дихроизма в растворе. [35]
Смотрите также
- Аномерный эффект
- Библиотека ротамеров, зависящих от скелета
- Циклоалкан
- Циклогексан
- эффект гоша
- Система Клайна–Прелога
- Макроциклический стереоконтроль
- Молекулярная конфигурация
- Молекулярное моделирование
- Молекулярная симметрия § Молекулярная нежесткость
- Стерические эффекты
- Штамм (химия)
Ссылки
- ^ "свободное вращение (затрудненное вращение, ограниченное вращение)". Золотая книга ИЮПАК .
- ^ ab Moss, GP (1996-01-01). "Основная терминология стереохимии (Рекомендации ИЮПАК 1996 г.)". Pure and Applied Chemistry . 68 (12): 2193–2222 . doi : 10.1351/pac199668122193 . ISSN 1365-3075. S2CID 98272391.
- ^ Ōki, Michinori (1983) Recent Advances in Atropisomerism, в Topics in Stereochemistry , Vol. 14 (NL Allinger, EL Eliel и SH Wilen, Eds.), Hoboken, NJ:John Wiley & Sons, стр. 1–82; опубликовано онлайн в 2007 г. , DOI: 10.1002/9780470147238.ch1, см. [1] и [2] [ постоянная мертвая ссылка ] , доступ получен 12 июня 2014 г.
- ^ Alkorta, Ibon; Jose Elguero; Christian Roussel; Nicolas Vanthuyne; Patrick Piras (2012). Атропоизомерия и аксиальная хиральность в гетероароматических соединениях . Достижения в гетероциклической химии. Т. 105. С. 1– 188. doi : 10.1016/B978-0-12-396530-1.00001-2. hdl : 10261/62060. ISBN 9780123965301.
- ^ Хант, Ян. "Стереохимия". Университет Калгари . Получено 28 октября 2013 г.
- ^ abc Anslyn, Eric; Dennis Dougherty (2006). Современная физическая органическая химия . Университетская наука. стр. 95. ISBN 978-1891389313.
- ^ Бартон, Дерек (1970). «Принципы конформационного анализа». Nobel Media AB 2013. 169 (3945). Elsevier Publishing Co.: 539– 44. Bibcode : 1970Sci...169..539B. doi : 10.1126/science.169.3945.539. PMID 17746022. Получено 10 ноября 2013 г.
- ^ "ротамер". Золотая книга . ИЮПАК. 2014. doi : 10.1351/goldbook.R05407 .
- ^ J, McMurry (2012). Органическая химия (8-е изд.). Belmont, CA: Brooks/Cole. стр. 98. ISBN 9780840054449.
- ^ Bauld, Nathan. "Конформационный анализ бутана". Техасский университет . Получено 28 октября 2013 г.
- ^ Данбрак, Р. (2002). «Библиотеки ротамеров в 21 веке». Current Opinion in Structural Biology . 12 (4): 431– 440. doi :10.1016/S0959-440X(02)00344-5. PMID 12163064.
- ^ Bruzik, Karol. "Глава 6: Конформация". Иллинойсский университет в Чикаго . Архивировано из оригинала 11 ноября 2013 года . Получено 10 ноября 2013 года .
- ^ Стандартное изменение энтальпии Δ H ° от гош до анти составляет –0,88 ккал/моль. Однако, поскольку существуют две возможные гош -формы, существует статистический фактор, который необходимо учитывать как энтропийный член. Таким образом, Δ G ° = Δ H ° – T Δ S° = Δ H° + RT ln 2 = –0,88 ккал/моль + 0,41 ккал/моль = –0,47 ккал/моль при 298 К.
- ^ Рзепа, Генри. «Конформационный анализ». Имперский колледж Лондона . Получено 11 ноября 2013 г.
- ^ Лю, Шубин (7 февраля 2013 г.). «Происхождение и природа барьеров вращения связей: единый взгляд». Журнал физической химии A. 117 ( 5): 962– 965. Bibcode :2013JPCA..117..962L. doi :10.1021/jp312521z. PMID 23327680.
- ^ Кэри, Фрэнсис А. (2011). Органическая химия (8-е изд.). Нью-Йорк: McGraw-Hill. стр. 105. ISBN 978-0-07-340261-1.
- ^ Драгойлович, Велько (2015). "Конформационный анализ циклоалканов" (PDF) . Chemtexts . 1 (3): 14. Bibcode :2015ChTxt...1...14D. doi :10.1007/s40828-015-0014-0. S2CID 94348487.
- ^ Макнот (1997). "Атропоизомеры". Сборник химических терминов ИЮПАК . Оксфорд: Blackwell Scientific Publications. doi :10.1351/goldbook.A00511. ISBN 978-0967855097.
- ^ Смит, Майкл Б.; Марч, Джерри (2007), Advanced Organic Chemistry: Reactions, Mechanisms, and Structure (6-е изд.), Нью-Йорк: Wiley-Interscience, стр. 195-196, ISBN 978-0-471-72091-1
- ^ Далтон, Луиза. "Уравнение Карплуса". Новости химии и машиностроения . Американское химическое общество . Получено 27 октября 2013 г.
- ^ Данбрак, Р. Л.; Коэн, Ф. Э. (1997). «Байесовский статистический анализ предпочтений ротамеров боковой цепи белка». Protein Science . 6 (8): 1661– 1681. doi :10.1002/pro.5560060807. ISSN 0961-8368. PMC 2143774 . PMID 9260279.
- ^ ab Eliel, EL; Wilen, SH; Mander, LN (1994). Стереохимия органических соединений . J. Wiley and Sons. ISBN 978-0-471-01670-0.
- ^ Jensen, Frederick R.; Bushweller, C. Hackett (1969-06-01). "Разделение конформеров. II. Аксиальные и экваториальные изомеры хлорциклогексана и тридейтериометоксициклогексана". Журнал Американского химического общества . 91 (12): 3223– 3225. Bibcode : 1969JAChS..91.3223J. doi : 10.1021/ja01040a022. ISSN 0002-7863.
- ^ Шнайдер, Х.-Дж.; Шмидт, Г.; Томас Ф.Дж. Американское химическое общество, 1983, 105, 3556. https://pubs.acs.org/doi/pdf/10.1021/ja00349a031
- ^ Рзепа, Генри С. (2014). «Циклоалканы». Имперский колледж Лондона.
- ^ Догерти, Эрик В. Анслин; Деннис, А. (2006). Современная физическая органическая химия (ред. Дод.). Саусалито, Калифорния: University Science Books. стр. 104. ISBN 978-1-891389-31-3.
- ^ ab IUPAC , Compendium of Chemical Terminology , 2nd ed. («Золотая книга») (1997). Онлайн-исправленная версия: (2006–) «torsion angle». doi :10.1351/goldbook.T06406
- ^ Мак-Мерри, Дж. Э. (2003). Органическая химия (6-е изд.). Брукс Коул. ISBN 978-0534000134.
- ^ Pophristic, Vojislava; Goodman, Lionel (2001). «Гиперконъюгация, а не стерическое отталкивание приводит к ступенчатой структуре этана». Nature . 411 (6837): 565– 568. Bibcode :2001Natur.411..565P. doi :10.1038/35079036. ISSN 1476-4687. PMID 11385566.
- ^ Weinhold, Frank (2001). «Новый поворот в молекулярной форме». Nature . 411 (6837). Springer Science and Business Media LLC: 539– 541. doi : 10.1038/35079225. ISSN 0028-0836. PMID 11385553.
- ^ Вайнхольд, Франк (15.09.2003). «Опровержение доводов Бикельхаупта–Бэрендса о стерическом отталкивании, вызывающем ступенчатую конформацию этана». Angewandte Chemie International Edition . 42 (35): 4188– 4194. doi :10.1002/anie.200351777. ISSN 1433-7851.
- ^ Bickelhaupt, F. Matthias; Baerends, Evert Jan (2003-09-15). «Дело в стерическом отталкивании, вызывающем ступенчатую конформацию этана». Angewandte Chemie (на немецком языке). 115 (35): 4315– 4320. Bibcode : 2003AngCh.115.4315B. doi : 10.1002/ange.200350947. ISSN 0044-8249.
- ^ Mo, Yirong; Wu, Wei; Song, Lingchun; Lin, Menghai; Zhang, Qianer; Gao, Jiali (2004-03-30). "Масштаб гиперконъюгации в этане: перспектива с точки зрения теории валентных связей Ab Initio". Angewandte Chemie International Edition . 43 (15). Wiley: 1986– 1990. doi :10.1002/anie.200352931. ISSN 1433-7851. PMID 15065281.
- ^ IUPAC , Compendium of Chemical Terminology , 2nd ed. («Золотая книга») (1997). Онлайн-исправленная версия: (2006–) «gauche». doi :10.1351/goldbook.G02593
- ^ Конформационный анализ хиральных спиральных перфторалкильных цепей VCD Kenji Monde, Nobuaki Miura, Mai Hashimoto, Tohru Taniguchi и Tamotsu Inabe J. Am. Chem. Soc .; 2006 ; 128(18) стр. 6000–6001; Графическое резюме