Оксид кобальта(II,III)
_oxide.jpg/440px-Cobalt(II,III)_oxide.jpg) | |
 | |
| Имена | |
|---|---|
| Название ИЮПАК оксид кобальта(II) дикобальта(III) | |
| Другие имена оксид кобальта, оксид кобальта(II,III), оксид кобальта, тетраоксид трикобальта | |
| Идентификаторы | |
3D модель ( JSmol ) |
|
| ChemSpider | |
| Информационная карта ECHA | 100.013.780 |
| Номер ЕС |
|
CID PubChem |
|
| Номер RTECS |
|
| УНИИ | |
Панель инструментов CompTox ( EPA ) |
|
| |
| |
| Характеристики | |
| Co3O4 CoO.Co 2 O 3 | |
| Молярная масса | 240,80 г/моль |
| Появление | черный сплошной |
| Плотность | 6,07 г/см 3 [2] |
| Температура плавления | 895 °C (1643 °F; 1168 K) |
| Точка кипения | 900 °C (1,650 °F; 1,170 K) (разлагается) |
| Нерастворимый | |
| Растворимость | растворим (с разложением) в кислотах и щелочах |
| +7380·10 −6 см 3 /моль | |
| Структура | |
| кубический | |
| Фд 3 м, № 227 [3] | |
| Опасности | |
| Маркировка СГС : | |
  | |
| Опасность | |
| Н317 , Н334 , Н350 , Н411 | |
| П261 , П273 , П284 , П304+П340 , П342+П311 | |
| NFPA 704 (огненный алмаз) | |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |
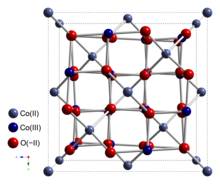
Оксид кобальта(II,III) — неорганическое соединение с формулой Co 3 O 4 . Это один из двух хорошо охарактеризованных оксидов кобальта . Это черное антиферромагнитное твердое вещество. Как соединение со смешанной валентностью , его формула иногда записывается как Co II Co III 2 O 4 , а иногда как CoO•Co 2 O 3 . [4]
Структура
Co 3 O 4 принимает обычную структуру шпинели с ионами Co 2+ в тетраэдрических пустотах и ионами Co 3+ в октаэдрических пустотах кубической плотноупакованной решетки оксидных анионов . [4]
 | 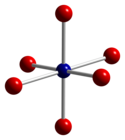 | 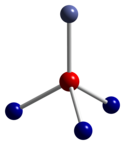 |
| тетраэдрическая координационная геометрия Co(II) | искаженная октаэдрическая координационная геометрия Co(III) | искаженная тетраэдрическая координационная геометрия O |
Синтез
Оксид кобальта(II) , CoO, превращается в Co 3 O 4 при нагревании до температуры около 600–700 °C на воздухе. [4] Выше 900 °C CoO стабилен. [4] [5] Эти реакции описываются следующим равновесием:
- 2Co3O4 ⇌ 6CoO + O2
Приложения
Оксид кобальта (II, III) используется в качестве синего красителя для керамической эмали и стекла , как альтернатива оксиду кобальта (II). [6]
Оксид кобальта (II, III) используется в качестве электрода в некоторых литий-ионных аккумуляторах , возможно, в форме наночастиц оксида кобальта .
Безопасность
Соединения кобальта в больших количествах потенциально ядовиты. [7]
Смотрите также
Ссылки
- ^ "Оксид кобальта (II,III) 203114". Sigma-Aldrich .
- ^ Lide, David R., ред. (2006). CRC Handbook of Chemistry and Physics (87-е изд.). Бока-Ратон, Флорида: CRC Press . ISBN 0-8493-0487-3.
- ^ "mp-18748: Co3O4 (кубический, Fd-3m, 227)". materialsproject.org . Получено 20.12.2019 .
- ^ abcd Гринвуд, Норман Н .; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн . стр. 1118. ISBN 978-0-08-037941-8.
- ↑ Справочник по препаративной неорганической химии, 2-е изд. Под редакцией Г. Брауэра, Academic Press, 1963, Нью-Йорк. С. 1520.
- ^ Фрэнк Хамер, Джанет Хамер (2004): Словарь материалов и методов Поттера. Издательство Пенсильванского университета; 437 стр. ISBN 0812238109
- ^ MSDS [ постоянная мертвая ссылка ]



