Биология депрессии
Научные исследования показали, что различные области мозга демонстрируют измененную активность у людей с большим депрессивным расстройством (БДР) [1] , и это воодушевило сторонников различных теорий, которые стремятся определить биохимическое происхождение заболевания, в отличие от теорий, которые подчеркивают психологические или ситуативные причины. Факторы, охватывающие эти причинные группы, включают дефицит магния [2] , витамина D [ 3] и триптофана с ситуативным происхождением, но биологическим воздействием. Несколько теорий относительно биологически обоснованной причины депрессии были предложены на протяжении многих лет, включая теории, вращающиеся вокруг моноаминовых нейротрансмиттеров , нейропластичности , нейрогенеза , воспаления и циркадного ритма . Физические заболевания, включая гипотиреоз и митохондриальные заболевания , также могут вызывать симптомы депрессии. [4] [5]
Нейронные цепи, вовлеченные в депрессию, включают те, которые участвуют в генерации и регуляции эмоций, а также в вознаграждении. Аномалии обычно обнаруживаются в боковой префронтальной коре, предполагаемая функция которой, как правило, считается связанной с регуляцией эмоций. Регионы, вовлеченные в генерацию эмоций и вознаграждения, такие как миндалевидное тело , передняя поясная кора (ППК) , орбитофронтальная кора (ОФК) и полосатое тело , также часто вовлечены. Эти регионы иннервируются моноаминергическими ядрами, и предварительные данные указывают на потенциальную роль аномальной моноаминергической активности. [6] [7]
Генетические факторы
Трудность генных исследований
Исторически исследования генов-кандидатов были основным направлением исследований. Однако, поскольку количество генов снижает вероятность выбора правильного гена-кандидата, ошибки типа I (ложноположительные результаты) весьма вероятны. Исследования генов-кандидатов часто обладают рядом недостатков, включая частые ошибки генотипирования и недостаточную статистическую мощность. Эти эффекты усугубляются обычной оценкой генов без учета взаимодействия генов. Эти ограничения отражаются в том факте, что ни один ген-кандидат не достиг общегеномной значимости. [8]
Гены-кандидаты
5-HTTLPR
Короткий аллель гена промотора 5-HTTLPR или переносчика серотонина был связан с повышенным риском депрессии; однако с 1990-х годов результаты были противоречивыми. [9] [10] [11] [12] [13] Другие гены, которые были связаны с взаимодействием генов и окружающей среды, включают CRHR1 , FKBP5 и BDNF , первые два из которых связаны с реакцией на стресс оси HPA , а последний из них участвует в нейрогенезе . Анализ гена-кандидата 5-HTTLPR на депрессию не дал окончательных результатов относительно его влияния, как отдельно, так и в сочетании с жизненным стрессом. [14]
Исследование 2003 года предположило, что взаимодействие генов и окружающей среды (GxE) может объяснить, почему жизненный стресс является предиктором депрессивных эпизодов у некоторых людей, но не у других, в зависимости от аллельной вариации промотора, связанного с переносчиком серотонина ( 5-HTTLPR ). [15] Эта гипотеза широко обсуждалась как в научной литературе, так и в популярных СМИ, где ее окрестили «геном орхидеи», но окончательно не подтвердилась в гораздо более крупных выборках, а наблюдаемые размеры эффекта в более ранних работах не согласуются с наблюдаемой полигенностью депрессии. [16]
БДНФ
Также предполагалось, что полиморфизмы BDNF имеют генетическое влияние, но ранние результаты и исследования не удалось воспроизвести в более крупных выборках, а размеры эффекта, обнаруженные в более ранних оценках, не соответствуют наблюдаемой полигенности депрессии. [16]
SIRT1 и LHPP
Исследование GWAS, проведенное в 2015 году среди женщин народности хань, положительно идентифицировало два варианта в интронных областях вблизи SIRT1 и LHPP со значимой ассоциацией по всему геному. [17] [18]
Полиморфизмы транспортера норадреналина
Попытки найти корреляцию между полиморфизмами транспортера норадреналина и депрессией дали отрицательные результаты. [19]
В одном обзоре были выявлены несколько часто изучаемых генов-кандидатов. Гены, кодирующие рецепторы 5-HTT и 5-HT 2A, были непоследовательно связаны с депрессией и ответом на лечение. Смешанные результаты были получены для полиморфизмов нейротрофического фактора мозга (BDNF) Val66Met. Было обнаружено, что полиморфизмы в гене триптофангидроксилазы предположительно связаны с суицидальным поведением. [20] Метаанализ 182 генетических исследований с контролем случая, опубликованных в 2008 году, показал, что аполипопротеин E эпсилон 2 является защитным, а GNB3 825T, MTHFR 677T, вставка или делеция SLC6A4 44bp и генотип SLC6A3 40 bpVNTR 9/10 представляют риск. [21]
Циркадный ритм

Депрессия может быть связана с нарушениями циркадного ритма [22] или биологических часов.
Хорошо синхронизированный циркадный ритм имеет решающее значение для поддержания оптимального здоровья . Неблагоприятные изменения и перестройки циркадного ритма связаны с различными неврологическими расстройствами и расстройствами настроения , включая депрессию. [23]
Спать
Нарушение сна является наиболее выраженным симптомом у пациентов с депрессией. [24] Исследования электроэнцефалограмм сна показали характерные изменения при депрессии, такие как снижение выработки сна без быстрого движения глаз, нарушение непрерывности сна и растормаживание сна с быстрым движением глаз (БДГ). [25] Быстрый сон с движением глаз (БДГ) — стадия, на которой происходят сновидения — может наступать быстро и быть интенсивным у людей с депрессией. Быстрый сон зависит от снижения уровня серотонина в стволе мозга , [26] и нарушается соединениями, такими как антидепрессанты, которые повышают серотонинергический тонус в структурах ствола мозга. [26] В целом, серотонинергическая система наименее активна во время сна и наиболее активна во время бодрствования. Длительное бодрствование из-за лишения сна [22] активирует серотонинергические нейроны, что приводит к процессам, аналогичным терапевтическому эффекту антидепрессантов, таких как селективные ингибиторы обратного захвата серотонина (СИОЗС). У людей с депрессией может наблюдаться значительный подъем настроения после ночи лишения сна. Терапевтический эффект СИОЗС может напрямую зависеть от усиления центральной серотонинергической нейротрансмиссии, той же системы, которая влияет на циклы сна и бодрствования. [26]
Светотерапия
Исследования эффектов светотерапии на сезонное аффективное расстройство показывают, что лишение света связано со снижением активности серотонинергической системы и нарушениями цикла сна, в частности, бессонницей. Воздействие света также нацелено на серотонинергическую систему, что подтверждает важную роль, которую эта система может играть в депрессии. [27] Лишение сна и светотерапия нацелены на ту же нейротрансмиттерную систему мозга и те же области мозга, что и антидепрессанты, и теперь используются в клинической практике для лечения депрессии. [28] Светотерапия, лишение сна и смещение времени сна (терапия опережающей фазы сна) используются в сочетании для быстрого прерывания глубокой депрессии у людей, госпитализированных с большим депрессивным расстройством (большое депрессивное расстройство). [27]
Увеличение и уменьшение продолжительности сна, по-видимому, является фактором риска депрессии. [29] У людей с БДР иногда наблюдаются суточные и сезонные колебания тяжести симптомов, даже при несезонной депрессии. Дневное улучшение настроения было связано с активностью дорсальных нейронных сетей. Также наблюдалось повышение средней температуры тела. Одна из гипотез предполагала, что депрессия является результатом фазового сдвига. [30]
Воздействие дневного света коррелирует со снижением активности переносчика серотонина, что может лежать в основе сезонности некоторых видов депрессии. [31]
Моноамины
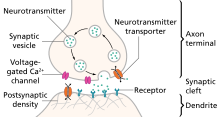
Моноамины — это нейротрансмиттеры , в число которых входят серотонин , дофамин , норадреналин и адреналин . [32]
Моноаминовая гипотеза депрессии
Многие антидепрессанты резко повышают синаптические уровни моноаминового нейротрансмиттера, серотонина, но они также могут повышать уровни норадреналина и дофамина. Наблюдение за этой эффективностью привело к моноаминовой гипотезе депрессии , которая постулирует, что дефицит определенных нейротрансмиттеров отвечает за депрессию, и даже что определенные нейротрансмиттеры связаны с определенными симптомами. Нормальные уровни серотонина были связаны с регуляцией настроения и поведения, сном и пищеварением; норадреналин с реакцией «бей или беги» ; и дофамин с движением, удовольствием и мотивацией. Некоторые также предложили связь между моноаминами и фенотипами, такими как серотонин во сне и самоубийстве, норадреналин при дисфории, усталости, апатии, когнитивной дисфункции и дофамин при потере мотивации и психомоторных симптомах. [33] Основным ограничением моноаминовой гипотезы депрессии является терапевтическая задержка между началом лечения антидепрессантами и воспринимаемым улучшением симптомов. Одним из объяснений этого терапевтического отставания является то, что первоначальное увеличение синаптического серотонина является лишь временным, поскольку активация серотонинергических нейронов в дорсальном шве адаптируется через активность ауторецепторов 5-HT 1A . Считается, что терапевтический эффект антидепрессантов возникает из-за десенсибилизации ауторецепторов в течение определенного периода времени, в конечном итоге повышая активацию серотонинергических нейронов. [34]

серотонин
Теория депрессии, основанная на «химическом дисбалансе» серотонина, предложенная в 1960-х годах [35] , не подтверждается имеющимися научными данными. [35] [36] СИОЗС изменяют баланс серотонина внутри и снаружи нейронов: их клинический антидепрессивный эффект (который устойчив при тяжелой депрессии [37] ), вероятно, обусловлен более сложными изменениями в функционировании нейронов, которые происходят как последствие этого. [38]
Первоначальные исследования серотонина при депрессии изучали периферические показатели, такие как метаболит серотонина 5-гидроксииндолуксусная кислота (5-HIAA) и связывание тромбоцитов. Результаты были в целом противоречивыми и не могли быть обобщены на центральную нервную систему. Однако данные исследований связывания рецепторов и фармакологических проблем предоставляют некоторые доказательства дисфункции нейротрансмиссии серотонина при депрессии. [39] Серотонин может косвенно влиять на настроение, изменяя эмоциональные предубеждения обработки, которые наблюдаются как на когнитивном/поведенческом, так и на нейронном уровне. [40] [39] Фармакологическое снижение синтеза серотонина и фармакологическое усиление синаптического серотонина могут вызывать и ослаблять негативные аффективные предубеждения, соответственно. Эти эмоциональные предубеждения обработки могут объяснить терапевтический разрыв. [40]
Дофамин
Хотя в дофаминергических системах наблюдались различные отклонения, результаты были противоречивыми. Люди с большим депрессивным расстройством имеют повышенную реакцию вознаграждения на декстроамфетамин по сравнению с контрольной группой, и было высказано предположение, что это является результатом гиперчувствительности дофаминергических путей из-за естественной гипоактивности. Хотя полиморфизмы рецепторов D 4 и D 3 были связаны с депрессией, ассоциации не были последовательно воспроизведены. Подобная непоследовательность была обнаружена в посмертных исследованиях, но различные агонисты дофаминовых рецепторов показывают многообещающие результаты в лечении большого депрессивного расстройства. [41] Есть некоторые доказательства того, что у людей с меланхолической депрессией наблюдается снижение активности нигростриарного пути (психомоторная заторможенность). [42] Дополнительным подтверждением роли дофамина в депрессии является постоянное обнаружение сниженных метаболитов дофамина в спинномозговой жидкости и яремной вене, [43] а также посмертные данные об измененной экспрессии дофаминового рецептора D 3 и транспортера дофамина . [44] Исследования на грызунах подтвердили потенциальный механизм, включающий вызванную стрессом дисфункцию дофаминергических систем. [45]
Катехоламины
Было сообщено о ряде линий доказательств, указывающих на снижение адренергической активности при депрессии. Результаты включают снижение активности тирозингидроксилазы, уменьшение размера голубого пятна, увеличение плотности адренергических рецепторов α 2 и снижение плотности адренергических рецепторов α 1. [43] Кроме того, нокаут транспортера норадреналина в моделях мышей повышает их толерантность к стрессу, что указывает на участие норадреналина в депрессии. [46]
Одним из методов, используемых для изучения роли моноаминов, является истощение моноаминов. Истощение триптофана (предшественника серотонина), тирозина и фенилаланина (предшественников дофамина) приводит к снижению настроения у людей с предрасположенностью к депрессии, но не у людей без предрасположенности. С другой стороны, ингибирование синтеза дофамина и норадреналина с помощью альфа-метил-пара-тирозина не всегда приводит к снижению настроения. [47]
Моноаминоксидаза
Ответвление гипотезы моноаминов предполагает, что моноаминоксидаза А (МАО-А), фермент, который метаболизирует моноамины, может быть чрезмерно активным у людей с депрессией. Это, в свою очередь, может вызвать пониженный уровень моноаминов. Эта гипотеза получила поддержку в исследовании ПЭТ , которое обнаружило значительно повышенную активность МАО-А в мозге некоторых людей с депрессией. [48] В генетических исследованиях изменения генов, связанных с МАО-А, не были последовательно связаны с депрессией. [49] [50] Вопреки предположениям гипотезы моноаминов, пониженная, но не повышенная активность МАО-А была связана с симптомами депрессии у подростков. Эта связь наблюдалась только у подвергшихся жестокому обращению молодых людей, что указывает на то, что как биологические (гены МАО), так и психологические (жестокое обращение) факторы важны для развития депрессивных расстройств. [51] Кроме того, некоторые данные указывают на то, что в основе депрессии может лежать нарушенная обработка информации в нейронных сетях, а не изменения химического баланса. [52]
Ограничения
Начиная с 1990-х годов исследования выявили многочисленные ограничения гипотезы моноаминов, и ее неадекватность подверглась критике в психиатрическом сообществе. [53] Во-первых, дисфункция серотониновой системы не может быть единственной причиной депрессии. Не у всех пациентов, лечившихся антидепрессантами, наблюдаются улучшения, несмотря на обычно быстрое повышение синаптического серотонина. Если и происходят значительные улучшения настроения, то часто это происходит не в течение как минимум двух-четырех недель. Одним из возможных объяснений этого отставания является то, что усиление активности нейротрансмиттера является результатом ауторецепторной десенсибилизации, которая может занять недели. [54] Интенсивные исследования не смогли найти убедительных доказательств первичной дисфункции определенной моноаминовой системы у людей с большим депрессивным расстройством. Антидепрессанты, которые не действуют через моноаминовую систему, такие как тианептин и опипрамол , известны уже давно. Также были получены противоречивые результаты относительно уровней сывороточного 5-HIAA , метаболита серотонина. [55] Эксперименты с фармакологическими средствами, вызывающими истощение моноаминов, показали, что это истощение не вызывает депрессию у здоровых людей. [56] [57] Другая проблема заключается в том, что препараты, истощающие моноамины, на самом деле могут обладать свойствами антидепрессантов. Кроме того, некоторые утверждают, что депрессия может быть отмечена гиперсеротонинергическим состоянием. [58] Уже ограниченная, гипотеза моноаминов была еще больше упрощена, когда была представлена широкой публике. [59]
Связывание рецептора
По состоянию на 2012 год попытки определить различия в экспрессии рецепторов нейротрансмиттеров или их функции в мозге людей с БДР с помощью позитронно-эмиссионной томографии (ПЭТ) дали противоречивые результаты. Используя технологию визуализации ПЭТ и реагенты, доступные по состоянию на 2012 год, выяснилось, что рецептор D 1 может быть недостаточно экспрессирован в полосатом теле людей с БДР. Литература по связыванию рецепторов 5-HT 1A противоречива; однако она склоняется к общему снижению в мезиотемпоральной коре. Связывание рецепторов 5-HT 2A , по-видимому, нарушено у людей с БДР. Результаты исследований связывания 5-HTT изменчивы, но, как правило, указывают на более высокие уровни у людей с БДР. Результаты исследований связывания рецепторов D 2 /D 3 слишком противоречивы, чтобы делать какие-либо выводы. Доказательства подтверждают повышенную активность МАО у людей с БДР, и это может даже быть маркером признака (не изменяющимся в ответ на лечение). Связывание мускариновых рецепторов, по-видимому, увеличивается при депрессии, и, учитывая динамику связывания лигандов, предполагает повышенную холинергическую активность. [60]
Было проведено четыре метаанализа связывания рецепторов при депрессии: два по переносчику серотонина (5-HTT), один по 5-HT 1A и еще один по переносчику дофамина (DAT) . Один метаанализ по 5-HTT сообщил, что связывание было снижено в среднем мозге и миндалевидном теле , причем первое коррелировало с большим возрастом, а второе — с тяжестью депрессии. [61] Другой метаанализ по 5-HTT, включающий как посмертные, так и in vivo исследования связывания рецепторов, сообщил, что в то время как исследования in vivo обнаружили снижение 5-HTT в полосатом теле, миндалевидном теле и среднем мозге, посмертные исследования не обнаружили значимых связей. [62] Было обнаружено, что 5-HT 1A был снижен в передней поясной коре, мезиовисочной доле, островке и гиппокампе, но не в миндалевидном теле или затылочной доле. Наиболее часто используемые лиганды 5-HT 1A не вытесняются эндогенным серотонином, что указывает на снижение плотности или сродства рецепторов. [63] Связывание транспортера дофамина не изменяется при депрессии. [64]
Обработка эмоций и нейронные цепи
Эмоциональная предвзятость
Люди с большим депрессивным расстройством демонстрируют ряд предубеждений в эмоциональной обработке , таких как тенденция оценивать счастливые лица более негативно и тенденция выделять больше ресурсов внимания на грустные выражения. [65] У людей с депрессией также нарушено распознавание счастливых, злых, испытывающих отвращение, испуганных и удивленных, но не грустных лиц. [66] Функциональная нейровизуализация продемонстрировала гиперактивность различных областей мозга в ответ на негативные эмоциональные стимулы и гипоактивность в ответ на позитивные стимулы. Один метаанализ показал, что у субъектов с депрессией наблюдалась сниженная активность в левой дорсолатеральной префронтальной коре и повышенная активность в миндалевидном теле в ответ на негативные стимулы. [67] Другой метаанализ показал повышенную активность гиппокампа и таламуса в подгруппе субъектов с депрессией, которые не принимали лекарства, не были пожилыми и не имели сопутствующих заболеваний. [68] Было высказано предположение, что терапевтическая задержка антидепрессантов является результатом изменения антидепрессантами эмоциональной обработки, что приводит к изменениям настроения. Это подтверждается наблюдением, что как острое, так и субхроническое введение СИОЗС увеличивает реакцию на позитивные лица. [69] Лечение антидепрессантами, по-видимому, обращает вспять предубеждения, соответствующие настроению, в лимбической , префронтальной и веретенообразной областях. Реакция dlPFC усиливается, а реакция миндалевидного тела ослабевает во время обработки негативных эмоций, первая из которых, как полагают, отражает повышенную регуляцию сверху вниз. Веретенообразная извилина и другие области визуальной обработки сильнее реагируют на позитивные стимулы при лечении антидепрессантами, что, как полагают, отражает положительное смещение обработки. [70] Эти эффекты, по-видимому, не являются уникальными для серотонинергических или норадренергических антидепрессантов, но также возникают при других формах лечения, таких как глубокая стимуляция мозга . [71]
Нейронные цепи
Один метаанализ функциональной нейровизуализации при депрессии выявил паттерн аномальной нейронной активности, предположительно отражающий предвзятость эмоциональной обработки. По сравнению с контрольной группой люди с БДР показали гиперактивность цепей в сети значимости (SN) , состоящей из ядер подушки , островка и дорсальной передней поясной коры (dACC), а также сниженную активность в регуляторных цепях, состоящих из полосатого тела и dlPFC. [72]

Нейроанатомическая модель, называемая лимбико-кортикальной моделью, была предложена для объяснения ранних биологических результатов при депрессии. Модель пытается связать определенные симптомы депрессии с неврологическими отклонениями. Повышенная активность миндалевидного тела в состоянии покоя была предложена для того, чтобы лежать в основе размышлений, поскольку стимуляция миндалевидного тела, как сообщалось, связана с навязчивым воспроизведением негативных воспоминаний. ППК была разделена на прегенуальную (pgACC) и субгенуальную области (sgACC) , причем первая была электрофизиологически связана со страхом, а вторая метаболически вовлечена в грусть у здоровых людей. Гиперактивность латеральных орбитофронтальных и островковых областей, наряду с отклонениями в латеральных префронтальных областях, была предложена для того, чтобы лежать в основе неадаптивных эмоциональных реакций, учитывая роль областей в обучении вознаграждению. [74] [75] Эта модель и другая, называемая «кортикально-стриарной моделью», которая больше фокусируется на аномалиях в кортико-базальных ганглиях-таламо-кортикальной петле , были поддержаны недавней литературой. Сниженная активность полосатого тела, повышенная активность OFC и повышенная активность sgACC были всеми результатами, согласующимися с предложенными моделями. Однако сообщалось, что активность миндалевидного тела была снижена, в отличие от лимбико-кортикальной модели. Более того, только латеральные префронтальные области были смодулированы лечением, что указывает на то, что префронтальные области являются маркерами состояния (т. е. зависят от настроения), в то время как подкорковые аномалии являются маркерами черт (т. е. отражают восприимчивость). [76]
Награда
В то время как тяжесть депрессии в целом не коррелирует с притупленной нейронной реакцией на вознаграждение, ангедония напрямую коррелирует со сниженной активностью в системе вознаграждения . [77] Изучение вознаграждения при депрессии ограничено неоднородностью в определении и концептуализации вознаграждения и ангедонии. Ангедония в широком смысле определяется как сниженная способность чувствовать удовольствие , но опросники и клинические оценки редко различают мотивационное «желание» и потребительскую «симпатию». Хотя ряд исследований показывают, что субъекты, страдающие депрессией, оценивают положительные стимулы менее позитивно и как менее возбуждающие, ряд исследований не находят разницы. Более того, реакция на естественные вознаграждения, такие как сахароза , по-видимому, не ослабевает. Общее аффективное притупление может объяснить «ангедонические» симптомы при депрессии, поскольку метаанализ как положительных, так и отрицательных стимулов выявляет сниженную оценку интенсивности. [78] [79] Поскольку ангедония является выраженным симптомом депрессии, прямое сравнение депрессивных и здоровых субъектов выявляет повышенную активацию субгенуальной передней поясной коры (sgACC) и пониженную активацию вентрального полосатого тела и, в частности, прилежащего ядра (NAcc) в ответ на положительные стимулы. [80] Хотя обнаружение пониженной активности NAcc во время парадигм вознаграждения довольно последовательно, NAcc состоит из функционально разнообразного диапазона нейронов, и пониженный сигнал , зависящий от уровня кислорода в крови (BOLD), в этой области может указывать на множество вещей, включая пониженную афферентную активность или пониженный тормозной выход. [81] Тем не менее, эти области важны в обработке вознаграждения, и считается, что их дисфункция при депрессии лежит в основе ангедонии . Остаточная ангедония, на которую не очень хорошо воздействуют серотонинергические антидепрессанты, предположительно является результатом ингибирования высвобождения дофамина путем активации рецепторов 5-HT 2C в полосатом теле. [80] Реакция на вознаграждение в медиальной орбитофронтальной коре (OFC) ослабевает при депрессии, в то время как реакция латеральной OFC усиливается на наказание. Латеральная OFC демонстрирует устойчивую реакцию на отсутствие вознаграждения или наказания, и считается, что она необходима для изменения поведения в ответ на изменяющиеся обстоятельства. Гиперчувствительность в lOFC может привести к депрессии, вызывая эффект, аналогичный выученной беспомощности у животных. [82]
Повышенная реакция в sgACC является постоянным результатом исследований нейровизуализации с использованием ряда парадигм, включая задачи, связанные с вознаграждением. [80] [83] [84] Лечение также связано с ослабленной активностью в sgACC, [85] а ингибирование нейронов в гомологе sgACC у грызунов, инфралимбической коре (IL) , производит антидепрессивный эффект. [86] Было высказано предположение, что гиперактивность sgACC приводит к депрессии через ослабление соматической реакции на вознаграждение или положительные стимулы. [87] В отличие от исследований функциональной реакции магнитно-резонансной томографии в sgACC во время задач, метаболизм покоя снижается в sgACC. Однако это становится очевидным только при коррекции заметного уменьшения объема sgACC, связанного с депрессией; структурные аномалии очевидны на клеточном уровне, поскольку нейропатологические исследования сообщают о снижении маркеров клеток sgACC. Модель депрессии, предложенная на основе этих результатов Древецом и соавторами, предполагает, что сниженная активность sgACC приводит к усилению активности симпатической нервной системы и ослаблению обратной связи оси HPA. [88] Активность в sgACC также может не быть причиной депрессии, поскольку авторы одного обзора, в котором изучалась нейровизуализация у депрессивных субъектов во время эмоциональной регуляции, предположили, что паттерн повышенной активности sgACC отражает повышенную потребность в модуляции автоматических эмоциональных реакций при депрессии. Более обширное вовлечение sgACC и общее префронтальное вовлечение во время положительной эмоциональной обработки было связано с ослабленной подкорковой реакцией на положительные эмоции и субъектной ангедонией. Это было интерпретировано авторами как отражение пониженной регуляции положительных эмоций из-за чрезмерного вовлечения префронтальной коры. [89]
Нейроанатомия
Хотя ряд результатов нейровизуализации постоянно сообщается о людях с большим депрессивным расстройством, неоднородность депрессивных популяций создает трудности в интерпретации этих результатов. Например, усреднение по популяциям может скрыть определенные результаты, связанные с подгруппами; в то время как сниженная активность dlPFC сообщается о депрессии, подгруппа может иметь повышенную активность dlPFC. Усреднение также может дать статистически значимые результаты, такие как сниженные объемы гиппокампа, которые фактически присутствуют в подгруппе субъектов. [90] Из-за этих и других проблем, включая продольную согласованность депрессии, большинство нейронных моделей, вероятно, неприменимы ко всем депрессиям. [76]
Структурная нейровизуализация

Метаанализы, проведенные с использованием d-картирования на основе семян , сообщили о сокращении серого вещества в ряде лобных областей. Один метаанализ общей депрессии с ранним началом сообщил о сокращении серого вещества в двусторонней передней поясной коре (ACC) и дорсомедиальной префронтальной коре (dmPFC). [92] Один метаанализ первого эпизода депрессии наблюдал различные закономерности сокращения серого вещества в популяциях без приема лекарств и в комбинированной популяции; депрессия без приема лекарств была связана с сокращением правой дорсолатеральной префронтальной коры , правой миндалевидной железы и правой нижней височной извилины ; анализ комбинации депрессии без приема лекарств и с приемом лекарств обнаружил сокращение в левом островке, правой дополнительной двигательной области и правой средней височной извилине. [93] Другой обзор, различающий популяции, принимающие и не принимающие лекарства, хотя и не ограничивающийся людьми с первым эпизодом большого депрессивного расстройства, обнаружил сокращение в объединенной популяции в двусторонней верхней, правой средней и левой нижней лобной извилине, а также в двустороннем парагиппокампе . Увеличение таламуса и серого вещества ППК было зарегистрировано в популяциях, не принимающих лекарства, и принимающих лекарства соответственно. [94] Метаанализ, проведенный с использованием «оценки вероятности активации», сообщил о сокращении парацингулярной коры, dACC и миндалевидного тела. [95]
Используя статистическое параметрическое картирование, один метаанализ повторил предыдущие результаты об уменьшении серого вещества в ППК, медиальной префронтальной коре, нижней лобной извилине, гиппокампе и таламусе; однако также сообщалось об уменьшении серого вещества в ОФК и вентромедиальной префронтальной коре . [96]
Были опубликованы два исследования депрессии от консорциума ENIGMA, одно по толщине коры, а другое по объему подкорки. Уменьшенная толщина коры была зарегистрирована в двусторонней OFC, ACC, островке, средней височной извилине, веретенообразной извилине и задней поясной коре, в то время как дефицит площади поверхности был обнаружен в медиальной затылочной, нижней теменной, орбитофронтальной и прецентральной областях. [97] Подкорковые аномалии, включая уменьшение объемов гиппокампа и миндалевидного тела, которые были особенно выражены при ранней депрессии. [98]

Множественный метаанализ был проведен в исследованиях, оценивающих целостность белого вещества с использованием фракционной анизотропии (ФА) . Снижение ФА было зарегистрировано в мозолистом теле (МТ) как у пациентов с первым эпизодом, не принимавших лекарства, [100] [101] , так и у пациентов с общей большой депрессией. [99] [102] Степень снижения МТ отличается от исследования к исследованию. У людей с БДР, которые ранее не принимали антидепрессанты, было зарегистрировано снижение только в теле МТ [100] и только в колене МТ. [101] С другой стороны, в образцах с общей БДР было зарегистрировано снижение в теле МТ, [101] теле и колене МТ, [99] и только в колене МТ. [102] Снижение FA также было отмечено в передней ножке внутренней капсулы (ALIC) [100] [99] и верхнем продольном пучке . [100] [101]
Функциональная нейровизуализация
В исследованиях активности в состоянии покоя использовался ряд показателей активности в состоянии покоя, включая региональную однородность (ReHO), амплитуду низкочастотных колебаний (ALFF), фракционную амплитуду низкочастотных колебаний (fALFF), маркировку артериального спина (ASL) и позитронно-эмиссионную томографию (ПЭТ) для измерения регионального мозгового кровотока или метаболизма.
Исследования с использованием ALFF и fALFF сообщили о повышении активности ACC, причем первый в первую очередь сообщил о более вентральных результатах, а второй — о более дорсальных результатах. [103] Конъюнктурный анализ исследований ALFF и CBF сошлись на левом островке, при этом ранее нелеченные люди имели повышенную активность островка. Также сообщалось о повышенном CBF хвостатого ядра [104] Метаанализ, объединяющий несколько показателей активности покоя, сообщил о повышенной активности передней поясной извилины, полосатого тела и таламуса и сниженной активности левого островка, постцентральной извилины и веретенообразной извилины. [105] Метаанализ оценки вероятности активации (ALE) исследований состояния покоя ПЭТ/ ОФЭКТ сообщил о сниженной активности в левом островке, прегенуальной и дорсальной передней поясной коре и повышенной активности в таламусе, хвостатом ядре, переднем гиппокампе и миндалевидном теле. [106] По сравнению с метаанализом ALE исследований ПЭТ/ОФЭКТ, исследование с использованием многоядерного анализа плотности сообщило о гиперактивности только в ядрах подушки таламуса. [72]
Области мозга
Исследования мозга людей с MDD обычно показывают нарушенные модели взаимодействия между несколькими частями мозга. Несколько областей мозга вовлечены в исследования, направленные на более полное понимание биологии депрессии:
Подколенная поясная извилина
Исследования показали, что область Бродмана 25 , также известная как субгенуальная поясная извилина, метаболически сверхактивна при резистентной к лечению депрессии . Эта область чрезвычайно богата переносчиками серотонина и считается регулятором обширной сети, включающей такие области, как гипоталамус и ствол мозга , которые влияют на изменения аппетита и сна; миндалевидное тело и островок , которые влияют на настроение и тревожность; гиппокамп , который играет важную роль в формировании памяти; и некоторые части лобной коры, отвечающие за самооценку. Таким образом, нарушения в этой области или меньший, чем обычно, размер этой области способствуют депрессии. Глубокая стимуляция мозга была направлена на эту область, чтобы снизить ее активность у людей с резистентной к лечению депрессией. [107] : 576–578 [108]
Префронтальная кора
В одном обзоре сообщалось о гипоактивности префронтальной коры у людей с депрессией по сравнению с контрольной группой. [109] Префронтальная кора участвует в эмоциональной обработке и регуляции, и дисфункция этого процесса может быть связана с этиологией депрессии. Одно исследование лечения антидепрессантами обнаружило увеличение активности ПФК в ответ на введение антидепрессантов. [110] Один метаанализ, опубликованный в 2012 году, показал, что области префронтальной коры были гипоактивны в ответ на негативные стимулы у людей с большим депрессивным расстройством. [72] Одно исследование предположило, что области префронтальной коры являются частью сети регионов, включая дорсальную и прегенуальную поясную извилину, двустороннюю среднюю лобную извилину, островок и верхнюю височную извилину, которые кажутся гипоактивными у людей с большим депрессивным расстройством. Однако авторы предупредили, что критерии исключения, отсутствие последовательности и небольшие выборки ограничивают результаты. [106]
Миндалевидное тело
Миндалевидное тело, структура, участвующая в обработке эмоций, по-видимому, гиперактивно у людей с большим депрессивным расстройством. [108] Миндалевидное тело у не принимающих лекарства депрессивных людей, как правило, меньше, чем у тех, кто принимал лекарства, однако совокупные данные не показывают никакой разницы между депрессивными и здоровыми людьми. [111] Во время задач по обработке эмоций правое миндалевидное тело более активно, чем левое, однако во время когнитивных задач различий нет, и в состоянии покоя только левое миндалевидное тело, по-видимому, более гиперактивно. [112] Однако одно исследование не обнаружило никакой разницы в активности миндалевидного тела во время задач по обработке эмоций. [113]
Гиппокамп
Атрофия гиппокампа наблюдается во время депрессии, что согласуется с животными моделями стресса и нейрогенеза. [114] [115]
Стресс может вызывать депрессию и симптомы, подобные депрессии, через моноаминергические изменения в нескольких ключевых областях мозга, а также подавление нейрогенеза гиппокампа. [116] Это приводит к изменению в областях мозга, связанных с эмоциями и познанием, а также к дисфункции оси HPA. Из-за дисфункции эффекты стресса могут быть усугублены, включая его воздействие на 5-HT. Более того, некоторые из этих эффектов отменяются антидепрессантным действием, которое может действовать путем увеличения нейрогенеза гиппокампа. Это приводит к восстановлению активности HPA и реактивности на стресс, тем самым восстанавливая пагубные эффекты, вызванные стрессом на 5-HT. [117]
Гипоталамо -гипофизарно-надпочечниковая ось представляет собой цепь эндокринных структур, которые активируются во время реакции организма на стрессоры различного рода. Ось HPA включает три структуры: гипоталамус, который выделяет CRH , который стимулирует гипофиз к выделению АКТГ , который стимулирует надпочечники к выделению кортизола. Кортизол оказывает отрицательное обратное воздействие на гипофиз и гипоталамус. У людей с большим депрессивным расстройством это часто показывает повышенную активацию у людей с депрессией, но механизм, стоящий за этим, пока не известен. [118] У людей с большим депрессивным расстройством наблюдались повышенные базальные уровни кортизола и аномальная реакция на дексаметазоновые пробы. [119] Стресс в раннем возрасте был выдвинут в качестве потенциальной причины дисфункции HPA. [120] [121] Регуляция оси HPA может быть исследована с помощью тестов на подавление дексаметазона, которые проверяют механизмы обратной связи. Неподавление дексаметазона является распространенным явлением при депрессии, но недостаточно последовательным, чтобы использовать его в качестве диагностического инструмента. [122] Изменения оси HPA могут быть ответственны за некоторые изменения, такие как снижение минеральной плотности костей и увеличение веса, обнаруженные у людей с БДР. Один препарат, кетоконазол , который в настоящее время находится на стадии разработки, показал себя многообещающим в лечении БДР. [123] [ необходимо разъяснение ]
Нейрогенез гиппокампа
Снижение нейрогенеза гиппокампа приводит к уменьшению объема гиппокампа. Генетически меньший гиппокамп связан с пониженной способностью обрабатывать психологическую травму и внешний стресс, а также с последующей предрасположенностью к психологическим заболеваниям. [124] Депрессия без семейного риска или детской травмы связана с нормальным объемом гиппокампа, но локализованной дисфункцией. [125]
Модели животных
Существует ряд моделей депрессии на животных, но они ограничены тем, что депрессия включает в себя в первую очередь субъективные эмоциональные изменения. Однако некоторые из этих изменений отражаются в физиологии и поведении, последнее из которых является целью многих моделей на животных. Эти модели обычно оцениваются по четырем аспектам валидности: отражение основных симптомов в модели; прогностическая валидность модели; валидность модели в отношении человеческих характеристик этиологии; [126] и биологическая правдоподобность. [127] [128]
Были использованы различные модели для индукции депрессивного поведения; нейроанатомические манипуляции, такие как удаление обонятельной луковицы или манипуляции с специфичными для цепей с помощью оптогенетики; генетические модели, такие как нокаут 5-HT 1A или селективно выведенные животные; [126] модели, включающие манипуляции окружающей средой, связанные с депрессией у людей, включая хронический легкий стресс, стресс раннего периода жизни и выученную беспомощность. [129] Валидность этих моделей в создании депрессивного поведения можно оценить с помощью ряда поведенческих тестов. Ангедония и дефицит мотивации могут, например, оцениваться путем изучения уровня взаимодействия животного с поощрительными стимулами, такими как сахароза или внутричерепная самостимуляция. Симптомы тревоги и раздражения можно оценить с помощью исследовательского поведения в присутствии стрессовой или новой среды, такой как тест открытого поля, кормление с подавлением новизны или приподнятый крестообразный лабиринт. Усталость, психомоторную слабость и возбуждение можно оценить с помощью двигательной активности , активности по уходу за собой и тестов в открытом поле .
Животные модели обладают рядом ограничений из-за природы депрессии. Некоторые основные симптомы депрессии, такие как размышления, низкая самооценка, чувство вины и подавленное настроение, не могут быть оценены у животных, поскольку они требуют субъективного отчета. [128] С эволюционной точки зрения считается, что поведенческие корреляты поражений или потерь являются адаптивной реакцией для предотвращения дальнейших потерь. Поэтому попытки смоделировать депрессию, которая стремится вызвать поражение или отчаяние, на самом деле могут отражать адаптацию, а не болезнь. Кроме того, хотя депрессия и тревожность часто сопутствуют друг другу, их диссоциации в животных моделях трудно достичь. [126] Фармакологическая оценка валидности часто не связана с клинической фармакотерапией, поскольку большинство скрининговых тестов оценивают острые эффекты, в то время как антидепрессанты обычно действуют у людей через несколько недель. [130]
Нейросхемы
Регионы, участвующие в вознаграждении, являются распространенными целями манипуляции в животных моделях депрессии, включая прилежащее ядро (NAc), вентральную область покрышки (VTA) , вентральный бледный шар (VP) , латеральную габенулу (LHb) и медиальную префронтальную кору (mPFC) . Предварительные исследования фМРТ у людей демонстрируют повышенную активность LHb при депрессии. [131] Латеральная габенула проецируется в RMTg, чтобы управлять торможением дофаминовых нейронов в VTA при отсутствии вознаграждения. В животных моделях депрессии повышенная активность была зарегистрирована в нейронах LHb, которые проецируются в вентральную область покрышки (якобы снижая высвобождение дофамина). LHb также проецируется на реактивные нейроны mPFC, которые могут обеспечивать косвенный механизм для создания депрессивного поведения. [132] Вызванная беспомощностью потенциация синапсов LHb отменяется при лечении антидепрессантами, обеспечивая прогностическую валидность. [131] Ряд входов в LHb вовлечены в создание депрессивного поведения. Подавление ГАМКергических проекций от NAc к LHb снижает обусловленное предпочтение места, вызванное социальной агрессией, а активация этих терминалов вызывает CPP. Активация вентрального паллидума также усиливается при депрессии, вызванной стрессом, эффект, который фармакологически обоснован, и подавление этих нейронов смягчает поведенческие корреляты депрессии. [131] Предварительные данные in vivo от людей с большим депрессивным расстройством предполагают аномалии в передаче сигналов дофамина. [133] Это привело к ранним исследованиям, изучающим активность VTA и манипуляции в животных моделях депрессии. Массовое разрушение нейронов VTA усиливает депрессивное поведение, в то время как нейроны VTA снижают активацию в ответ на хронический стресс. Однако более поздние специфические манипуляции VTA дают различные результаты, при этом конкретная модель животного, продолжительность манипуляции VTA, метод манипуляции VTA и субрегион манипуляции VTA — все это потенциально приводит к различным результатам. [134] Депрессивные симптомы, вызванные стрессом и социальным поражением, включая ангедонию, связаны с потенциацией возбуждающих входов в средние шипиковые нейроны, экспрессирующие дофаминовые рецепторы D2 (D2-MSN), и депрессией возбуждающих входов в средние шипиковые нейроны, экспрессирующие дофаминовые рецепторы D1 (D1-MSN). Оптогенетическое возбуждение D1-MSN облегчает депрессивные симптомы и является вознаграждением, в то время как то же самое с D2-MSN усиливает депрессивные симптомы. Возбуждение глутаминэргических входов из вентрального гиппокампа снижает социальные взаимодействия, а усиление этих проекций создает восприимчивость к депрессии, вызванной стрессом. [134]Манипуляции с различными областями mPFC могут вызывать и ослаблять депрессивное поведение. Например, ингибирование нейронов mPFC, особенно в интралимбической коре, ослабляет депрессивное поведение. Противоречивые результаты, связанные со стимуляцией mPFC, по сравнению с относительно специфическими результатами в инфралимбической коре, предполагают, что прелимбическая кора и инфралимбическая кора могут опосредовать противоположные эффекты. [86] Проекции mPFC к ядрам шва в основном являются ГАМКергическими и подавляют активацию серотонинергических нейронов. Специфическая активация этих областей снижает неподвижность в тесте принудительного плавания, но не влияет на поведение открытого поля или принудительного плавания. Ингибирование шва смещает поведенческий фенотип неконтролируемого стресса к фенотипу, более близкому к контролируемому стрессу. [135]
Измененная нейропластичность
Недавние исследования привлекли внимание к роли измененной нейропластичности при депрессии. Обзор обнаружил конвергенцию трех явлений:
- Хронический стресс снижает синаптическую и дендритную пластичность
- У лиц, страдающих депрессией, наблюдаются признаки нарушения нейропластичности (например, укорочение и снижение сложности дендритных деревьев).
- Антидепрессанты могут усиливать нейропластичность как на молекулярном, так и на дендритном уровне.
Вывод заключается в том, что нарушенная нейропластичность является основной чертой депрессии и устраняется антидепрессантами. [136]
Уровень BDNF в крови у людей с БДР значительно увеличивается при лечении антидепрессантами и коррелирует с уменьшением симптомов. [137] Исследования посмертно и модели на крысах демонстрируют снижение плотности нейронов в префронтальной коре у людей с БДР. Модели на крысах демонстрируют гистологические изменения, соответствующие результатам МРТ у людей, однако исследования нейрогенеза у людей ограничены. Антидепрессанты, по-видимому, обращают вспять изменения в нейрогенезе как у животных моделей, так и у людей. [138]
Воспаление
Различные обзоры показали, что общее воспаление может играть роль в депрессии. [139] [140] Один метаанализ цитокинов у людей с большим депрессивным расстройством обнаружил повышенные уровни провоспалительных уровней IL-6 и TNF-α по сравнению с контрольной группой. [141] Первые теории появились, когда было замечено, что терапия интерфероном вызывала депрессию у большого числа людей, получавших ее. [142] Метаанализ уровней цитокинов у людей с большим депрессивным расстройством продемонстрировал повышенные уровни IL-1 , IL-6 , C-реактивного белка , но не IL-10 . [143] [144] При депрессии наблюдалось повышенное количество Т-клеток, представляющих маркеры активации, уровни неоптерина , IFN-γ , sTNFR и рецепторов IL-2. [145] Были выдвинуты гипотезы о различных источниках воспаления при депрессивном заболевании, включая травму, проблемы со сном, диету, курение и ожирение. [146] Цитокины, манипулируя нейротрансмиттерами, участвуют в формировании болезненного поведения, которое в некоторой степени совпадает с симптомами депрессии. Гипотетически затронутыми нейротрансмиттерами являются дофамин и серотонин, которые являются обычными мишенями для антидепрессантов. Индукция индоламин- 2,3-диоксигеназы цитокинами была предложена в качестве механизма, посредством которого иммунная дисфункция вызывает депрессию . [147] В одном обзоре была обнаружена нормализация уровней цитокинов после успешного лечения депрессии. [148] Метаанализ, опубликованный в 2014 году, показал, что использование противовоспалительных препаратов, таких как НПВП и исследуемые ингибиторы цитокинов, снижает симптомы депрессии. [149] Физические упражнения могут действовать как стрессор, снижая уровни ИЛ-6 и ФНО-α и повышая уровни ИЛ-10, противовоспалительного цитокина. [150]
Воспаление также тесно связано с метаболическими процессами у людей. Например, низкий уровень витамина D был связан с повышенным риском депрессии. [151] Роль метаболических биомаркеров при депрессии является активной областью исследований. Недавние работы изучали потенциальную связь между плазменными стеролами и тяжестью симптомов депрессии. [152]
Окислительный стресс
Маркер окисления ДНК, 8-оксо-2'-дезоксигуанозин , был обнаружен повышенным как в плазме, так и в моче людей с большим депрессивным расстройством. Это, наряду с обнаружением повышенных уровней F2-изопростанов, обнаруженных в крови, моче и спинномозговой жидкости, указывает на повышенное повреждение липидов и ДНК у людей с большим депрессивным расстройством. Исследования с 8-оксо-2'-дезоксигуанозином различались по методам измерения и типу депрессии, но уровень F2-изопростана был постоянным для всех типов депрессии. Авторы предположили, что факторы образа жизни, нарушение регуляции оси HPA, иммунной системы и автономной нервной системы являются возможными причинами. [153] Другой метаанализ показал схожие результаты в отношении продуктов окислительного повреждения, а также сниженной окислительной способности. [154] Окислительное повреждение ДНК может играть роль в большом депрессивном расстройстве. [155]
Митохондриальная дисфункция
У людей с БДР были обнаружены повышенные маркеры окислительного стресса по сравнению с контрольной группой. [156] Эти маркеры включают высокие уровни АФА и АФК , которые, как было показано, влияют на хроническое воспаление, повреждая цепь переноса электронов и биохимические каскады в митохондриях . Это снижает активность ферментов в дыхательной цепи, что приводит к дисфункции митохондрий. [157] Мозг потребляет много энергии и имеет мало возможностей для хранения глюкозы в виде гликогена, поэтому сильно зависит от митохондрий. Дисфункция митохондрий связана с ослабленной нейропластичностью, наблюдаемой в депрессивном мозге. [158]
Теория крупномасштабной мозговой сети
Вместо изучения одной области мозга, изучение крупномасштабных сетей мозга является другим подходом к пониманию психиатрических и неврологических расстройств, [159] поддержанным недавними исследованиями, которые показали, что в этих расстройствах задействованы несколько областей мозга. Понимание нарушений в этих сетях может дать важные сведения о вмешательствах для лечения этих расстройств. Недавние исследования показывают, что по крайней мере три крупномасштабные сети мозга важны для психопатологии: [159]
Центральная исполнительная сеть
Центральная исполнительная сеть состоит из лобно-теменных областей, включая дорсолатеральную префронтальную кору и латеральную заднюю теменную кору. [160] [161] Эта сеть участвует в когнитивных функциях высокого уровня , таких как сохранение и использование информации в рабочей памяти , решение проблем и принятие решений. [159] [162] Дефициты в этой сети распространены при большинстве серьезных психиатрических и неврологических расстройств, включая депрессию. [163] [164] Поскольку эта сеть имеет решающее значение для повседневной жизни, у людей, страдающих депрессией, могут наблюдаться нарушения в таких основных видах деятельности, как прохождение тестов и принятие решений. [165]
Сеть в режиме по умолчанию
Сеть режима по умолчанию включает в себя концентраторы в префронтальной коре и задней поясной извилине, с другими заметными областями сети в медиальной височной доле и угловой извилине. [159] Сеть режима по умолчанию обычно активна во время блуждания ума и размышлений о социальных ситуациях. Напротив, во время определенных задач, исследуемых в когнитивной науке (например, простых задач на внимание), сеть по умолчанию часто деактивируется. [166] [167] Исследования показали, что области в сети режима по умолчанию (включая медиальную префронтальную кору и заднюю поясную извилину) демонстрируют большую активность, когда участники с депрессией размышляют (то есть когда они занимаются повторяющимся самофокусированным мышлением), чем когда размышляют типичные здоровые участники. [168] Люди с большим депрессивным расстройством также демонстрируют повышенную связанность между сетью режима по умолчанию и субгенуальной поясной извилиной и прилегающей вентромедиальной префронтальной корой по сравнению со здоровыми людьми, людьми с деменцией или с аутизмом. Многочисленные исследования показывают, что субгенуальная поясная извилина играет важную роль в дисфункции, которая характеризует большую депрессию. [169] Повышенная активация в сети пассивного режима во время размышлений и нетипичная связь между основными областями пассивного режима и субгенуальной поясной извилиной могут лежать в основе тенденции человека, страдающего депрессией, «застревать» в негативных, сосредоточенных на себе мыслях, которые часто характеризуют депрессию. [170] Однако необходимы дальнейшие исследования, чтобы получить точное понимание того, как эти сетевые взаимодействия соотносятся с конкретными симптомами депрессии.
Сеть значимости
Сеть заметности — это сеть поясной извилины и лобной оболочки, которая включает основные узлы в передней поясной извилине и передней островковой доле. [160] Сеть заметности — это крупномасштабная мозговая сеть, участвующая в обнаружении и ориентации наиболее важных внешних стимулов и внутренних событий, которые представляются. [159] У людей, которые склонны испытывать негативные эмоциональные состояния (имеющих высокие баллы по показателям невротизма ), наблюдается увеличение правой передней островковой доли во время принятия решений, даже если решение уже принято. [171] Считается, что эта нетипично высокая активность в правой передней островковой доле способствует переживанию негативных и тревожных чувств. [172] При большом депрессивном расстройстве тревога часто является частью эмоционального состояния, которое характеризует депрессию. [173]
Смотрите также
- Эпигенетика депрессии
- Фиксаторы разума
- Энн Харрингтон § Психотерапевты: Беспокойный поиск психиатрией биологии психических заболеваний
Ссылки
- ^ Чжан, Фэй-Фэй; Пэн, Вэй; Суини, Джон А.; Цзя, Чжи-Юнь; Гун, Ци-Юн (ноябрь 2018 г.). «Изменения структуры мозга при депрессии: психорадиологические данные». CNS Neuroscience & Therapeutics . 24 (11): 994–1003. doi :10.1111/cns.12835. ISSN 1755-5949. PMC 6489983 . PMID 29508560.
- ^ Серефко, Анна; Шопа, Александра; Полешак, Ева (1 марта 2016 г.). «Магний и депрессия». Исследования магния . 29 (3): 112–119. doi :10.1684/mrh.2016.0407 (неактивен с 1 ноября 2024 г.). ISSN 1952-4021. ПМИД 27910808.
{{cite journal}}: CS1 maint: DOI неактивен по состоянию на ноябрь 2024 г. ( ссылка ) - ^ Гэн, Чунмей; Шейх, Абдул Сами; Хан, Вэньсю; Чэнь, Дэн; Го, Юйцзинь; Цзян, Пей (2019). «Витамин D и депрессия: механизмы, определение и применение». Asia Pacific Journal of Clinical Nutrition . 28 (4): 689–694. doi :10.6133/apjcn.201912_28(4).0003. ISSN 1440-6047. PMID 31826364.
- ^ Anglin, Rebecca E.; Tarnopolsky, Mark A.; Mazurek, Michael F.; Rosebush, Patricia I. (январь 2012 г.). «Психиатрическое представление митохондриальных расстройств у взрослых». The Journal of Neuropsychiatry and Clinical Neurosciences . 24 (4): 394–409. doi :10.1176/appi.neuropsych.11110345. ISSN 0895-0172. PMID 23224446.
- ^ CARROLL, BERNARD J. (октябрь 2004 г.). «Психонейроэндокринология: научная основа клинической практики. Под редакцией OM Wolkowitz и AJ Rothschild. (Стр. 606; $73.95; ISBN 0-88048-857-3 pb.) American Psychiatric Publishing, Inc.: Арлингтон, Вирджиния, 2003 г.». Психологическая медицина . 34 (7): 1359–1360. doi :10.1017/S0033291704213678. ISSN 0033-2917. S2CID 73645516.
- ^ Купфер DJ, Фрэнк E, Филлипс ML (17 марта 2012 г.). «Большое депрессивное расстройство: новые клинические, нейробиологические и терапевтические перспективы». Lancet . 379 (9820): 1045–55. doi :10.1016/S0140-6736(11)60602-8. PMC 3397431 . PMID 22189047.
- ^ aan het Rot M, Mathew SJ, Charney DS (3 февраля 2009 г.). «Нейробиологические механизмы при большом депрессивном расстройстве». Журнал Канадской медицинской ассоциации . 180 (3): 305–13. doi :10.1503/cmaj.080697. PMC 2630359. PMID 19188629 .
- ^ Левинсон, Дуглас Ф.; Николс, Уолтер Э. (2018). "24. Генетика депрессии". В Чарни, Деннис С.; Склар, Памела; Буксбаум, Джозеф Д.; Нестлер, Эрик Дж. (ред.). Нейробиология психических заболеваний Чарни и Нестлера (5-е изд.). Нью-Йорк: Oxford University Press. стр. 310.
- ^ Каспи, Авшалом; Сагден, Карен; Моффитт, Терри Э.; Тейлор, Алан; Крейг, Ян В.; Харрингтон, Хонали; МакКлей, Джозеф; Милл, Джонатан; Мартин, Джуди; Брейтуэйт, Энтони; Поултон, Ричи (июль 2003 г.). «Влияние жизненного стресса на депрессию: модерация полиморфизмом гена 5-HTT». Science . 301 (5631): 386–89. Bibcode :2003Sci...301..386C. doi :10.1126/science.1083968. PMID 12869766. S2CID 146500484.
- ^ Kendler KS, Kuhn JW, Vittum J, Prescott CA, Riley B (май 2005 г.). «Взаимодействие стрессовых жизненных событий и полиморфизма транспортера серотонина в прогнозировании эпизодов большой депрессии: репликация». Архивы общей психиатрии . 62 (5): 529–35. doi : 10.1001/archpsyc.62.5.529 . PMID 15867106.
- ^ Risch N, Herrell R, Lehner T, Liang KY, Eaves L, Hoh J, Griem A, Kovacs M, Ott J, Merikangas KR (июнь 2009 г.). «Взаимодействие между геном переносчика серотонина (5-HTTLPR), стрессовыми жизненными событиями и риском депрессии: метаанализ». JAMA . 301 (23): 2462–71. doi :10.1001/jama.2009.878. PMC 2938776 . PMID 19531786.
- ^ Munafò MR, Durrant C, Lewis G, Flint J (февраль 2009 г.). «Взаимодействие гена X с окружающей средой в локусе транспортера серотонина». Биологическая психиатрия . 65 (3): 211–19. doi :10.1016/j.biopsych.2008.06.009. PMID 18691701. S2CID 5780325.
- ^ Карг К, Бурмейстер М, Шедден К, Сен С (май 2011). «Повторный анализ варианта промотора транспортера серотонина (5-HTTLPR), стресса и депрессии: доказательства генетической умеренности». Архивы общей психиатрии . 68 (5): 444–54. doi :10.1001/archgenpsychiatry.2010.189. PMC 3740203. PMID 21199959 .
- ^ Culverhouse RC, Saccone NL, Horton AC, Ma Y, Anstey KJ, Banaschewski T и др. (январь 2018 г.). «Совместный метаанализ не выявил доказательств сильного взаимодействия между стрессом и генотипом 5-HTTLPR, способствующим развитию депрессии». Молекулярная психиатрия . 23 (1): 133–142. doi :10.1038/mp.2017.44. PMC 5628077. PMID 28373689 .
- ^ Ниренберг, АА (2009). «Длинная история короткого плеча промоутерной области гена, кодирующего белок захвата серотонина». CNS Spectrums . 14 (9): 462–3. doi :10.1017/s1092852900023506. PMID 19890228. S2CID 24236284.
- ^ ab Border, Richard; Johnson, Emma; Evans, Luke; Smolen, Andrew; Berley, Noah; Sullivan, Patrick; Keller, Matthew (1 мая 2019 г.). «Нет поддержки для исторических гипотез гена-кандидата или гипотез гена-кандидата по взаимодействию для большой депрессии в нескольких больших выборках». American Journal of Psychiatry . 176 (5): 376–387. doi : 10.1176/appi.ajp.2018.18070881 . PMC 6548317 . PMID 30845820.
- ^ Конвергентный консорциум; Бигдели, Тим Б.; Кречмар, Уоррен; Ли, Ихан; Лян, Цзецинь; Сун, Ли; Ху, Цзинчу; Ли, Цибинь; Джин, Вэй; Ху, Женфэй; Ван, Гуанбяо; Ван, Линьмао; Цянь, Пуи; Лю, Юань; Цзян, Тао; Лу, Яо; Чжан, Сюцин; Инь, Йе; Ли, Инжуй; Сюй, Сюнь; Гао, Цзинфан; Реймерс, Марк; Уэбб, Тодд; Райли, Брайен; Бакану, Сильвиу; Петерсон, Розанна Э.; Чен, Ипин; Чжун, Хуэй; Лю, Чжэнжун; и др. (2015). «Редкое полногеномное секвенирование идентифицирует два локуса большого депрессивного расстройства». Природа . 523 (7562): 588–91. Bibcode :2015Natur.523..588C. doi : 10.1038/nature14659. PMC 4522619. PMID 26176920.
- ^ Smoller, Jordan W (2015). «Генетика расстройств, связанных со стрессом: ПТСР, депрессия и тревожные расстройства». Neuropsychopharmacology . 41 (1): 297–319. doi :10.1038/npp.2015.266. PMC 4677147. PMID 26321314 .
- ^ Чжао, Сяофэн; Хуан, Инлинь; Ма, Хуэй; Цзинь, Цю; Ван, Юань; Чжу, Ган (15 августа 2013 г.). «Связь между большим депрессивным расстройством и полиморфизмами транспортера норадреналина T-182C и G1287A: метаанализ». Журнал аффективных расстройств . 150 (1): 23–28. doi :10.1016/j.jad.2013.03.016. ISSN 1573-2517. PMID 23648227.
- ^ Lohoff, Falk W. (6 декабря 2016 г.). «Обзор генетики большого депрессивного расстройства». Current Psychiatry Reports . 12 (6): 539–546. doi :10.1007/s11920-010-0150-6. ISSN 1523-3812. PMC 3077049. PMID 20848240 .
- ^ Лопес-Леон, С.; Янссенс, ACJW; Гонсалес-Сулоэта Лэдд, AM; Дель-Фаверо, Дж.; Клаас, С.Дж.; Оостра, Бакалавр; ван Дуйн, CM (1 августа 2008 г.). «Метаанализ генетических исследований большого депрессивного расстройства». Молекулярная психиатрия . 13 (8): 772–785. дои : 10.1038/sj.mp.4002088 . ISSN 1476-5578. ПМИД 17938638.
- ^ ab Карлсон, Нил Р. (2013). Физиология поведения (11-е изд.). Бостон: Пирсон. С. 578–582. ISBN 978-0-205-23939-9. OCLC 769818904.
- ^ Сатьянараянан, Сентил Кумаран; Су, Хуаньсин; Линь, И-Вэнь; Су, Куан-Пин (19 октября 2018 г.). «Циркадный ритм и мелатонин в лечении депрессии». Текущий фармацевтический дизайн . 24 (22): 2549–2555. дои : 10.2174/1381612824666180803112304. PMID 30073921. S2CID 51904516.
- ^ Фан, Хонг; Ту, Шэн; Шэн, Цзифан; Шао, Аньвэнь (апрель 2019 г.). «Депрессия при нарушении сна: обзор двунаправленной связи, механизмов и лечения». Журнал клеточной и молекулярной медицины . 23 (4): 2324–2332. doi :10.1111/jcmm.14170. PMC 6433686. PMID 30734486 .
- ^ Ван, И-Цюнь; Ли, Руй; Чжан, Мэн-Ци; Чжан, Цзе; Цюй, Вэй-Мин; Хуан, Чжи-Ли (31 августа 2015 г.). «Нейробиологические механизмы и методы лечения нарушений быстрого сна при депрессии». Current Neuropharmacology . 13 (4): 543–553. doi :10.2174/1570159x13666150310002540. PMC 4790401. PMID 26412074 .
- ^ abc Adrien J. (2003). «Нейробиологические основы связи между сном и депрессией». Sleep Medicine Reviews . 6 (5): 341–51. doi :10.1053/smrv.2001.0200. PMID 12531125.
- ^ ab Terman M (2007). «Развивающиеся применения светотерапии». Sleep Medicine Reviews . 11 (6): 497–507. doi :10.1016/j.smrv.2007.06.003. PMID 17964200. S2CID 2054580.
- ^ Бенедетти Ф, Барбини Б, Коломбо С, Смеральди Э (2007). «Хронотерапия в психиатрическом отделении». Обзоры медицины сна . 11 (6): 509–22. doi :10.1016/j.smrv.2007.06.004. ПМИД 17689120.
{{cite journal}}: CS1 maint: несколько имен: список авторов ( ссылка ) - ^ Чжай, Лонг; Чжан, Хуа; Чжан, Дунфэн (1 сентября 2015 г.). «Продолжительность сна и депрессия среди взрослых: метаанализ перспективных исследований». Депрессия и тревога . 32 (9): 664–670. doi : 10.1002/da.22386 . ISSN 1520-6394. PMID 26047492. S2CID 19071838.
- ^ Germain, Anne; Kupfer, David J. (6 декабря 2016 г.). «Нарушения циркадного ритма при депрессии». Human Psychopharmacology . 23 (7): 571–585. doi :10.1002/hup.964. ISSN 0885-6222. PMC 2612129. PMID 18680211 .
- ^ Savitz, Jonathan B.; Drevets, Wayne C. (1 апреля 2013 г.). «Визуализация нейрорецепторов при депрессии». Neurobiology of Disease . 52 : 49–65. doi : 10.1016/j.nbd.2012.06.001 . ISSN 1095-953X. PMID 22691454.
- ^ Карлсон, Нил Р. (2005). Основы физиологической психологии (6-е изд.). Бостон: Пирсон А. и Б. стр. 108. ISBN 978-0-205-42723-9. OCLC 60880502.
- ^ Маршан; Валентина; Йенсен. «Нейробиология расстройств настроения». Врач больницы : 17–26.
- ^ Hjorth, S; Bengtsson, HJ; Kullberg, A; Carlzon, D; Peilot, H; Auerbach, SB (июнь 2000 г.). «Функция ауторецептора серотонина и действие антидепрессантов». Журнал психофармакологии . 14 (2): 177–85. doi :10.1177/026988110001400208. PMID 10890313. S2CID 33440228.
- ^ ab Moncrieff, Joanna ; Horowitz, Mark (20 июля 2022 г.). «Депрессия, вероятно, не вызвана химическим дисбалансом в мозге – новое исследование». The Conversation . Получено 21 июля 2022 г. .
- ^ Монкрифф, Джоанна ; Купер, Рут Э.; Стокманн, Том; Амендола, Симона; Хенгартнер, Майкл П.; Горовиц, Марк А. (20 июля 2022 г.). «Теория серотонина в депрессии: систематический обзор доказательств». Молекулярная психиатрия . 28 (8): 3243–3256. doi : 10.1038/s41380-022-01661-0 . ISSN 1476-5578. PMC 10618090. PMID 35854107. S2CID 250646781 .
- ^ Cipriani, Andrea; Furukawa, Toshi A.; Chaimani, Anna; Atkinson, Lauren Z.; Ogawa, Yusuke; Leucht, Stefan. (8 февраля 2018 г.). «Сравнительная эффективность и приемлемость 21 антидепрессанта для острого лечения взрослых с большим депрессивным расстройством: систематический обзор и сетевой метаанализ». The Lancet . 391 (10128): 1357–1366. doi :10.1016/S0140-6736(17)32802-7. PMC 5889788 . PMID 29477251.
- ^ «Реакция экспертов на обзорную статью о «серотониновой теории депрессии» | Научный медиацентр».
- ^ ab COWEN, P (сентябрь 2008 г.). «Серотонин и депрессия: патофизиологический механизм или маркетинговый миф?». Trends in Pharmacological Sciences . 29 (9): 433–436. doi :10.1016/j.tips.2008.05.004. PMID 18585794.
- ^ ab Harmer, CJ (ноябрь 2008 г.). «Серотонин и эмоциональная обработка: помогает ли это объяснить действие антидепрессантов?». Neuropharmacology . 55 (6): 1023–8. doi :10.1016/j.neuropharm.2008.06.036. PMID 18634807. S2CID 43480495.
- ^ Данлоп, Боди В.; Немерофф, Чарльз Б. (1 апреля 2007 г.). «Роль дофамина в патофизиологии депрессии». Архив общей психиатрии . 64 (3): 327–37. doi :10.1001/archpsyc.64.3.327. ISSN 0003-990X. PMID 17339521. S2CID 26550661.
- ^ Виллнер, Пол (1 декабря 1983 г.). «Дофамин и депрессия: обзор последних данных. I. Эмпирические исследования». Brain Research Reviews . 6 (3): 211–224. doi :10.1016/0165-0173(83)90005-X. PMID 6140979. S2CID 974017.
- ^ ab HASLER, GREGOR (4 декабря 2016 г.). «Патофизиология депрессии: есть ли у нас веские доказательства, представляющие интерес для клиницистов?». World Psychiatry . 9 (3): 155–161. doi :10.1002/j.2051-5545.2010.tb00298.x. ISSN 1723-8617. PMC 2950973. PMID 20975857 .
- ^ Кунуги, Хироши; Хори, Хироаки; Огава, Синтаро (1 октября 2015 г.). «Биохимические маркеры подтипирования большого депрессивного расстройства». Psychiatry and Clinical Neurosciences . 69 (10): 597–608. doi : 10.1111/pcn.12299 . ISSN 1440-1819. PMID 25825158.
- ^ Ламмель, С.; Тай, К. М.; Уорден, М. Р. (1 января 2014 г.). «Прогресс в понимании расстройств настроения: оптогенетическое препарирование нейронных цепей». Гены, мозг и поведение . 13 (1): 38–51. doi : 10.1111/gbb.12049 . ISSN 1601-183X. PMID 23682971.
- ^ Delgado PL, Moreno FA (2000). «Роль норадреналина в депрессии». J Clin Psychiatry . 61 (Suppl 1): 5–12. PMID 10703757.
- ^ Ruhe, HG; Mason, NS; Schene, AH (2007). «Настроение косвенно связано с уровнями серотонина, норадреналина и дофамина у людей: метаанализ исследований истощения моноаминов». Молекулярная психиатрия . 12 (4): 331–359. doi : 10.1038/sj.mp.4001949 . PMID 17389902.
- ^ Meyer JH, Ginovart N, Boovariwala A, et al. (Ноябрь 2006). «Повышенные уровни моноаминоксидазы a в мозге: объяснение дисбаланса моноаминов при большой депрессии». Архивы общей психиатрии . 63 (11): 1209–16. doi : 10.1001/archpsyc.63.11.1209 . PMID 17088501.
- ^ Huang SY, Lin MT, Lin WW, Huang CC, Shy MJ, Lu RB (19 декабря 2007 г.). «Связь полиморфизмов моноаминоксидазы A (MAOA) и клинических подгрупп больших депрессивных расстройств в популяции китайцев хань». World Journal of Biological Psychiatry . 10 (4 Pt 2): 544–51. doi :10.1080/15622970701816506. PMID 19224413. S2CID 30281258.
- ^ Yu YW, Tsai SJ, Hong CJ, Chen TJ, Chen MC, Yang CW (сентябрь 2005 г.). «Исследование связи полиморфизма промотора гена моноаминоксидазы a с большим депрессивным расстройством и реакцией на антидепрессанты». Neuropsychopharmacology . 30 (9): 1719–23. doi : 10.1038/sj.npp.1300785 . PMID 15956990.
- ^ Cicchetti D, Rogosch FA, Sturge-Apple ML (2007). «Взаимодействие жестокого обращения с детьми и полиморфизмов переносчика серотонина и моноаминоксидазы A: депрессивная симптоматика среди подростков из семей с низким социально-экономическим статусом». Dev. Psychopathol . 19 (4): 1161–80. doi :10.1017/S0954579407000600. PMID 17931441. S2CID 32519363.
- ^ Кастрен, Э. (2005). «Является ли настроение химией?». Nature Reviews Neuroscience . 6 (3): 241–46. doi :10.1038/nrn1629. PMID 15738959. S2CID 34523310.
- ^ Хиршфельд Р. М. (2000). «История и эволюция моноаминовой гипотезы депрессии». Журнал клинической психиатрии . 61 (Приложение 6): 4–6. PMID 10775017.
- ^ Дэвис, Кеннет Л.; и др., ред. (2002). Нейропсихофармакология: пятое поколение прогресса: официальное издание Американского колледжа нейропсихофармакологии (5-е изд.). Филадельфия, Пенсильвания: Lippincott Williams & Wilkins. стр. 1139–1163. ISBN 9780781728379.
- ^ Якобсен, Якоб PR; Медведев, Иван О.; Кэрон, Марк Г. (5 сентября 2012 г.). «Теория депрессии, обусловленная дефицитом 5-HT: перспективы натуралистической модели дефицита 5-HT, триптофангидроксилаза 2Arg439His knockin mouse». Philosophical Transactions of the Royal Society B: Biological Sciences . 367 (1601): 2444–2459. doi :10.1098/rstb.2012.0109. ISSN 0962-8436. PMC 3405680 . PMID 22826344.
- ^ Delgado PL, Moreno FA (2000). «Роль норадреналина в депрессии». J Clin Psychiatry . 61 (Suppl 1): 5–12. PMID 10703757.
- ^ Delgado PL (2000). «Депрессия: случай дефицита моноаминов». Журнал клинической психиатрии . 61 (Приложение 6): 7–11. PMID 10775018.
- ^ Эндрюс, Пол В.; Бхарвани, Аадил; Ли, Кьювон Р.; Фокс, Молли; Томсон, Дж. Андерсон (1 апреля 2015 г.). «Серотонин — это возбуждающее или подавляющее вещество? Эволюция серотонинергической системы и ее роль в депрессии и реакция на антидепрессанты». Neuroscience and Biobehavioral Reviews . 51 : 164–188. doi : 10.1016/j.neubiorev.2015.01.018. ISSN 1873-7528. PMID 25625874. S2CID 23980182.
- ^ Лакасс, Джеффри Р.; Лео, Джонатан (8 ноября 2005 г.). «Серотонин и депрессия: разрыв между рекламой и научной литературой». PLOS Medicine . 2 (12): e392. doi : 10.1371/journal.pmed.0020392 . PMC 1277931. PMID 16268734 .

- ^ Савиц, Джонатан; Древец, Уэйн (2013). «Визуализация нейрорецепторов при депрессии». Neurobiology of Disease . 52 : 49–65. doi : 10.1016/j.nbd.2012.06.001 . PMID 22691454.
- ^ Грыглевски, Г.; Ланценбергер, Р.; Кранц, Г.С.; Камминг, П. (июль 2014 г.). «Метаанализ молекулярной визуализации переносчиков серотонина при большой депрессии». Журнал мозгового кровотока и метаболизма . 34 (7): 1096–103. doi :10.1038/jcbfm.2014.82. PMC 4083395. PMID 24802331 .
- ^ Камбейц, Дж. П.; Хоус, О. Д. (1 ноября 2015 г.). «Транспортёр серотонина при депрессии: метаанализ результатов in vivo и посмертных исследований и их значение для понимания и лечения депрессии». Журнал аффективных расстройств . 186 : 358–66. doi : 10.1016/j.jad.2015.07.034. PMID 26281039.
- ^ Ван, Л.; Чжоу, К.; Чжу, Д.; Ван, Х.; Фан, Л.; Чжун, Дж.; Мао, К.; Сан, Л.; Гун, Х.; Ся, Дж.; Лянь, Б.; Се, П. (13 сентября 2016 г.). «Изменения рецептора серотонина-1А при депрессии: метаанализ исследований молекулярной визуализации». BMC Psychiatry . 16 (1): 319. doi : 10.1186/s12888-016-1025-0 . PMC 5022168 . PMID 27623971.
- ^ Li, Z; He, Y; Tang, J; Zong, X; Hu, M; Chen, X (15 марта 2015 г.). «Молекулярная визуализация транспортеров дофамина в полосатом теле при большой депрессии — метаанализ». Journal of Affective Disorders . 174 : 137–43. doi : 10.1016/j.jad.2014.11.045. PMID 25497470.
- ^ Бурк, Сесилия; Дуглас, Кэти; Портер, Ричард (1 августа 2010 г.). «Обработка выражения эмоций на лице при большой депрессии: обзор». Австралийский и новозеландский журнал психиатрии . 44 (8): 681–696. doi :10.3109/00048674.2010.496359. ISSN 1440-1614. PMID 20636189. S2CID 20302084.
- ^ Dalili, MN; Penton-Voak, IS; Harmer, CJ; Munafò, MR (7 декабря 2016 г.). «Метаанализ дефицита распознавания эмоций при большом депрессивном расстройстве». Psychological Medicine . 45 (6): 1135–1144. doi :10.1017/S0033291714002591. ISSN 0033-2917. PMC 4712476 . PMID 25395075.
- ^ Groenewold, Nynke A.; Opmeer, Esther M.; de Jonge, Peter; Aleman, André; Costafreda, Sergi G. (1 февраля 2013 г.). «Эмоциональная валентность модулирует функциональные отклонения мозга при депрессии: доказательства из метаанализа исследований фМРТ». Neuroscience and Biobehavioral Reviews . 37 (2): 152–163. doi :10.1016/j.neubiorev.2012.11.015. ISSN 1873-7528. PMID 23206667. S2CID 9980163.
- ^ Мюллер, VI; Чеслик, EC; Сербанеску, I; Лэрд, AR; Фокс, PT; Эйкхофф, SB (1 января 2017 г.). «Измененная активность мозга при униполярной депрессии: метаанализ исследований нейровизуализации». JAMA Psychiatry . 74 (1): 47–55. doi :10.1001/jamapsychiatry.2016.2783. PMC 5293141 . PMID 27829086.
- ^ Harmer, CJ; Goodwin, GM; Cowen, PJ (31 июля 2009 г.). «Почему антидепрессанты так долго действуют? Когнитивная нейропсихологическая модель действия антидепрессантов». Британский журнал психиатрии . 195 (2): 102–108. doi : 10.1192/bjp.bp.108.051193 . PMID 19648538.
- ^ Delaveau, P; Jabourian, M; Lemogne, C; Guionnet, S; Bergouignan, L; Fossati, P (апрель 2011 г.). «Влияние антидепрессантов на мозг при тяжелой депрессии: метаанализ исследований эмоциональной обработки». Журнал аффективных расстройств . 130 (1–2): 66–74. doi :10.1016/j.jad.2010.09.032. PMID 21030092.
- ^ Pringle, A; Harmer, CJ (декабрь 2015 г.). «Влияние лекарств на человеческие модели эмоциональной обработки: отчет о лечении антидепрессантами». Dialogues in Clinical Neuroscience . 17 (4): 477–87. doi :10.31887/DCNS.2015.17.4/apringle. PMC 4734885. PMID 26869848 .
- ^ abc Hamilton, J. Paul; Etkin, Amit; Furman, Daniella J.; Lemus, Maria G.; Johnson, Rebecca F.; Gotlib, Ian H. (1 июля 2012 г.). «Функциональная нейровизуализация большого депрессивного расстройства: метаанализ и новая интеграция данных об активации базовой линии и нейронном ответе». The American Journal of Psychiatry . 169 (7): 693–703. doi :10.1176/appi.ajp.2012.11071105. ISSN 1535-7228. PMID 22535198.
- ^ Drevets, WC; Price, JL; Furey, ML (сентябрь 2008 г.). «Структурные и функциональные аномалии мозга при расстройствах настроения: последствия для нейросетевых моделей депрессии». Brain Structure & Function . 213 (1–2): 93–118. doi :10.1007/s00429-008-0189-x. PMC 2522333. PMID 18704495 .
- ^ Древец, WC (апрель 2001 г.). «Нейровизуализация и нейропатологические исследования депрессии: влияние на когнитивно-эмоциональные особенности расстройств настроения». Current Opinion in Neurobiology . 11 (2): 240–9. doi :10.1016/S0959-4388(00)00203-8. PMID 11301246. S2CID 36416079.
- ^ Mayberg, Helen (1 августа 1997 г.). «Лимбико-кортикальная дисрегуляция: предложенная модель депрессии». Журнал нейропсихиатрии и клинических нейронаук . 9 (3): 471–481. doi :10.1176/jnp.9.3.471. ISSN 0895-0172. PMID 9276848.
- ^ ab Грэм, Джулия; Салими-Хоршиди, Голамреза; Хаган, Синди; Уолш, Николас; Гудьер, Ян; Леннокс, Белинда; Саклинг, Джон (1 ноября 2013 г.). «Метааналитические данные в пользу нейровизуализационных моделей депрессии: состояние или черта?». Журнал аффективных расстройств . 151 (2): 423–431. doi : 10.1016/j.jad.2013.07.002 . PMID 23890584.
- ^ Антицевич, А; Шлейфер, К; Янгсан, ТС (декабрь 2015 г.). «Эмоциональная и когнитивная дисрегуляция при шизофрении и депрессии: понимание общих и отдельных поведенческих и нейронных механизмов». Диалоги в клинической нейронауке . 17 (4): 421–34. doi :10.31887/DCNS.2015.17.4/aanticevic. PMC 4734880. PMID 26869843 .
- ^ Рёмер Томсен, К.; Уайброу, П. К.; Крингельбах, М. Л. (2015). «Переосмысление ангедонии: новые перспективы балансировки сетей удовольствия в человеческом мозге». Frontiers in Behavioral Neuroscience . 9 : 49. doi : 10.3389/fnbeh.2015.00049 . PMC 4356228. PMID 25814941 .
- ^ Treadway, MT; Zald, DH (январь 2011). «Переосмысление ангедонии при депрессии: уроки трансляционной нейронауки». Neuroscience and Biobehavioral Reviews . 35 (3): 537–55. doi :10.1016/j.neubiorev.2010.06.006. PMC 3005986. PMID 20603146 .
- ^ abc Sternat T, Katzman MA (1 января 2016 г.). «Нейробиология гедонистического тона: связь между резистентной к терапии депрессией, синдромом дефицита внимания и гиперактивности и злоупотреблением психоактивными веществами». Neuropsychiatric Disease and Treatment . 12 : 2149–64. doi : 10.2147/NDT.S111818 . PMC 5003599. PMID 27601909 .
- ^ Russo, SJ; Nestler, EJ (сентябрь 2013 г.). «Контур вознаграждения мозга при расстройствах настроения». Nature Reviews. Neuroscience . 14 (9): 609–25. doi : 10.1038/nrn3381. PMC 3867253. PMID 23942470.
- ^ Роллс, ET (сентябрь 2016 г.). «Теория депрессии как аттрактора без вознаграждения» (PDF) . Neuroscience and Biobehavioral Reviews . 68 : 47–58. doi : 10.1016/j.neubiorev.2016.05.007. PMID 27181908. S2CID 8145667.
- ^ Miller, CH; Hamilton, JP; Sacchet, MD; Gotlib, IH (октябрь 2015 г.). «Метаанализ функциональной нейровизуализации большого депрессивного расстройства у молодежи». JAMA Psychiatry . 72 (10): 1045–53. doi : 10.1001/jamapsychiatry.2015.1376 . PMID 26332700.
- ^ Грэм, Дж.; Салими-Хоршиди, Г.; Хаган, К.; Уолш, Н.; Гудьер, И.; Леннокс, Б.; Саклинг, Дж. (ноябрь 2013 г.). «Метааналитические данные о нейровизуализационных моделях депрессии: состояние или черта?». Журнал аффективных расстройств . 151 (2): 423–31. doi : 10.1016/j.jad.2013.07.002 . PMID 23890584.
- ^ Drevets, WC; Savitz, J; Trimble, M (август 2008 г.). «Субгенуальная передняя поясная кора при расстройствах настроения». CNS Spectrums . 13 (8): 663–81. doi :10.1017/S1092852900013754. PMC 2729429 . PMID 18704022.
- ^ ab Lammel, S; Tye, KM; Warden, MR (январь 2014 г.). «Прогресс в понимании расстройств настроения: оптогенетическое препарирование нейронных цепей». Genes, Brain and Behavior . 13 (1): 38–51. doi : 10.1111/gbb.12049 . PMID 23682971.
- ^ Groenewold, NA; Opmeer, EM; de Jonge, P; Aleman, A; Costafreda, SG (февраль 2013 г.). «Эмоциональная валентность модулирует функциональные нарушения мозга при депрессии: доказательства из метаанализа исследований фМРТ». Neuroscience and Biobehavioral Reviews . 37 (2): 152–63. doi :10.1016/j.neubiorev.2012.11.015. PMID 23206667. S2CID 9980163.
- ^ Drevets, WC; Savitz, J; Trimble, M (август 2008 г.). «Субгенуальная передняя поясная кора при расстройствах настроения». CNS Spectrums . 13 (8): 663–81. doi :10.1017/S1092852900013754. PMC 2729429 . PMID 18704022.
В совокупности эти данные предполагают гипотезу о том, что дисфункция sgACC приводит к недостаточной стимуляции парасимпатического тонуса при расстройствах настроения.
- ^ Rive, MM; van Rooijen, G; Veltman, DJ; Phillips, ML; Schene, AH; Ruhé, HG (декабрь 2013 г.). «Нейронные корреляты дисфункциональной регуляции эмоций при большом депрессивном расстройстве. Систематический обзор исследований нейровизуализации». Neuroscience and Biobehavioral Reviews . 37 (10 Pt 2): 2529–53. doi :10.1016/j.neubiorev.2013.07.018. PMID 23928089. S2CID 33607901.
- ^ Данлоп, Б. В.; Майберг, Х. С. (декабрь 2014 г.). «Биомаркеры на основе нейровизуализации для выбора лечения при большом депрессивном расстройстве». Диалоги в клинической нейронауке . 16 (4): 479–90. doi : 10.31887/DCNS.2014.16.4/bdunlop. PMC 4336918. PMID 25733953.
- ^ Мудрый, Т; Радуа, Дж; Виа, Е; Кардонер, Н.; Эйб, О; Адамс, ТМ; Амико, Ф; Ченг, Ю; Коул, Дж. Х.; де Азеведо Маркес Перико, C; Дикштейн, ДП; Фэрроу, TFD; Фродл, Т; Вагнер, Г; Готлиб, штат Айдахо; Грубер, О; Хэм, Би Джей; Джоб, Делавэр; Кемптон, MJ; Ким, MJ; Коольшейн, PCMP; Малхи, Г.С.; Матэ-Колс, Д; Макинтош, AM; Ньюджент, AC; О'Брайен, Джей Ти; Пеццоли, С; Филлипс, ML; Сачдев, П.С.; Сальвадор, Дж; Сельварадж, С; Стэнфилд, AC; Томас, Эй Джей; ван Тол, MJ; ван дер Ви, Нью-Джерси; Вельтман, диджей; Янг, АХ; Fu, CH; Cleare, AJ; Arnone, D (октябрь 2017 г.). «Общие и отличительные закономерности изменения объема серого вещества при большой депрессии и биполярном расстройстве: данные метаанализа на основе вокселей». Молекулярная психиатрия . 22 (10 ): 1455–1463. doi :10.1038/mp.2016.72. PMC 5622121 . PMID 27217146.
- ^ Бора, Э.; Форнито, А.; Пантелис, К.; Юсель, М. (апрель 2012 г.). «Аномалии серого вещества при большом депрессивном расстройстве: метаанализ исследований морфометрии на основе вокселей». Журнал аффективных расстройств . 138 (1–2): 9–18. doi :10.1016/j.jad.2011.03.049. PMID 21511342.
- ^ Чжан, Х.; Ли, Л.; У, М.; Чен, З.; Ху, Х.; Чен, И.; Чжу, Х.; Цзя, З.; Гун, К. (январь 2016 г.). «Изменения серого вещества мозга при первых эпизодах депрессии: метаанализ исследований всего мозга». Neuroscience and Biobehavioral Reviews . 60 : 43–50. doi : 10.1016/j.neubiorev.2015.10.011. PMID 26592799. S2CID 207092294.
- ^ Чжао, YJ; Ду, MY; Хуан, XQ; Луи, S; Чэнь, ZQ; Лю, J; Луо, Y; Ван, XL; Кемп, GJ; Гун, QY (октябрь 2014 г.). «Аномалии серого вещества мозга у пациентов с тяжелым депрессивным расстройством, не принимающих лекарства: метаанализ». Психологическая медицина . 44 (14): 2927–37. doi : 10.1017/S0033291714000518 . PMID 25065859.
- ^ Sacher, J; Neumann, J; Fünfstück, T; Soliman, A; Villringer, A; Schroeter, ML (октябрь 2012 г.). «Картирование депрессивного мозга: метаанализ структурных и функциональных изменений при большом депрессивном расстройстве». Journal of Affective Disorders . 140 (2): 142–8. doi : 10.1016/j.jad.2011.08.001 . PMID 21890211.
- ^ Arnone, D; Job, D; Selvaraj, S; Abe, O; Amico, F; Cheng, Y; Colloby, SJ; O'Brien, JT; Frodl, T; Gotlib, IH; Ham, BJ; Kim, MJ; Koolschijn, PC; Périco, CA; Salvadore, G; Thomas, AJ; Van Tol, MJ; van der Wee, NJ; Veltman, DJ; Wagner, G; McIntosh, AM (апрель 2016 г.). «Вычислительный метаанализ статистических параметрических карт при большой депрессии». Картирование человеческого мозга . 37 (4): 1393–404. doi :10.1002/hbm.23108. PMC 6867585. PMID 26854015 .
- ^ Шмаал, Л; Хибар, ДП; Земанн, П.Г.; Холл, Великобритания; Бауне, Британская Колумбия; Джаханшад, Н.; Чунг, Дж.В.; ван Эрп, TGM; Бос, Д; Икрам, Массачусетс; Верной, М.В.; Ниссен, WJ; Тимейер, Х; Хофман, А; Витфельд, К; Грабе, HJ; Яновиц, Д; Бюлов, Р; Селонке, М; Вёльцке, Х; Гротегерд, Д; Даннловски, Ю; Арольт, В; Опель, Н; Хейндель, В; Кугель, Х; Хен, Д; Чиш, М; Куви-Дюшен, Б; Рентерия, Мэн; Страйк, LT; Райт, MJ; Миллс, Северная Каролина; де Зубикарай, Дж.И.; МакМахон, КЛ; Медланд, ЮВ; Мартин, Нью-Йорк; Гиллеспи, Северная Каролина; Гойя-Мальдонадо, Р; Грубер, О; Кремер, Б; Хаттон, С.Н.; Лагопулос, Дж; Хики, ИБ; Фродл, Т; Карбальедо, А; Фрей, Э.М.; ван Вельзен, Л.С.; Пеннинкс, BWJH; ван Тол, MJ; ван дер Ви, Нью-Джерси; Дэйви, CG; Харрисон, Би Джей; Мванги, Б; Цао, Б; Соареш, Дж. К.; Вир, И.М.; Уолтер, Х; Шепф, Д; Зуровский, Б; Конрад, К; Шрамм, Э; Норманн, К; Шнелл, К; Саше, доктор медицины; Готлиб, штат Айдахо; МакКуин, генеральный директор; Годлевска, БР; Никсон, Т; Макинтош, AM; Папмейер, М; Уолли, ХК; Холл, Дж.; Сассманн, Дж. Э.; Ли, М.; Уолтер, М.; Афтанас, Л.; Брак, И.; Бохан, Н. А.; Томпсон, П. М.; Вельтман, Д. Дж. (июнь 2017 г.). «Кортикальные аномалии у взрослых и подростков с тяжелой депрессией на основе сканирования мозга 20 групп по всему миру в рабочей группе ENIGMA Major Depressive Disorder». Молекулярная психиатрия . 22 (6): 900–909. doi :10.1038/mp.2016.60. PMC 5444023. PMID 27137745 .
- ^ Шмаал, Л; Вельтман, диджей; ван Эрп, Т.Г.; Земанн, П.Г.; Фродл, Т; Джаханшад, Н.; Лёрер, Э; Тимейер, Х; Хофман, А; Ниссен, WJ; Верной, М.В.; Икрам, Массачусетс; Витфельд, К; Грабе, HJ; Блок, А; Хегеншайд, К; Вёльцке, Х; Хен, Д; Чиш, М; Лагопулос, Дж; Хаттон, С.Н.; Хики, ИБ; Гойя-Мальдонадо, Р; Кремер, Б; Грубер, О; Куви-Дюшен, Б; Рентерия, Мэн; Страйк, LT; Миллс, Северная Каролина; де Зубикарай, Дж.И.; МакМахон, КЛ; Медланд, ЮВ; Мартин, Нью-Йорк; Гиллеспи, Северная Каролина; Райт, М.Дж.; Холл, ГБ; Маккуин, ГМ; Фрей, Э.М.; Карбалледо, А.; ван Велзен, Л.С.; ван Тол, М.Дж.; ван дер Ви, Н.Дж.; Вир, И.М.; Вальтер, Х.; Шнелл, К.; Шрамм, E; Норманн, C; Шёпф, D; Конрад, C; Зуровски, B; Никсон, T; Макинтош, AM; Папмейер, M; Уолли, HC; Сассманн, JE; Годлевска, BR; Коуэн, PJ; Фишер, FH; Rose, M; Penninx, BW; Thompson, PM; Hibar, DP (июнь 2016 г.). «Подкорковые изменения мозга при большом депрессивном расстройстве: выводы рабочей группы ENIGMA по большому депрессивному расстройству». Молекулярная психиатрия . 21 (6): 806– 12. doi : 10.1038 / mp.2015.69.PMC 4879183.PMID 26122586 .
- ^ abcd Chen, G; Hu, X; Li, L; Huang, X; Lui, S; Kuang, W; Ai, H; Bi, F; Gu, Z; Gong, Q (24 февраля 2016 г.). «Дезорганизация архитектуры белого вещества при большом депрессивном расстройстве: метаанализ диффузионно-тензорной визуализации с пространственной статистикой на основе тракта». Scientific Reports . 6 : 21825. Bibcode :2016NatSR...621825C. doi :10.1038/srep21825. PMC 4764827 . PMID 26906716.
- ^ abcd Chen, G; Guo, Y; Zhu, H; Kuang, W; Bi, F; Ai, H; Gu, Z; Huang, X; Lui, S; Gong, Q (2 июня 2017 г.). «Внутреннее нарушение микроархитектуры белого вещества при первом эпизоде большого депрессивного расстройства, не принимавшего лекарства: метаанализ на основе вокселей диффузионно-тензорной визуализации». Progress in Neuro-psychopharmacology & Biological Psychiatry . 76 : 179–187. doi :10.1016/j.pnpbp.2017.03.011. PMID 28336497. S2CID 4610677.
- ^ abcd Jiang, J; Zhao, YJ; Hu, XY; Du, MY; Chen, ZQ; Wu, M; Li, KM; Zhu, HY; Kumar, P; Gong, QY (май 2017 г.). «Микроструктурные аномалии мозга у пациентов с большим депрессивным расстройством, не принимающих лекарства: систематический обзор и метаанализ диффузионно-тензорной визуализации». Journal of Psychiatry & Neuroscience . 42 (3): 150–163. doi :10.1503/jpn.150341. PMC 5403660 . PMID 27780031.
- ^ ab Wise, T; Radua, J; Nortje, G; Cleare, AJ; Young, AH; Arnone, D (15 февраля 2016 г.). «Воксельные метааналитические доказательства структурной разобщенности при большой депрессии и биполярном расстройстве». Биологическая психиатрия . 79 (4): 293–302. doi : 10.1016/j.biopsych.2015.03.004 . PMID 25891219.
- ^ Чжоу, М; Ху, X; Лу, Л; Чжан, Л; Чэнь, Л; Гун, К; Хуан, X (3 апреля 2017 г.). «Внутренняя мозговая активность в состоянии покоя у взрослых с большим депрессивным расстройством: метаанализ». Прогресс в нейропсихофармакологии и биологической психиатрии . 75 : 157–164. doi :10.1016/j.pnpbp.2017.02.001. PMID 28174129. S2CID 20054773.
- ^ Li, W; Chen, Z; Wu, M; Zhu, H; Gu, L; Zhao, Y; Kuang, W; Bi, F; Kemp, GJ; Gong, Q (1 марта 2017 г.). «Характеристика мозгового кровотока и амплитуда низкочастотных колебаний при большом депрессивном расстройстве: мультимодальный метаанализ». Journal of Affective Disorders . 210 : 303–311. doi : 10.1016/j.jad.2016.12.032. PMID 28068619.
- ^ Кюн, С.; Галлинат, Дж. (март 2013 г.). «Активность мозга в состоянии покоя при шизофрении и большой депрессии: количественный метаанализ». Schizophrenia Bulletin . 39 (2): 358–65. doi :10.1093/schbul/sbr151. PMC 3576173 . PMID 22080493.
- ^ ab Fitzgerald, PB; Laird, AR; Maller, J; Daskalakis, ZJ (июнь 2008 г.). «Метааналитическое исследование изменений активации мозга при депрессии». Human Brain Mapping . 29 (6): 683–95. doi :10.1002/hbm.20426. PMC 2873772. PMID 17598168 .
- ^ Карлсон, Нил Р. (2012). Physiology of Behavior Books a La Carte Edition (11-е изд.). Бостон: Pearson College Div. ISBN 978-0-205-23981-8.
- ^ ab Miller, Chris H.; Hamilton, J. Paul; Sacchet, Matthew D.; Gotlib, Ian H. (1 октября 2015 г.). «Метаанализ функциональной нейровизуализации большого депрессивного расстройства у молодежи». JAMA Psychiatry . 72 (10): 1045–1053. doi : 10.1001/jamapsychiatry.2015.1376 . ISSN 2168-6238. PMID 26332700.
- ^ Wessa, Michèle; Lois, Giannis (30 ноября 2016 г.). «Функциональные эффекты психофармакологического лечения при тяжелой депрессии: фокус на нейронных цепях аффективной обработки». Current Neuropharmacology . 13 (4): 466–479. doi : 10.2174/1570159X13666150416224801. ISSN 1570-159X. PMC 4790403. PMID 26412066 .
- ^ Outhred, Tim; Hawkshead, Brittany E.; Wager, Tor D.; Das, Pritha; Malhi, Gin S.; Kemp, Andrew H. (1 сентября 2013 г.). «Острые нейронные эффекты селективных ингибиторов обратного захвата серотонина по сравнению с ингибиторами обратного захвата норадреналина на обработку эмоций: последствия для дифференциальной эффективности лечения» (PDF) . Neuroscience and Biobehavioral Reviews . 37 (8): 1786–1800. doi :10.1016/j.neubiorev.2013.07.010. ISSN 1873-7528. PMID 23886514. S2CID 15469440.
- ^ Гамильтон, Дж. Пол; Саймер, Маттиас; Готлиб, Ян Х. (8 сентября 2009 г.). «Объем миндалины при большом депрессивном расстройстве: метаанализ исследований магнитно-резонансной томографии». Молекулярная психиатрия . 13 (11): 993–1000. doi :10.1038/mp.2008.57. ISSN 1359-4184. PMC 2739676. PMID 18504424 .
- ^ Палмер, Сьюзан М.; Крютер, Шейла Г.; Кэри, Лианн М. (14 января 2015 г.). «Метаанализ изменений активности мозга при клинической депрессии». Frontiers in Human Neuroscience . 8 : 1045. doi : 10.3389/fnhum.2014.01045 . ISSN 1662-5161. PMC 4294131. PMID 25642179 .
- ^ Фицджеральд, Пол Б.; Лэрд, Анджела Р.; Маллер, Джером; Даскалакис, Зафирис Дж. (5 декабря 2016 г.). «Метааналитическое исследование изменений активации мозга при депрессии». Картирование человеческого мозга . 29 (6): 683–695. дои : 10.1002/hbm.20426. ISSN 1065-9471. ПМЦ 2873772 . ПМИД 17598168.
- ^ Коул, Джеймс; Костафреда, Серджи Г.; Макгаффин, Питер; Фу, Синтия HY (1 ноября 2011 г.). «Атрофия гиппокампа при первом эпизоде депрессии: метаанализ исследований магнитно-резонансной томографии». Журнал аффективных расстройств . 134 (1–3): 483–487. doi :10.1016/j.jad.2011.05.057. ISSN 1573-2517. PMID 21745692.
- ^ Видебек, Пол; Равнкильде, Барбара (1 ноября 2004 г.). «Объем гиппокампа и депрессия: метаанализ исследований МРТ». Американский журнал психиатрии . 161 (11): 1957–1966. doi :10.1176/appi.ajp.161.11.1957. ISSN 0002-953X. PMID 15514393.
- ^ Махар, И; Бамбико, Ф. Р.; Мехавар, Н.; Нобрега, Дж. Н. (январь 2014 г.). «Стресс, серотонин и нейрогенез гиппокампа в связи с депрессией и эффектами антидепрессантов». Neuroscience and Biobehavioral Reviews . 38 : 173–92. doi : 10.1016/j.neubiorev.2013.11.009. PMID 24300695. S2CID 207090692.
- ^ Willner, P; Scheel-Krüger, J; Belzung, C (декабрь 2013 г.). «Нейробиология депрессии и действие антидепрессантов». Neuroscience and Biobehavioral Reviews . 37 (10 Pt 1): 2331–71. doi :10.1016/j.neubiorev.2012.12.007. PMID 23261405. S2CID 46160087.
- ^ Pariante CM, Lightman SL (сентябрь 2008 г.). «Ось HPA при большой депрессии: классические теории и новые разработки». Trends Neurosci . 31 (9): 464–468. doi :10.1016/j.tins.2008.06.006. PMID 18675469. S2CID 13308611.
- ^ Бельведери Мурри, Мартино; Парианте, Кармине ; Монделли, Валерия; Масотти, Маттиа; Атти, Анна Рита; Меллаква, Зефиро; Антониоли, Марко; Гио, Лусио; Менчетти, Марко; Занетиду, Стаматула; Иннаморати, Марко; Аморе, Марио (1 марта 2014 г.). «Ось HPA и старение при депрессии: систематический обзор и метаанализ». Психонейроэндокринология . 41 : 46–62. doi :10.1016/j.psyneuen.2013.12.004. hdl : 11567/691367. ISSN 1873-3360. PMID 24495607. S2CID 24419374.
- ^ Juruena, Mario F. (1 сентября 2014 г.). «Стресс раннего возраста и ось HPA вызывают рецидивирующую депрессию во взрослом возрасте». Epilepsy & Behavior . 38 : 148–159. doi : 10.1016/j.yebeh.2013.10.020. ISSN 1525-5069. PMID 24269030. S2CID 24251067.
- ^ Хейм, Кристин; Ньюпорт, Д. Джеффри; Млетцко, Таня; Миллер, Эндрю Х.; Немерофф, Чарльз Б. (1 августа 2008 г.). «Связь между детской травмой и депрессией: выводы из исследований оси HPA у людей». Психонейроэндокринология . 33 (6): 693–710. doi :10.1016/j.psyneuen.2008.03.008. ISSN 0306-4530. PMID 18602762. S2CID 2629673.
- ^ Arana, GW; Baldessarini, RJ; Ornsteen, M. (1 декабря 1985 г.). «Тест подавления дексаметазоном для диагностики и прогнозирования в психиатрии. Комментарий и обзор». Архивы общей психиатрии . 42 (12): 1193–1204. doi :10.1001/archpsyc.1985.01790350067012. ISSN 0003-990X. PMID 3000317.
- ^ Varghese, Femina P.; Brown, E. Sherwood (1 января 2001 г.). «Гипоталамо-гипофизарно-надпочечниковая ось при большом депрессивном расстройстве: краткий учебник для врачей первичной медицинской помощи». Primary Care Companion to the Journal of Clinical Psychiatry . 3 (4): 151–155. doi :10.4088/pcc.v03n0401. ISSN 1523-5998. PMC 181180. PMID 15014598 .
- ^ Gilbertson, MW; Shenton, ME; Ciszewski, A.; Kasai, K.; Lasko, NB; Orr, SP; Pitman, RK (2002). «Меньший объем гиппокампа предсказывает патологическую уязвимость к психологической травме». Nature Neuroscience . 5 (11): 1242–7. doi :10.1038/nn958. PMC 2819093 . PMID 12379862.
- ^ Vythilingam, Meena; Vermetten, Eric; Anderson, George M.; Luckenbaugh, David; Anderson, Eric R.; Snow, Joseph; Staib, Lawrence H.; Charney, Dennis S.; Bremner, J. Douglas (15 июля 2004 г.). «Объем гиппокампа, память и статус кортизола при большом депрессивном расстройстве: эффекты лечения». Biological Psychiatry . 56 (2): 101–112. doi :10.1016/j.biopsych.2004.04.002. ISSN 0006-3223. PMID 15231442. S2CID 34280275.
- ^ abc Кришнан, В.; Нестлер, Э.Дж. (2011). Животные модели депрессии: молекулярные перспективы . Текущие темы в поведенческих нейронауках. Том 7. С. 121–47. doi :10.1007/7854_2010_108. ISBN 978-3-642-19702-4. PMC 3270071 . PMID 21225412.
- ^ Belzung, C; Lemoine, M (7 ноября 2011 г.). «Критерии валидности для животных моделей психических расстройств: фокус на тревожные расстройства и депрессию». Biology of Mood & Anxiety Disorders . 1 (1): 9. doi : 10.1186/2045-5380-1-9 . PMC 3384226 . PMID 22738250.
- ^ ab Alcantara, Lyonna F.; Praise, Eric M.; Bolanos-Guzman, Carlos A. (2018). "26. Животные модели расстройств настроения". В Charney, Dennis; Sklar, Pamela; Nestler, Eric; Buxbaum, Joseph (ред.). Charney & Nestler's Neurobiology of Mental Illness (5-е изд.). Нью-Йорк: Oxford University Press. стр. 329–333.
- ^ Yan, HC; Cao, X; Das, M; Zhu, XH; Gao, TM (август 2010 г.). «Поведенческие модели депрессии у животных». Neuroscience Bulletin . 26 (4): 327–37. doi :10.1007/s12264-010-0323-7. PMC 5552573. PMID 20651815 .
- ^ Czéh, B; Fuchs, E; Wiborg, O; Simon, M (4 января 2016 г.). «Животные модели большой депрессии и их клинические последствия». Progress in Neuro-psychopharmacology & Biological Psychiatry . 64 : 293–310. doi :10.1016/j.pnpbp.2015.04.004. PMID 25891248. S2CID 207410936.
- ^ abc Yang, Y; Wang, H; Hu, J; Hu, H (февраль 2018 г.). «Латеральная габенула в патофизиологии депрессии». Current Opinion in Neurobiology . 48 : 90–96. doi : 10.1016/j.conb.2017.10.024 . PMID 29175713.
- ^ Proulx, CD; Hikosaka, O; Malinow, R (сентябрь 2014 г.). «Обработка вознаграждения латеральной габенулой при нормальном и депрессивном поведении». Nature Neuroscience . 17 (9): 1146–52. doi :10.1038/nn.3779. PMC 4305435 . PMID 25157511.
- ^ Belujon, P; Grace, AA (1 декабря 2017 г.). «Нарушение регуляции дофаминовой системы при серьезных депрессивных расстройствах». Международный журнал нейропсихофармакологии . 20 (12): 1036–1046. doi :10.1093/ijnp/pyx056. PMC 5716179. PMID 29106542 .
- ^ ab Knowland, D; Lim, BK (5 января 2018 г.). «Основанные на контурах структуры депрессивного поведения: роль контуров вознаграждения и не только». Pharmacology Biochemistry and Behavior . 174 : 42–52. doi : 10.1016/j.pbb.2017.12.010. PMC 6340396. PMID 29309799 .
- ^ Хеллер, А.С. (2016). «Корково-подкорковые взаимодействия при депрессии : от моделей животных до психопатологии человека». Frontiers in Systems Neuroscience . 10 : 20. doi : 10.3389/fnsys.2016.00020 . PMC 4780432. PMID 27013988.
- ^ Кристофер Питтенгер; Рональд С. Думан (2008). «Стресс, депрессия и нейропластичность: конвергенция механизмов». Нейропсихофармакология . 33 (1): 88–109. doi : 10.1038/sj.npp.1301574 . PMID 17851537.
- ^ Брунони, Андре Руссовски; Лопес, Мариана; Фрегни, Фелипе (1 декабря 2008 г.). «Систематический обзор и метаанализ клинических исследований большой депрессии и уровней BDNF: последствия для роли нейропластичности при депрессии». Международный журнал нейропсихофармакологии . 11 (8): 1169–1180. doi : 10.1017/S1461145708009309 . ISSN 1461-1457. PMID 18752720.
- ^ Серафини, Джанлука (22 июня 2012 г.). «Нейропластичность и большая депрессия, роль современных антидепрессантов». World Journal of Psychiatry . 2 (3): 49–57. doi : 10.5498/wjp.v2.i3.49 . ISSN 2220-3206. PMC 3782176. PMID 24175168 .
- ^ Кришнадас, Раджив; Каванаг, Джонатан (1 мая 2012 г.). «Депрессия: воспалительное заболевание?». Журнал неврологии, нейрохирургии и психиатрии . 83 (5): 495–502. doi : 10.1136/jnnp-2011-301779 . ISSN 1468-330X. PMID 22423117.
- ^ Патель, Амиша (1 сентября 2013 г.). «Обзор: роль воспаления при депрессии». Psychiatria Danubina . 25 (Suppl 2): S216–223. ISSN 0353-5053. PMID 23995180.
- ^ Dowlati, Yekta; Herrmann, Nathan; Swardfager, Walter; Liu, Helena; Sham, Lauren; Reim, Elyse K.; Lanctôt, Krista L. (1 марта 2010 г.). «Метаанализ цитокинов при большой депрессии». Biological Psychiatry . 67 (5): 446–457. doi :10.1016/j.biopsych.2009.09.033. ISSN 1873-2402. PMID 20015486. S2CID 230209.
- ^ Данцер, Роберт; О'Коннор, Джейсон С.; Фройнд, Грегори Г.; Джонсон, Родни В.; Келли, Кит В. (3 декабря 2016 г.). «От воспаления к болезни и депрессии: когда иммунная система подчиняет себе мозг». Nature Reviews Neuroscience . 9 (1): 46–56. doi :10.1038/nrn2297. ISSN 1471-003X. PMC 2919277. PMID 18073775 .
- ^ Хайлз, Сара А.; Бейкер, Аманда Л.; де Мальманш, Тео; Аттиа, Джон (1 октября 2012 г.). «Метаанализ различий в ИЛ-6 и ИЛ-10 между людьми с депрессией и без нее: изучение причин гетерогенности». Мозг, поведение и иммунитет . 26 (7): 1180–1188. doi : 10.1016/j.bbi.2012.06.001. hdl : 1959.13/1040816 . ISSN 1090-2139. PMID 22687336. S2CID 205862714.
- ^ Howren, M. Bryant; Lamkin, Donald M.; Suls, Jerry (1 февраля 2009 г.). «Связь депрессии с С-реактивным белком, IL-1 и IL-6: метаанализ». Психосоматическая медицина . 71 (2): 171–186. doi :10.1097/PSY.0b013e3181907c1b. ISSN 1534-7796. PMID 19188531. S2CID 10130027.
- ^ Maes, Michael (29 апреля 2011 г.). «Депрессия — это воспалительное заболевание, но активация клеточного иммунитета является ключевым компонентом депрессии». Progress in Neuro-Psychopharmacology & Biological Psychiatry . 35 (3): 664–675. doi :10.1016/j.pnpbp.2010.06.014. ISSN 1878-4216. PMID 20599581. S2CID 11653910.
- ^ Берк, Майкл; Уильямс, Лана Дж; Джека, Фелис Н ; О'Нил, Адриенна; Паско, Джули А; Мойлан, Стивен; Аллен, Николас Б; Стюарт, Аманда Л; Хейли, Эми С; Бирн, Мишель Л; Мэйс, Майкл (12 сентября 2013 г.). «Итак, депрессия — это воспалительное заболевание, но откуда берется воспаление?». BMC Medicine . 11 : 200. doi : 10.1186/1741-7015-11-200 . ISSN 1741-7015. PMC 3846682. PMID 24228900 .
- ^ Леонард, Брайан; Мэйс, Майкл (1 февраля 2012 г.). «Механистические объяснения того, как клеточно-опосредованная иммунная активация, воспаление и пути окислительного и нитрозативного стресса и их последствия и сопутствующие факторы играют роль в патофизиологии униполярной депрессии». Neuroscience and Biobehavioral Reviews . 36 (2): 764–785. doi :10.1016/j.neubiorev.2011.12.005. ISSN 1873-7528. PMID 22197082. S2CID 37761511.
- ^ Рэдлер, Томас Дж. (1 ноября 2011 г.). «Воспалительные механизмы при большом депрессивном расстройстве». Current Opinion in Psychiatry . 24 (6): 519–525. doi :10.1097/YCO.0b013e32834b9db6. ISSN 1473-6578. PMID 21897249. S2CID 24215407.
- ^ Кёлер, Оле; Бенрос, Майкл Э.; Нордентофт, Мерете; Фаркух, Майкл Э.; Айенгар, Рупа Л.; Морс, Оле; Крог, Йеспер (1 декабря 2014 г.). «Влияние противовоспалительного лечения на депрессию, депрессивные симптомы и побочные эффекты: систематический обзор и метаанализ рандомизированных клинических испытаний». JAMA Psychiatry . 71 (12): 1381–1391. doi : 10.1001/jamapsychiatry.2014.1611 . ISSN 2168-6238. PMID 25322082.
- ^ Медина, Джонна Л.; Жакар, Джолин; Смитс, Джаспер А. Дж. (2015). «Оптимизация назначения упражнений при депрессии: поиск биомаркеров ответа». Current Opinion in Psychology . 4 : 43–47. doi : 10.1016/j.copsyc.2015.02.003. ISSN 2352-250X. PMC 4545504. PMID 26309904 .
- ^ Parker GB, Brotchie H, Graham RK (январь 2017 г.). «Витамин D и депрессия». J Affect Disord . 208 : 56–61. doi :10.1016/j.jad.2016.08.082. PMID 27750060.
- ^ Cenik B, Cenik C, Snyder MP, Brown ES (2017). «Плазменные стерины и тяжесть симптомов депрессии в популяционной когорте». PLOS ONE . 12 (9): e0184382. Bibcode : 2017PLoSO..1284382C. doi : 10.1371/journal.pone.0184382 . PMC 5590924. PMID 28886149 .
- ^ Блэк, Кэтрин Н.; Бот, Мариска; Шеффер, Питер Г.; Кёйперс, Пим; Пеннинкс, Бренда У. Дж. Х. (1 января 2015 г.). «Связана ли депрессия с повышенным окислительным стрессом? Систематический обзор и метаанализ». Психонейроэндокринология . 51 : 164–175. doi : 10.1016/j.psyneuen.2014.09.025 . ISSN 1873-3360. PMID 25462890. S2CID 6896118.
- ^ Лю, Тао; Чжун, Шумин; Ляо, Сяосяо; Чэнь, Цзянь; Хэ, Тинтин; Лай, Шункай; Цзя, Яньбинь (1 января 2015 г.). «Метаанализ маркеров окислительного стресса при депрессии». PLOS ONE . 10 (10): e0138904. Bibcode : 2015PLoSO..1038904L. doi : 10.1371/journal.pone.0138904 . ISSN 1932-6203. PMC 4596519. PMID 26445247 .
- ^ Raza MU, Tufan T, Wang Y, Hill C, Zhu MY (август 2016 г.). «Повреждение ДНК при основных психиатрических заболеваниях». Neurotox Res . 30 (2): 251–67. doi :10.1007/s12640-016-9621-9. PMC 4947450. PMID 27126805 .
- ^ Лю, Тао; Чжун, Шуминг; Ляо, Сяосяо; Чен, Цзянь; Он, Тингтинг; Лай, Шункай; Цзя, Янбинь (7 октября 2015 г.). «Метаанализ маркеров окислительного стресса при депрессии». ПЛОС ОДИН . 10 (10): e0138904. Бибкод : 2015PLoSO..1038904L. дои : 10.1371/journal.pone.0138904 . ISSN 1932-6203. ПМЦ 4596519 . ПМИД 26445247.
- ^ M, Morris G и Berk (2015). «Множество путей к митохондриальной дисфункции при нейроиммунных и нейропсихиатрических расстройствах». BMC Medicine . 13 : 68. doi : 10.1186/s12916-015-0310-y . PMC 4382850. PMID 25889215 .
- ^ Аллен, Джош; Ромей-Таллон, Ракель; Браймер, Кайл Дж.; Карунчо, Гектор Дж.; Калинчук, Лиза Э. (6 июня 2018 г.). «Митохондрии и настроение: митохондриальная дисфункция как ключевой игрок в проявлении депрессии». Frontiers in Neuroscience . 12 : 386. doi : 10.3389/fnins.2018.00386 . ISSN 1662-453X. PMC 5997778. PMID 29928190 .
- ^ abcde Менон, Винод (октябрь 2011 г.). «Крупномасштабные мозговые сети и психопатология: объединяющая модель тройной сети». Тенденции в когнитивных науках . 15 (10): 483–506. doi :10.1016/j.tics.2011.08.003. PMID 21908230. S2CID 26653572.
- ^ ab Seeley, WW; et al. (февраль 2007 г.). «Диссоциативные внутренние сети связей для обработки значимости и исполнительного контроля». Журнал нейронауки . 27 (9): 2349–56. doi :10.1523/JNEUROSCI.5587-06.2007. PMC 2680293. PMID 17329432 .
- ^ Хабас, К. и др. (1 июля 2009 г.). «Отдельные вклады мозжечка в внутренние сети связей». Журнал нейронауки . 29 (26): 8586–94. doi :10.1523/JNEUROSCI.1868-09.2009. PMC 2742620. PMID 19571149 .
- ^ Петридес, М. (2005). «Латеральная префронтальная кора: архитектура и функциональная организация». Philosophical Transactions of the Royal Society B. 360 ( 1456): 781–795. doi :10.1098/rstb.2005.1631. PMC 1569489. PMID 15937012 .
- ^ Вудворд, НД; и др. (2011). «Функциональные сети состояния покоя по-разному повреждаются при шизофрении». Исследования шизофрении . 130 (1–3): 86–93. doi :10.1016/j.schres.2011.03.010. PMC 3139756. PMID 21458238 .
- ^ Менон, Винод и др. (2001). «Функциональная нейроанатомия слуховой рабочей памяти при шизофрении: связь с позитивными и негативными симптомами». NeuroImage . 13 (3): 433–446. doi :10.1006/nimg.2000.0699. PMID 11170809. S2CID 12757905.
- ^ Левин, Р. Л.; и др. (2007). «Когнитивные дефициты при депрессии и функциональная специфика региональной активности мозга». Когнитивная терапия и исследования . 31 (2): 211–233. doi :10.1007/s10608-007-9128-z. S2CID 22374128.
- ^ Цинь, П.; Нортхофф, Г. (2011). «Как наше «я» связано с регионами средней линии и сетью режима по умолчанию?». NeuroImage . 57 (3): 1221–1233. doi :10.1016/j.neuroimage.2011.05.028. PMID 21609772. S2CID 16242246.
- ^ Raichle, ME; et al. (2001). "Режим работы мозга по умолчанию". Труды Национальной академии наук Соединенных Штатов Америки . 98 (2): 676–682. Bibcode :2001PNAS...98..676R. doi : 10.1073/pnas.98.2.676 . PMC 14647 . PMID 11209064.
- ^ Куни, Р. Э.; и др. (2010). «Нейронные корреляты размышлений при депрессии». Когнитивная, аффективная и поведенческая нейронаука . 10 (4): 470–478. doi :10.3758/cabn.10.4.470. PMC 4476645. PMID 21098808 .
- ^ Бройд, С. Дж. и др. (2009). «Дисфункция мозга в режиме ожидания при психических расстройствах: систематический обзор». Neuroscience & Biobehavioral Reviews . 33 (3): 279–296. doi :10.1016/j.neubiorev.2008.09.002. PMID 18824195. S2CID 7175805.
- ^ Хамани, К; и др. (15 февраля 2011 г.). «Подмозолистая поясная извилина в контексте большой депрессии». Биологическая психиатрия . 69 (4): 301–8. doi : 10.1016/j.biopsych.2010.09.034 . PMID 21145043. S2CID 35458273.
- ^ Feinstein, JS; et al. (сентябрь 2006 г.). «Реактивность передней островковой доли во время принятия определенных решений связана с невротизмом». Social Cognitive and Affective Neuroscience . 1 (2): 136–142. doi :10.1093/scan/nsl016. PMC 2555442 . PMID 18985124.
- ^ Паулюс, MP; Стайн, MB (2006). «Островной взгляд на тревогу». Биологическая психиатрия . 60 (4): 383–387. doi :10.1016/j.biopsych.2006.03.042. PMID 16780813. S2CID 17889111.
- ^ Энтони, ММ (2009). Оксфордский справочник по тревожности и связанным с ней расстройствам . Oxford University Press.
Дальнейшее чтение
- Науменко, ВС; Попова, НК; Лацивита, Э; Леопольдо, М; Понимаскин, ЭГ (июль 2014 г.). «Взаимодействие между рецепторами серотонина 5-HT1A и 5-HT7 при депрессивных расстройствах». CNS Neuroscience & Therapeutics . 20 (7). Wiley-Blackwell : 582–90. doi : 10.1111/cns.12247 . ISSN 1755-5949. PMC 6493079. PMID 24935787. S2CID 13089087 .
- Silić, A; Vukojević, J; Peitl, V; De Hert, M; Karlović, D (январь 2022 г.). Wegener, G (ред.). «Большое депрессивное расстройство: возможная типизация в соответствии с серотонином, воспалением и метаболическим синдромом» (PDF) . Acta Neuropsychiatrica . 34 (1). Кембридж и Нью-Йорк : Cambridge University Press от имени Скандинавского колледжа нейропсихофармакологии : 15–23. doi : 10.1017/neu.2021.30 . ISSN 1601-5215. PMID 34503595. S2CID 237469505 . Получено 10 марта 2022 г. .
- Szafran, K; Faron-Górecka, A; Kolasa, M; Kuśmider, M; Solich, J; Zurawek, D; Dziedzicka-Wasylewska, M (ноябрь–декабрь 2013 г.). «Потенциальная роль гетеродимеризации рецепторов, сопряженных с G-белком (GPCR), при нейропсихиатрических расстройствах: фокус на депрессию» (PDF) . Pharmacological Reports . 65 (6). Elsevier от имени Института фармакологии Польской академии наук : 1498–505. doi :10.1016/s1734-1140(13)71510-x. ISSN 1734-1140. PMID 24552997. S2CID 4726214 . Получено 10 марта 2022 г.
