Арсенид кадмия
 Кристаллы Cd 3 As 2 с ориентациями (112) и (400) [1] | |
 Изображение STM поверхности (112) [1] | |
| Имена | |
|---|---|
| Другие имена Трикадмий диарсенид | |
| Идентификаторы | |
| |
3D модель ( JSmol ) |
|
| ChemSpider |
|
| Информационная карта ECHA | 100.031.336 |
| Номер ЕС |
|
CID PubChem |
|
Панель инструментов CompTox ( EPA ) |
|
| |
| |
| Характеристики | |
| Кд 3 Ас 2 | |
| Молярная масса | 487,08 г/моль |
| Появление | сплошной, темно-серый |
| Плотность | 3.031 |
| Температура плавления | 716 °C (1321 °F; 989 K) |
| разлагается в воде | |
| Структура [2] | |
| Тетрагональный, tI208 | |
| И4 1 /акд, № 142-2 | |
а = 1,26512(3) нм, с = 2,54435(4) нм | |
| Опасности | |
| Маркировка СГС : | |
    | |
| Опасность | |
| Н301 , Н312 , Н330 , Н350 , Н410 | |
| Р201 , Р202 , Р260 , Р261 , Р264 , Р270 , Р271 , Р273 , Р280 , Р281 , Р284 , Р301+Р310 , Р302+Р352 , Р304+Р340 , Р308+Р313 , Р310 , Р311 , Р312 , Р320 , Р321 , Р322 , Р330 , Р363 , Р391 , Р403+Р233 , Р405 , Р501 | |
| NFPA 704 (огненный алмаз) | |
| Летальная доза или концентрация (ЛД, ЛК): | |
LD 50 ( средняя доза ) | нет данных |
| NIOSH (пределы воздействия на здоровье в США): | |
PEL (допустимый) | [1910.1027] TWA 0,005 мг/м 3 (как Cd) [3] |
РЕЛ (рекомендуется) | Ка [3] |
IDLH (Непосредственная опасность) | Ca [9 мг/м 3 (как Cd)] [3] |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |
Арсенид кадмия ( Cd 3 As 2 ) — неорганический полуметалл семейства II-V . Проявляет эффект Нернста .
Характеристики
Термальный
Cd 3 As 2 диссоциирует между 220 и 280 °C согласно реакции [4]
- 2 Cd 3 As 2 (т) → 6 Cd(г) + As 4 (г)
Обнаружен энергетический барьер для нестехиометрического испарения мышьяка из-за нерегулярности парциальных давлений с температурой. Диапазон энергетической щели составляет от 0,5 до 0,6 эВ. Cd 3 As 2 плавится при 716 °C и меняет фазу при 615 °C/ [5]
Фазовый переход
Чистый арсенид кадмия претерпевает несколько фазовых переходов при высоких температурах, образуя фазы, обозначенные как α (стабильная), α', α” (метастабильная) и β. [6] При 593° происходит полиморфный переход α → β.
- α-Cd 3 As 2 ↔ α'-Cd 3 As 2 происходит при ~500 К.
- α'-Cd 3 As 2 ↔ α''-Cd 3 As 2 происходит при температуре ~742 К и представляет собой обычный фазовый переход первого рода с выраженной петлей гистерезиса.
- α”-Cd 3 As 2 ↔ β-Cd 3 As 2 происходит при 868 К.
Для определения параметров решетки Cd 3 As 2 между 23 и 700 °C использовалась рентгеновская дифракция монокристалла . Переход α → α′ происходит медленно и поэтому, скорее всего, является промежуточной фазой. Переход α′ → α″ происходит намного быстрее, чем α → α′, и имеет очень малый термический гистерезис . Этот переход приводит к изменению оси четвертого порядка тетрагональной ячейки, вызывая двойникование кристалла . Ширина петли не зависит от скорости нагрева, хотя она становится уже после нескольких температурных циклов. [7]
Электронный
Соединение арсенида кадмия имеет более низкое давление паров (0,8 атм), чем кадмий и мышьяк по отдельности. Арсенид кадмия не разлагается при испарении и повторной конденсации. Концентрация носителей в Cd 3 As 2 обычно составляет (1–4)×10 18 электронов/см 3 . Несмотря на высокую концентрацию носителей, подвижность электронов также очень высока (до 10 000 см 2 /(В·с) при комнатной температуре). [8]
В 2014 году было показано, что Cd 3 As 2 является полуметаллическим материалом, аналогичным графену , который существует в трехмерной форме, которую должно быть намного легче формировать в электронные устройства. [9] [10] Трехмерные (3D) топологические полуметаллы Дирака (TDS) являются объемными аналогами графена , которые также демонстрируют нетривиальную топологию в своей электронной структуре, которая имеет сходство с топологическими изоляторами. Более того, TDS потенциально может быть переведен в другие экзотические фазы (такие как полуметаллы Вейля, аксионные изоляторы и топологические сверхпроводники ), фотоэмиссионная спектроскопия с угловым разрешением выявила пару трехмерных фермионов Дирака в Cd 3 As 2 . По сравнению с другими трехмерными TDS, например, β-кристобалитом BiO
2и Na3Bi , Cd 3 As 2 стабилен и имеет гораздо более высокие скорости Ферми. Легирование in situ использовалось для настройки его энергии Ферми. [10]
Проведение
Арсенид кадмия является полупроводником II-V, демонстрирующим вырожденную собственную проводимость полупроводника n-типа с большой подвижностью, малой эффективной массой и сильно непараболической зоной проводимости, или узкозонным полупроводником . Он демонстрирует инвертированную зонную структуру, а оптическая энергетическая щель, например , меньше 0. При осаждении методом термического испарения (осаждения) арсенид кадмия проявлял эффект Шоттки ( термоэлектронная эмиссия ) и эффект Пула-Френкеля в сильных электрических полях. [11]
Магнитосопротивление
Арсенид кадмия демонстрирует очень сильные квантовые колебания сопротивления даже при относительно высокой температуре 100 К. [12] Это делает его полезным для тестирования криомагнитных систем, поскольку наличие такого сильного сигнала является четким индикатором функционирования.
Подготовка
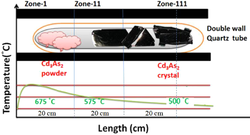
Арсенид кадмия может быть получен в виде аморфного полупроводникового стекла . Согласно Хискоксу и Эллиоту, [5] приготовление арсенида кадмия было произведено из металлического кадмия, который имел чистоту 6 N от Kock-Light Laboratories Limited. Хобокен поставлял β-мышьяк с чистотой 99,999%. Стехиометрические пропорции элементов кадмия и мышьяка нагревались вместе. Разделение было трудным и длительным из-за того, что слитки прилипали к кремнезему и ломались. Был создан рост Стокбаргера в жидкой капсуле. Кристаллы вытягиваются из летучих расплавов в жидкой капсуле. Расплав покрывается слоем инертной жидкости, обычно B 2 O 3 , и применяется давление инертного газа, превышающее равновесное давление паров. Это исключает испарение из расплава, что позволяет затравке и вытягиванию происходить через слой B 2 O 3 .
Кристаллическая структура
Элементарная ячейка Cd 3 As 2 является тетрагональной. [2] [13] Ионы мышьяка кубически плотно упакованы , а ионы кадмия координированы тетраэдрически. Вакантные тетраэдрические позиции спровоцировали исследования фон Штакельберга и Паулюса (1935), которые определили первичную структуру. Каждый ион мышьяка окружен ионами кадмия в шести из восьми углов искаженного куба, а два вакантных места находились на диагоналях. [2]
Кристаллическая структура арсенида кадмия очень похожа на структуру фосфида цинка (Zn 3 P 2 ) , арсенида цинка (Zn 3 As 2 ) и фосфида кадмия (Cd 3 P 2 ) . Эти соединения четверной системы Zn-Cd-P-As демонстрируют полный непрерывный твердый раствор. [14]
эффект Нернста
Арсенид кадмия используется в инфракрасных детекторах, использующих эффект Нернста, и в тонкопленочных динамических датчиках давления . Он также может быть использован для изготовления магниторезисторов , и в фотодетекторах . [15]
Арсенид кадмия может использоваться в качестве легирующей примеси для HgCdTe .
Ссылки
- ^ abc Sankar, R.; Neupane, M.; Xu, S.-Y.; Butler, CJ; Zeljkovic, I.; Panneer Muthuselvam, I.; Huang, F.-T.; Guo, S.-T.; Karna, Sunil K.; Chu, M.-W.; Lee, WL; Lin, M.-T.; Jayavel, R.; Madhavan, V.; Hasan, MZ; Chou, FC (2015). "Большой рост монокристаллов, транспортные свойства и спектроскопические характеристики трехмерного дираковского полуметалла Cd3As2". Scientific Reports . 5 : 12966. Bibcode :2015NatSR...512966S. doi :10.1038/srep12966. PMC 4642520 . PMID 26272041.
- ^ abc Ali, MN; Gibson, Q.; Jeon, S.; Zhou, BB; Yazdani, A.; Cava, RJ (2014). «Кристаллические и электронные структуры Cd3As2 , трехмерного электронного аналога графена». Неорганическая химия . 53 (8): 4062– 4067. arXiv : 1312.7576 . doi : 10.1021/ic403163d. PMID 24679042.
- ^ abc NIOSH Карманный справочник по химическим опасностям. "#0087". Национальный институт охраны труда и здоровья (NIOSH).
- ^ Westmore, JB; Mann, KH; Tickner, AW (1964). "Масс-спектрометрическое исследование нестехиометрического испарения арсенида кадмия 1 ". Журнал физической химии . 68 (3): 606– 612. doi :10.1021/j100785a028.
- ^ ab Hiscocks, SER; Elliott, CT (1969). "О получении, росте и свойствах Cd 3 As 2 ". Журнал материаловедения . 4 (9): 784– 788. Bibcode :1969JMatS...4..784H. doi :10.1007/BF00551073. S2CID 136483003.
- ^ Пьетрашко, А.; Лукашевич, К. (1969). «Уточнение кристаллической структуры α»-Cd 3 As 2 ». Acta Crystallographica Section B . 25 (5): 988– 990. doi :10.1107/S0567740869003323.
- ^ Пьетрашко, А.; Лукашевич, К. (1973). «Тепловое расширение и фазовые переходы Cd 3 As 2 и Zn 3 As 2 ». Physica Status Solidi A . 18 (2): 723– 730. Bibcode :1973PSSAR..18..723P. doi :10.1002/pssa.2210180234.
- ^ Довгялло-Пленкевич, Б.; Пленкевич, П. (1979). «Инвертированная зонная структура Cd 3 As 2 ». Физический статус Solidi B. 94 (1): К57 – К60 . Бибкод :1979ПССБР..94...57Д. дои : 10.1002/pssb.2220940153.
- ^ Neupane, M.; Xu, SY; Sankar, R.; Alidoust, N.; Bian, G.; Liu, C.; Belopolski, I.; Chang, TR; Jeng, HT; Lin, H.; Bansil, A.; Chou, F.; Hasan, MZ (2014). "Наблюдение трехмерной топологической дираковской полуметаллической фазы в высокоподвижном Cd 3 As 2 ". Nature Communications . 5 : 3786. arXiv : 1309.7892 . Bibcode : 2014NatCo...5.3786N. doi : 10.1038/ncomms4786. PMID 24807399.
- ^ ab Liu, ZK; Jiang, J.; Zhou, B.; Wang, ZJ; Zhang, Y.; Weng, HM; Prabhakaran, D.; Mo, SK; Peng, H.; Dudin, P.; Kim, T.; Hoesch, M.; Fang, Z.; Dai, X.; Shen, ZX; Feng, DL; Hussain, Z.; Chen, YL (2014). "Стабильный трехмерный топологический дираковский полуметалл Cd 3 As 2 ". Nature Materials . 13 (7): 677– 81. Bibcode :2014NatMa..13..677L. doi :10.1038/nmat3990. PMID 24859642.
- ^ Дин, М.; Гулд, РД (2006). "Измерения сопротивления Ван дер Пау на испаренных тонких пленках арсенида кадмия, Cd 3 As 2 ". Applied Surface Science . 252 (15): 5508– 5511. Bibcode :2006ApSS..252.5508D. doi :10.1016/j.apsusc.2005.12.151.
- ^ Narayanan, A.; Watson, MD; Blake, SF; Bruyant, N.; Drigo, L.; Chen, YL; Prabhakaran, D.; Yan, B.; Felser, C.; Kong, T.; Canfield, PC; Coldea, AI (19 марта 2015 г.). "Линейное магнитосопротивление, вызванное флуктуациями подвижности в -легированных соединениях". Physical Review Letters . 114 (11): 117201. arXiv : 1412.4105 . doi :10.1103/PhysRevLett.114.117201. PMID 25839304. S2CID 35607875.
- ^ Ким, Х.; Гойал, М.; Салмани-Резайе, С.; Шуманн, Т.; Пардью, ТН; Цзо, Дж. М.; Стеммер, С. (2019). «Симметрия точечной группы тонких пленок арсенида кадмия, определенная методом электронной дифракции сходящегося пучка». Physical Review Materials . 3 : 084202. arXiv : 1908.05734 . doi : 10.1103/PhysRevMaterials.3.084202 .
- ^ Трухан, ВМ; Изотов, АД; Шукавая, ТВ (2014). «Соединения и твердые растворы системы Zn-Cd-P-As в полупроводниковой электронике». Неорганические материалы . 50 (9): 868– 873. doi :10.1134/S0020168514090143. S2CID 94409384.
- ^ Дин, МБ; Гулд, РД (1998). "Механизм проводимости высокого поля тонких пленок испаренного арсенида кадмия". ICSE'98. Международная конференция IEEE по полупроводниковой электронике 1998 года. Труды (Кат. № 98EX187) . стр. 168. doi :10.1109/SMELEC.1998.781173. ISBN 0-7803-4971-7. S2CID 110904915.
Внешние ссылки
- Национальный реестр загрязняющих веществ – Кадмий и его соединения

