Бластицидин S
 | |
| Имена | |
|---|---|
| Предпочтительное название ИЮПАК (2 S ,3 S ,6 R )-3-{(3 S )-3-амино-5-[карбамимидоил(метил)амино]пентанамидо}-6-(4-амино-2-оксопиримидин-1(2 H )-ил)-3,6-дигидро-2 H- пиран-2-карбоновая кислота | |
| Идентификаторы | |
3D модель ( JSmol ) |
|
| ЧЭБИ | |
| ChEMBL | |
| ChemSpider | |
| Информационная карта ECHA | 100.109.057 |
| КЕГГ | |
CID PubChem |
|
| УНИИ | |
Панель инструментов CompTox ( EPA ) |
|
| |
| |
| Характеристики | |
| С17Н26Н8О5 | |
| Молярная масса | 422,44 г/моль |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |
Бластицидин S — это антибиотик , который используется в биологических исследованиях для отбора клеток в клеточной культуре . Интересующие клетки могут экспрессировать гены устойчивости к бластицидину BSD или bsr, а затем могут выдерживать лечение антибиотиком. Бластицидин S — это антибиотик -аналог нуклеозида , напоминающий нуклеозид цитидин . Бластицидин действует против человеческих клеток, грибков и бактерий, нарушая трансляцию белка . Первоначально он был описан японскими исследователями в 1950-х годах, которые искали антибиотики для грибка, вызывающего пирикуляриоз риса .
Химия
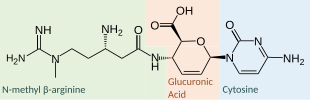
Аналог нуклеозида, бластицидин S, напоминает нуклеозид цитидин . Химическая структура состоит из молекулы цитозина , связанной с кольцом, полученным из глюкуроновой кислоты , которое в свою очередь связано с пептидом N-метил β-аргинином. [1]
Использует
Бластицидин S широко используется в клеточной культуре для отбора и поддержания генетически модифицированных клеток. Клетки, представляющие интерес, экспрессируют гены устойчивости к бластицидину S BSD или bsr, и затем могут выживать при добавлении бластицидина S в культуральную среду . [2] Бластицидин S обычно используется в концентрации 2–300 микрограмм на миллилитр среды в зависимости от типа выращиваемых клеток. [2]
Механизм действия
Бластицидин предотвращает рост как эукариотических , так и прокариотических клеток. Он работает , ингибируя стадию терминации трансляции и образование пептидной связи (в меньшей степени) рибосомой . Это означает, что клетки больше не могут производить новые белки посредством трансляции мРНК . Он конкурирует с пуромицином, предполагая очень похожий сайт связывания. [3]
Биосинтез
Первым шагом в биосинтезе бластицидина S является соединение UDP-глюкуроновой кислоты с цитозином для образования цитозилглюкуроновой кислоты (CGA). Учитывая название продукта, фермент, который осуществляет это соединение, называется CGA-синтазой. [1]
Эксперименты по клонированию космид из производителя бластицидина S Streptomyces griseochromogenes , за которыми последовала оценка предполагаемого кластера генов биосинтеза посредством гетерологичной реконструкции продукции бластицидина S в Streptomyces lividans , показали, что кластер генов размером 20 кбн с 19 генами, а также, возможно, пептидаза вне кластера генов, которая действует на конечный промежуточный продукт лейцилбластицидин S (LBS), были достаточны для реконструкции биосинтеза бластицидина S. [3]
Гены резистентности
Устойчивость к бластицидину S может быть обусловлена одной из двух дезаминаз : BSD, первоначально выделенной из Aspergillus terreus , или bsr, выделенной из Bacillus cereus . Обе дезаминазы работают, напрямую модифицируя бластицидин S, заменяя амин в цитозиновом кольце гидроксильной группой, что приводит к неактивному дезаминогидроксибластицину S. [2] [4]
Наиболее часто используемые гены устойчивости — bsr и BSD. Белки, вырабатываемые этими генами, позволяют клеткам, несущим их, вырабатывать белки в присутствии бластицидина.
История
В 1950-х годах в Японии была разработана программа скрининга лекарственных препаратов с целью обнаружения нового антибиотика, который предотвращал бы пирикуляриоз, вызываемый грибком Magnaporthe grisea . [5]
Ссылки
- ^ ab Niu G, Tan H (февраль 2015 г.). «Нуклеозидные антибиотики: биосинтез, регулирование и биотехнология». Trends Microbiol . 23 (2): 110– 9. doi :10.1016/j.tim.2014.10.007. PMID 25468791.
- ^ abc "Протоколы бластицидина S HCl". ThermoFisher Scientific . Получено 22 апреля 2021 г.
- ^ ab Cone, Martha C.; Yin, Xihou; Grochowski, Laura L.; Parker, Morgan R.; Zabriskie, T. Mark (2003-09-04). "Кластер генов биосинтеза бластицидина S из Streptomyces griseochromogenes: анализ последовательности, организация и начальная характеристика". ChemBioChem . 4 (9). Wiley: 821– 828. doi :10.1002/cbic.200300583. ISSN 1439-4227. PMID 12964155. S2CID 20991778.
- ^ Кимура М., Ямамото М., Фуруичи М., Кумасака Т., Ямагучи И. (2002). «Неожиданный подарок от исследований метаболизма фунгицидов: бластицидин S-деаминаза (BSD) из Aspergillus terreus ». Прогресс в биотехнологии . 22 : 55– 60. doi : 10.1016/S0921-0423(02)80043-0. ISBN 9780444507396.
- ^ Изоляция натуральных продуктов: методы разделения противомикробных препаратов, противовирусных препаратов и ингибиторов ферментов. Wagman GH, Elsevier RC; стр. 191 (1988).
Внешние ссылки
- Таксономия Streptomyces griseochromogenes


