Птичий грипп
| Грипп (грипп) |
|---|
 |
Птичий грипп , также известный как птичий грипп , — это заболевание, вызываемое вирусом гриппа А , которое в первую очередь поражает птиц, но иногда может поражать млекопитающих, включая людей. [1] Дикие водоплавающие птицы являются основными хозяевами вируса гриппа А, который является энзоотическим (постоянно присутствующим) во многих популяциях птиц. [2] [3]
Симптомы птичьего гриппа различаются в зависимости как от штамма вируса, лежащего в основе инфекции, так и от вида пораженной птицы или млекопитающего. Классификация штамма вируса как низкопатогенного птичьего гриппа (LPAI) или высокопатогенного птичьего гриппа (HPAI) основана на тяжести симптомов у домашних кур и не предсказывает тяжесть симптомов у других видов. [4] Куры, инфицированные LPAI, проявляют легкие симптомы или бессимптомны , тогда как HPAI вызывает серьезные затруднения дыхания, значительное снижение яйценоскости и внезапную смерть. [5] Домашняя птица может быть потенциально защищена от определенных штаммов вируса путем вакцинации. [6]
Люди и другие млекопитающие могут заразиться птичьим гриппом только после длительного тесного контакта с инфицированными птицами. [7] У млекопитающих, включая людей, заражение птичьим гриппом (будь то LPAI или HPAI) встречается редко. Симптомы инфекции варьируются от легких до тяжелых, включая лихорадку, диарею и кашель. [8]
Вирус гриппа А выделяется со слюной, слизью и фекалиями инфицированных птиц; другие инфицированные животные могут выделять вирусы птичьего гриппа с респираторными выделениями и другими жидкостями организма (например, коровьим молоком). [9] Вирус может быстро распространяться среди домашних птиц и среди диких птиц. [9] Особенно вирулентный штамм, вирус гриппа А подтипа H5N1 (A/H5N1), может уничтожить поголовье домашней птицы, и, по оценкам, в попытках сдержать вирус было убито около полумиллиарда птиц, выращиваемых на фермах. [10]
Высокопатогенный грипп птиц
Из-за воздействия птичьего гриппа на экономически важные птицеводческие фермы в 1981 году была разработана система классификации, которая разделила штаммы птичьего вируса на высокопатогенные (и, следовательно, потенциально требующие решительных мер контроля) или низкопатогенные. Тест на это основан исключительно на воздействии на кур — штамм вируса является высокопатогенным птичьим гриппом (ВППГ), если 75% или более кур погибают после преднамеренного заражения им. Альтернативная классификация — низкопатогенный птичий грипп (НППГ). [11] С тех пор эта система классификации была изменена, чтобы принять во внимание структуру белка гемагглютинина вируса. [12] Другие виды птиц, особенно водоплавающие, могут заразиться вирусом HPAI, не испытывая серьезных симптомов, и могут распространять инфекцию на большие расстояния; точные симптомы зависят от вида птицы и штамма вируса. [11] Классификация штамма птичьего вируса как HPAI или LPAI не позволяет предсказать, насколько серьезным может быть заболевание, если оно заразит людей или других млекопитающих. [11] [13]
С 2006 года Всемирная организация здравоохранения животных требует сообщать обо всех случаях обнаружения LPAI H5 и H7 из-за их потенциальной возможности мутировать в высокопатогенные штаммы. [14]
Вирусология

Птичий грипп вызывается вирусом гриппа А , который в основном поражает птиц, но может также инфицировать людей и других млекопитающих. [16] [17] Грипп А — это РНК-вирус с геномом, включающим отрицательно-полярный РНК-сегментированный геном, который кодирует 11 вирусных генов. [18] Вирусная частица (также называемая вирионом) имеет диаметр 80–120 нанометров и эллиптическую или нитевидную форму. [19] [20] Имеются данные о том, что вирус может выживать в течение длительного времени в пресной воде после выделения с фекалиями его птичьим хозяином и может выдерживать длительное замораживание. [21]
На поверхности вирусной оболочки находятся два белка : гемагглютинин и нейраминидаза. [4] Это основные антигены вируса, против которых вырабатываются нейтрализующие антитела. Эпидемии и эпизоотии вируса гриппа связаны с изменениями в его антигенной структуре. [22]
Гемагглютинин (H) — это антигенный гликопротеин , который позволяет вирусу связываться с клеткой-хозяином и проникать в нее. Нейраминидаза (N) — это антигенный гликозилированный фермент , который облегчает высвобождение потомства вирусов из инфицированных клеток. [23] Известно 18 типов гемагглютинина, из которых H1 — H16 были обнаружены у птиц, и 11 типов нейраминидазы. [16]
Подтипы
Подтипы гриппа A определяются комбинацией белков H и N в вирусной оболочке ; например, « H5N1 » обозначает подтип гриппа A, который имеет белок гемагглютинина (H) типа 5 и белок нейраминидазы (N) типа 1. [7] Схема подтипирования учитывает только два белка оболочки, а не другие белки, кодируемые РНК вируса. Почти все возможные комбинации H (от 1 до 16) и N (от 1 до 11) были выделены из диких птиц. [24] Дополнительные вариации существуют внутри подтипов и могут привести к очень значительным различиям в способности вируса инфицировать и вызывать заболевание. [25]
Номенклатура вируса гриппа

Для однозначного описания конкретного изолята вируса исследователи используют международно принятую номенклатуру вирусов гриппа [26] , которая описывает, среди прочего, вид животного, от которого был выделен вирус, а также место и год сбора. Например, A/chicken/Nakorn-Patom/Thailand/CU-K2/04(H5N1) : [27]
- A обозначает род гриппа ( A , B или C )
- курица — вид животного, у которого был обнаружен изолят (примечание: у человеческих изолятов этот компонент отсутствует, поэтому по умолчанию они идентифицируются как человеческие изоляты)
- Накхон-Патом/Таиланд – это место, где был выделен этот вирус.
- CU-K2 — это лабораторный номер, который отличает его от других вирусов гриппа, выделенных в том же месте и в том же году.
- 04 представляет год изоляции 2004
- H5 обозначает пятый из нескольких известных типов белка гемагглютинина.
- N1 обозначает первый из нескольких известных типов белка нейраминидазы .
Другие примеры включают: A/duck/Hong Kong/308/78(H5N3), A/avian/NY/01(H5N2), A/chicken/Mexico/31381-3/94(H5N2) и A/shoveler/Egypt/03(H5N2). [28]
Генетическая характеристика
Анализ генома вируса позволяет исследователям определить порядок его нуклеотидов. Сравнение генома вируса с геномом другого вируса может выявить различия между двумя вирусами. [16] [29] Генетические вариации важны, поскольку они могут изменять аминокислоты, из которых состоят белки вируса гриппа, что приводит к структурным изменениям белков и, таким образом, к изменению свойств вируса. Некоторые из этих свойств включают способность обходить иммунитет и способность вызывать тяжелое заболевание. [29]
Генетическое секвенирование позволяет дополнительно охарактеризовать штаммы гриппа по их кладам или субкладам , выявляя связи между различными образцами вируса и отслеживая эволюцию вируса с течением времени. [29]
Видовой барьер
Люди могут заразиться птичьим гриппом, если они находятся в тесном контакте с инфицированными птицами. Симптомы варьируются от легких до тяжелых (включая смерть), но по состоянию на декабрь 2024 года не было зафиксировано ни одного случая устойчивой передачи вируса от человека к человеку. [4] [17] [30]
Существует ряд факторов, которые обычно не позволяют птичьему гриппу вызывать эпидемии среди людей или других млекопитающих. [31] [32] Одним из них является то, что белок HA птичьего гриппа связывается с рецепторами сиаловой кислоты альфа-2,3 , которые присутствуют в дыхательных путях и кишечнике птиц, в то время как HA человеческого гриппа связывается с рецепторами сиаловой кислоты альфа-2,6, которые присутствуют в верхних дыхательных путях человека. [33] [34] Другие факторы включают способность реплицировать геном вирусной РНК в ядре клетки-хозяина, избегать иммунных реакций хозяина и передаваться между особями. [35]
Вирусы гриппа постоянно изменяются по мере накопления небольших генетических мутаций , процесс, известный как антигенный дрейф . Со временем мутация может привести к изменению антигенных свойств, так что антитела хозяина (приобретенные в результате вакцинации или предшествующей инфекции) не будут обеспечивать эффективную защиту, что приведет к новой вспышке заболевания. [36]
Сегментированный геном вирусов гриппа облегчает генетическую реассортацию . Это может произойти, если хозяин одновременно инфицирован двумя разными штаммами вируса гриппа; тогда вирусы могут обмениваться генетическим материалом по мере размножения в клетках хозяина. [37] Таким образом, вирус птичьего гриппа может приобретать характеристики, такие как способность заражать людей, от другого штамма вируса. Наличие как альфа-2,3, так и альфа-2,6 рецепторов сиаловой кислоты в тканях свиньи допускает коинфекцию вирусами птичьего гриппа и человеческого гриппа. Эта восприимчивость делает свиней потенциальным «плавильным котлом» для реассортации вирусов гриппа А. [38]
Эпидемиология
История
Птичий грипп (исторически известный как птичья чума) вызывается адаптированными к птицам штаммами вируса гриппа типа А. [ 4] Заболевание было впервые выявлено Эдоардо Перрончито в 1878 году, когда он был дифференцирован от других заболеваний, вызывающих высокий уровень смертности среди птиц; в 1955 году было установлено, что вирус птичьей чумы тесно связан с человеческим гриппом. В 1972 году стало очевидно, что многие подтипы птичьего гриппа были эндемичными в популяциях диких птиц. [11]
В период с 1959 по 1995 год было зафиксировано 15 вспышек высокопатогенного птичьего гриппа (ВПГП) среди домашней птицы, при этом потери варьировались от нескольких птиц на одной ферме до многих миллионов. В период с 1996 по 2008 год вспышки ВПГП среди домашней птицы были зарегистрированы по меньшей мере 11 раз, и 4 из этих вспышек привели к гибели или выбраковке миллионов птиц. [11] С тех пор несколько штаммов вируса (как ВПГП, так и ВПГП) стали эндемичными среди диких птиц, а вспышки среди домашней птицы стали все более частыми, особенно подтипов H5 и H7.
Передача и профилактика

Птицы – вирусы гриппа А различных подтипов имеют большой резервуар в диких водоплавающих птицах отрядов гусеобразных (например, утки, гуси и лебеди) и ржанкообразных (например, чайки, крачки и кулики), которые могут инфицировать дыхательные пути и желудочно-кишечный тракт, не влияя на здоровье хозяина. [40] Затем они могут переноситься птицей на большие расстояния, особенно во время ежегодной миграции. Инфицированные птицы могут выделять вирусы птичьего гриппа А в своей слюне, носовых выделениях и фекалиях; восприимчивые птицы заражаются при контакте с вирусом, который выделяют инфицированные птицы. [41] Вирус может выживать в течение длительного времени в воде и при низких температурах и может распространяться с одной фермы на другую на сельскохозяйственном оборудовании. [42] Домашние птицы (куры, индейки, утки и т. д.) могут заразиться вирусами птичьего гриппа А через прямой контакт с инфицированными водоплавающими птицами или другими инфицированными домашними птицами, а также через контакт с загрязненными фекалиями или поверхностями.
Вспышки птичьего гриппа у домашних птиц вызывают беспокойство по нескольким причинам. Существует вероятность того, что вирусы птичьего гриппа с низкой патогенностью (LPAI) могут эволюционировать в штаммы, которые являются высокопатогенными для домашней птицы (HPAI), и последующий потенциал для значительного заболевания и смерти среди домашней птицы во время вспышек. В связи с этим международные правила гласят, что любое обнаружение подтипов H5 или H7 (независимо от их патогенности) должно быть сообщено в соответствующий орган. [43] [44] Также возможно, что вирусы птичьего гриппа могут передаваться людям и другим животным, которые контактировали с инфицированными птицами, вызывая инфекцию с непредсказуемыми, но иногда и фатальными последствиями.
При обнаружении инфекции HPAI у домашней птицы обычно забивают инфицированных животных и тех, кто находится поблизости, чтобы быстро сдержать, контролировать и искоренить болезнь. Это делается вместе с ограничениями передвижения, улучшением гигиены и биологической безопасности, а также усилением наблюдения. [42]
Люди — вирусы птичьего гриппа, как HPAI, так и LPAI, могут заражать людей, которые находятся в тесном, незащищенном контакте с инфицированной домашней птицей. Случаи межвидовой передачи редки, с симптомами, варьирующимися по степени тяжести от отсутствия симптомов или легкого заболевания до тяжелого заболевания, приведшего к смерти. [45] [44] По состоянию на февраль 2024 года было очень мало случаев передачи от человека к человеку, и каждая вспышка была ограничена несколькими людьми. [46] Все подтипы птичьего гриппа A имеют потенциал для преодоления видового барьера, при этом H5N1 и H7N9 считаются самыми большими угрозами. [47] [48]
Чтобы избежать заражения, широкой общественности рекомендуется избегать контакта с больными птицами или потенциально зараженными материалами, такими как туши или фекалии. Людям, работающим с птицами, например, экологам или работникам птицеводства, рекомендуется носить соответствующие средства индивидуальной защиты. [49]
Другие животные – птичий грипп поразил широкий спектр других животных , как правило, из-за употребления в пищу инфицированных птиц. [50] Были случаи, когда могла произойти передача заболевания между млекопитающими, включая тюленей и коров. [51] [52]
Вероятность пандемии
Вирусы гриппа имеют относительно высокую скорость мутаций, что характерно для РНК-вирусов . [53] Сегментация генома вируса гриппа А облегчает генетическую рекомбинацию путем реассортации сегментов у хозяев, которые одновременно заражаются двумя разными штаммами вирусов гриппа. [54] [55] При реассортации между штаммами птичий штамм, который не поражает людей, может приобрести характеристики от другого штамма, которые позволяют ему заражать и передаваться между людьми — зоонозное событие. [41] Считается, что все вирусы гриппа А, вызывающие вспышки или пандемии среди людей с 1900-х годов, произошли от штаммов, циркулирующих среди диких водоплавающих птиц, путем реассортации с другими штаммами гриппа. [56] [57] Возможно (хотя и не наверняка), что свиньи могут выступать в качестве промежуточного хозяина для реассортации. [58]
По состоянию на июнь 2024 года существует обеспокоенность по поводу двух подтипов птичьего гриппа, которые циркулируют в популяциях диких птиц по всему миру, H5N1 и H7N9 . Оба они потенциально могут уничтожить поголовье домашней птицы, и оба перешли на людей с относительно высокими показателями летальности . [59]
Наблюдение
Глобальная система надзора за гриппом и реагирования на него (GISRS) — это глобальная сеть лабораторий, которые отслеживают распространение гриппа с целью предоставления Всемирной организации здравоохранения информации о контроле гриппа и информирования о разработке вакцин. [60] Ежегодно сеть GISRS тестирует несколько миллионов образцов через сеть лабораторий в 127 странах. [61] Помимо человеческих вирусов, GISRS отслеживает птичьи, свиные и другие потенциально зоонозные вирусы гриппа.
Вакцина
Птица – можно вакцинировать птицу против определенных штаммов гриппа HPAI. Вакцинацию следует сочетать с другими мерами контроля, такими как мониторинг инфекции, раннее обнаружение и биобезопасность. [62] [63]
Люди – Доступно несколько «кандидатных вакцин» на случай, если птичий вирус приобретет способность заражать и передаваться среди людей. Существуют стратегические запасы вакцин против подтипа H5N1, который считается самым рискованным. [64] [65] [66] Вакцина против подтипа H7N9, который также заражал людей, прошла ограниченное количество испытаний. [67] В случае вспышки «кандидатная» вакцина будет быстро проверена на безопасность, а также эффективность против зоонозного штамма, а затем авторизована и распространена среди производителей вакцин. [68]
Вакцина против зоонозного гриппа Seqirus разрешена к использованию в Европейском Союзе. [69] Это вакцина H5N8, которая предназначена для обеспечения приобретенного иммунитета против вирусов гриппа А подтипа H5. [69]
Вирус гриппа А подтипа H5N1
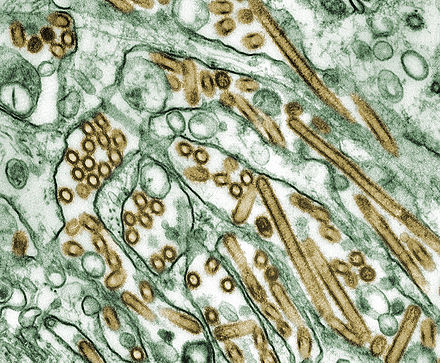 |
Высокопатогенный вирус гриппа А подтипа H5N1 — это новый вирус птичьего гриппа, который вызывает глобальную обеспокоенность как потенциальная угроза пандемии . Его часто называют просто «птичьим гриппом» или «птичьим гриппом», хотя это всего лишь один из многих подтипов.
A/H5N1 убил миллионы домашних птиц во все большем числе стран Азии, Европы и Африки. Эксперты в области здравоохранения обеспокоены тем, что сосуществование вирусов гриппа человека и вирусов птичьего гриппа (особенно H5N1) предоставит возможность для обмена генетическим материалом между вирусами, специфичными для конкретных видов, что может привести к появлению нового вирулентного штамма гриппа, который легко передается и смертелен для людей. [70]
Грипп A/H5N1 был впервые зарегистрирован в небольшой вспышке среди домашней птицы в Шотландии [71] в 1959 году, с многочисленными вспышками впоследствии на каждом континенте. [72] Первая известная передача A/H5N1 человеку произошла в Гонконге в 1997 году, когда произошла вспышка из 18 случаев заболевания людей, приведшая к 6 смертельным исходам. Было установлено, что все инфицированные люди контактировали с инфицированными птицами на рынках домашней птицы. Поскольку болезнь продолжала распространяться среди домашних птиц на территории, было принято решение забить все 1,6 миллиона домашних птиц в этом районе и ввести строгий контроль за перемещением и обращением с домашней птицей. Это положило конец вспышке. [73] [74]
Имеются слабые доказательства в поддержку ограниченной передачи вируса A/H5N1 от человека к человеку в 139 вспышках между 2005 и 2009 годами на Суматре. Число репродукций было значительно ниже порогового значения для устойчивой передачи. [75]
В период с 2003 по ноябрь 2024 года Всемирная организация здравоохранения зарегистрировала 948 подтвержденных случаев гриппа H5N1, приведших к 464 смертельным случаям. [76] Истинный уровень смертности может быть ниже, поскольку некоторые случаи со слабовыраженными симптомами могли не быть идентифицированы как H5N1. [77]
Вирус гриппа А подтипа H7N9

Значительная вспышка вируса гриппа А подтипа H7N9 (A/H7N9) началась в марте 2013 года, когда тяжелый грипп поразил 18 человек в Китае; шесть впоследствии умерли. [78] Было обнаружено, что низкопатогенный штамм A/H7N9 циркулировал среди кур, и что все пострадавшие люди были подвержены воздействию на рынках птицы . Дальнейшие случаи среди людей и птицы в материковом Китае продолжали выявляться спорадически в течение года, за которыми последовал пик около праздничного сезона китайского Нового года (январь и февраль) в начале 2014 года, который был приписан сезонному всплеску производства птицы. До декабря 2013 года было зарегистрировано 139 случаев с 47 смертельными исходами. [79]
Инфекции среди людей и домашней птицы продолжались в течение следующих нескольких лет, снова с пиками около нового года. В 2016 году появился штамм вируса, который был высокопатогенным для кур. [80] [81] Чтобы сдержать вспышку HPAI, китайские власти в 2017 году инициировали крупномасштабную кампанию вакцинации против птичьего гриппа у домашней птицы. С тех пор количество вспышек среди домашней птицы, а также количество случаев заболевания людей значительно сократилось. У людей симптомы и смертность как от штаммов LPAI, так и HPAI были схожими. [80] Хотя с февраля 2019 года не было зарегистрировано ни одного случая заражения человека H7N9, вирус все еще циркулирует среди домашней птицы, особенно среди кур-несушек. Он продемонстрировал антигенный дрейф, чтобы уклоняться от вакцин, и остается потенциальной угрозой для птицеводческой отрасли и общественного здравоохранения. [81]
Генетический и эволюционный анализы показали, что вирусы A(H7) в китайской вспышке, вероятно, перешли от домашней утки к популяциям кур в Китае, а затем реассортировали с птичьим гриппом A(H9N2), чтобы создать штамм гриппа A(H7N9), который поразил людей. Генетические характеристики вируса A(H7N9) вызывают беспокойство из-за их пандемического потенциала, например, их способности распознавать рецепторы вируса человеческого и птичьего гриппа, что влияет на способность вызывать устойчивую передачу от человека к человеку или способность реплицироваться в организме человека. [78]
В период с февраля 2013 года по февраль 2019 года было зарегистрировано 1568 подтвержденных случаев заболевания людей и 616 смертей, связанных со вспышкой в Китае. [82] [83] Большинство случаев заболевания людей были связаны с контактом с домашней птицей на рынках или фермах. Передача между людьми остается ограниченной с некоторыми свидетельствами небольших семейных кластеров. Однако нет никаких доказательств устойчивой передачи гриппа A/H7N9 от человека к человеку. [80]
В начале 2017 года в США произошли вспышки птичьего гриппа A(H7N9) среди домашней птицы. Штамм в этих вспышках имел североамериканское происхождение и не связан с азиатской линией H7N9, которая связана с человеческими инфекциями в Китае. [80]
Домашние животные

Несколько видов домашних животных были инфицированы вирусом H5N1 и продемонстрировали симптомы этой инфекции, включая кошек, собак, хорьков, свиней и птиц. [84]
Птица
В Соединенных Штатах предпринимаются попытки минимизировать присутствие HPAI у домашней птицы посредством рутинного наблюдения за стадами домашней птицы в коммерческих птицеводческих хозяйствах. Обнаружение вируса HPAI может привести к немедленной выбраковке стада. Менее патогенные вирусы контролируются вакцинацией. [85]
Молочные коровы
В апреле 2024 года птичий грипп был впервые обнаружен у молочных коров в нескольких штатах США и впоследствии распространился более широко в течение года. Было обнаружено, что грипп A(H5N1) присутствует в высоких концентрациях в молочных железах и в молоке пораженных коров. [86] [87] [88] Было показано, что вирус может сохраняться на доильном оборудовании, что обеспечивает вероятный путь передачи от коровы к корове и от коровы к человеку. [89] У ряда людей, которые контактировали с коровами, был положительный результат теста на вирус со слабыми симптомами. [90] По данным CDC, 7% из 115 работников молочной промышленности имели признаки недавнего заражения в исследовании, проведенном в Мичигане и Колорадо с июня по август 2024 года, причем у половины из них не было симптомов. Это выше оценок предыдущих исследований передачи среди домашней птицы. Все работники молочной промышленности работали на уборке молочного зала, и никто из них не использовал средства индивидуальной защиты. [91]
Кошки
Глобальные аспекты
Глобальные меры
В 2005 году было объявлено о создании Международного партнерства по птичьему и пандемическому гриппу с целью повышения значимости птичьего гриппа, координации усилий и улучшения отчетности и надзора за болезнями для лучшего реагирования на будущие пандемии. Появились новые сети лабораторий для обнаружения и реагирования на птичий грипп, такие как Центр управления кризисами в области здоровья животных, Глобальная сеть по надзору за птичьим гриппом, OFFLU и Глобальная система раннего предупреждения об основных болезнях животных. После вспышки 2003 года государства-члены ВОЗ также признали необходимость более прозрачного и справедливого обмена вакцинами и другими преимуществами этих сетей. [95] Совместные меры, принятые в ответ на HPAI, послужили основой для программ, связанных с другими возникающими и повторно возникающими инфекционными заболеваниями.
Влияние на национальную политику
Контроль HPAI также использовался в политических целях. В Индонезии переговоры с глобальными сетями реагирования были использованы для рецентрализации власти и финансирования в Министерстве здравоохранения. [96] Во Вьетнаме политики при поддержке Продовольственной и сельскохозяйственной организации Объединенных Наций (ФАО) использовали контроль HPAI для ускорения индустриализации производства животноводческой продукции на экспорт, предложив увеличить долю крупных коммерческих ферм и сократить количество птицеводов с 8 до 2 миллионов к 2010 году. [97]
Традиционные азиатские практики
Производство домашней птицы на заднем дворе рассматривалось как «традиционная азиатская» сельскохозяйственная практика, которая контрастировала с современным коммерческим производством домашней птицы и рассматривалась как угроза биологической безопасности. Производство домашней птицы на заднем дворе, по-видимому, несло в себе больший риск, чем коммерческое производство, из-за отсутствия биологической безопасности и тесного контакта с людьми, хотя распространение HPAI в интенсивно выращиваемых стадах было выше из-за высокой плотности выращивания и генетической однородности. [98] [99] Сама азиатская культура была обвинена в качестве причины, по которой определенные вмешательства, такие как те, которые рассматривали только вмешательства на основе размещения, потерпят неудачу без поиска многогранных решений. [97]
Экономическое воздействие
Примерно 20% потребляемого в развивающихся странах белка поступает из птицы. [98] В отчете ФАО подсчитано, что общие экономические потери, вызванные птичьим гриппом в Юго-Восточной Азии к 2005 году, составили около 10 миллиардов долларов США. Это оказало наибольшее влияние на мелких коммерческих и домашних производителей. [100]
Поскольку домашняя птица служит источником продовольственной безопасности и ликвидных активов, наиболее уязвимыми группами населения были бедные мелкие фермеры. [97] Потеря птиц из-за HPAI и выбраковки во Вьетнаме привела к средней потере 2,3 месяцев производства и 69–108 долларов США для домохозяйств, многие из которых имеют доход 2 доллара в день или меньше. [100] Потерю продовольственной безопасности для уязвимых домохозяйств можно увидеть в задержке роста детей в возрасте до пяти лет в Египте. Женщины являются еще одной группой риска, поскольку в большинстве регионов мира небольшие стада находятся под присмотром женщин. Широко распространенная выбраковка также привела к сокращению числа девочек, посещающих школы в Турции. [98]
Ожидается, что цены на яйца в США вырастут из-за птичьего гриппа. [101]
Смотрите также
- Глобальное распространение H5N1
- Подтипы вируса гриппа А
- Вирус гриппа А подтипа H5N1
- Вирус гриппа А подтипа H7N9
- Грипп
- вирус гриппа А
- Пандемия гриппа
- Проект секвенирования генома гриппа
- Исследования гриппа
- Вакцина против гриппа
- Международное партнерство по борьбе с птичьим и пандемическим гриппом
- Сеть экспертов МЭБ/ФАО по гриппу животных
Ссылки
- ^ "Птичий грипп A H5N1 – Соединенное Королевство Великобритании и Северной Ирландии". www.who.int . Получено 2024-05-16 .
- ^ Li YT, Linster M, Mendenhall IH, Su YC, Smith GJ (декабрь 2019 г.). «Вирусы птичьего гриппа у людей: уроки прошлых вспышек». British Medical Bulletin . 132 (1): 81– 95. doi :10.1093/bmb/ldz036. PMC 6992886. PMID 31848585 .
- ^ Джозеф У, Су ЙК, Виджайкришна Д, Смит ГДж (январь 2017 г.). «Экология и адаптивная эволюция межвидовой передачи гриппа А». Грипп и другие респираторные вирусы . 11 (1): 74– 84. doi :10.1111/irv.12412. PMC 5155642. PMID 27426214 .
- ^ abcd "Птичий грипп у птиц". Центры по контролю и профилактике заболеваний США (CDC) . 2022-06-14 . Получено 2024-05-06 .
- ^ "Птичий грипп: как обнаружить и сообщить о нем у домашней птицы или других птиц, содержащихся в неволе". Департамент окружающей среды, продовольствия и сельского хозяйства и Агентство по охране здоровья животных и растений . 2022-12-13 . Получено 2024-05-06 .
- ^ «Вакцинация домашней птицы против высокопатогенного птичьего гриппа – Доступные вакцины и стратегии вакцинации». www.efsa.europa.eu . 2023-10-10 . Получено 2024-05-09 .
- ^ ab "Вирусы гриппа типа А". Центры по контролю и профилактике заболеваний США (CDC) . 2024-02-01 . Получено 2024-05-03 .
- ^ "Птичий грипп: руководство, данные и анализ". GOV.UK . 2021-11-18 . Получено 2024-05-09 .
- ^ ab "Профилактика и противовирусное лечение вирусов птичьего гриппа у людей". Центры по контролю и профилактике заболеваний . 2024-04-19.
- ^ Bourk I (26 апреля 2024 г.). «'Беспрецедентный': как птичий грипп стал пандемией среди животных». www.bbc.com . Получено 08.05.2024 .
- ^ abcde Alexander DJ, Brown IH (апрель 2009). «История высокопатогенного птичьего гриппа». Revue Scientifique et Technique . 28 (1): 19– 38. doi :10.20506/rst.28.1.1856. PMID 19618616.
- ^ "Информационный листок по A(H5N1)". www.ecdc.europa.eu . 2017-06-15 . Получено 2024-05-21 .
- ^ "Текущая ситуация с птичьим гриппом у людей в США". Центры по контролю и профилактике заболеваний США (CDC) . 2024-04-05 . Получено 2024-05-22 .
- ^ "Национальный план надзора за птичьим гриппом H5/H7". Министерство сельского хозяйства США . Служба инспекции здоровья животных и растений. Октябрь 2013 г.
- ^ "Воссозданы вирионы гриппа 1918 года". Центры по контролю и профилактике заболеваний США (CDC) . Архивировано из оригинала 26 октября 2020 года . Получено 24 апреля 2018 года .
- ^ abc "Типы вирусов гриппа". Центры по контролю и профилактике заболеваний США (CDC) . 2023-03-30 . Получено 2024-05-22 .
- ^ ab "Грипп (птичий и другие зоонозные)". Всемирная организация здравоохранения . 3 октября 2023 г. Получено 2024-05-06 .
- ^ Samji T (декабрь 2009 г.). «Грипп A: понимание жизненного цикла вируса». Йельский журнал биологии и медицины . 82 (4): 153–159 . PMC 2794490. PMID 20027280 .
- ^ Noda T (2011). " Нативная морфология вирионов гриппа". Frontiers in Microbiology . 2 : 269. doi : 10.3389/fmicb.2011.00269 . PMC 3249889. PMID 22291683.
- ^ Dadonaite B, Vijayakrishnan S, Fodor E, Bhella D, Hutchinson EC (август 2016 г.). «Нитчатые вирусы гриппа». Журнал общей вирусологии . 97 (8): 1755–1764 . doi :10.1099/jgv.0.000535. PMC 5935222. PMID 27365089 .
- ^ Шохам Д., Джахангир А., Руенфет С., Такехара К. (2012-10-04). "Сохранение вирусов птичьего гриппа в различных типах искусственно замороженной воды окружающей среды". Исследования и лечение гриппа . 2012 : 912326. doi : 10.1155/2012/912326 . PMC 3471417. PMID 23091712 .
- ^ "Птичий грипп". Тема NIOSH по охране труда и технике безопасности . Национальный институт охраны труда и техники безопасности. 2018-10-17.
- ^ Couch R (1996). "Глава 58. Размножение ортомиксовирусов". В Baron S (ред.). Медицинская микробиология . Галвестон: Медицинское отделение Техасского университета в Галвестоне. ISBN 978-0-9631172-1-2. PMID 21413353. Архивировано из оригинала 3 мая 2009 г.
- ^ "FluGlobalNet - Птичий грипп" . science.vla.gov.uk . Проверено 5 июня 2024 г.
- ^ Eisfeld AJ, Neumann G, Kawaoka Y (январь 2015 г.). «В центре: рибонуклеопротеины вируса гриппа А». Nature Reviews. Microbiology . 13 (1): 28– 41. doi :10.1038/nrmicro3367. PMC 5619696. PMID 25417656 .
- ^ «Пересмотр системы номенклатуры вирусов гриппа: меморандум ВОЗ». Бюллетень Всемирной организации здравоохранения . 58 (4): 585–591 . 1980. PMC 2395936. PMID 6969132.
Настоящий Меморандум был составлен подписавшими его лицами, указанными на странице 590, по случаю встречи, состоявшейся в Женеве в феврале 1980 года.
- ^ CDC (2024-09-27). "Типы вирусов гриппа". Центры по контролю и профилактике заболеваний . Получено 2024-12-15 .
- ^ Payungporn S, Chutinimitkul S, Chaisingh A, Damrongwantanapokin S, Nuansrichay B, Pinyochon W и др. (апрель 2006 г.). «Дискриминация высокопатогенных и низкопатогенных вирусов птичьего гриппа H5 A». Emerging Infectious Diseases . 12 (4): 700– 701. doi :10.3201/eid1204.051427. PMC 3294708 . PMID 16715581.
- ^ abc "Секвенирование генома вируса гриппа и генетическая характеристика". Центры по контролю и профилактике заболеваний . 2024-02-27 . Получено 2024-05-24 .
- ^ Lin TH, Zhu X, Wang S, Zhang D, McBride R, Yu W и др. (2024-12-06). «Единственная мутация в гемагглютинине бычьего гриппа H5N1 переключает специфичность на человеческие рецепторы». Science . 386 (6726): 1128– 1134. doi : 10.1126/science.adt0180 .
- ^ Petric PP, Schwemmle M, Graf L (июль 2023 г.). «Факторы рестрикции вируса гриппа А, которые формируют барьер человеческого вида и эволюцию вируса». PLOS Pathogens . 19 (7): e1011450. doi : 10.1371/journal.ppat.1011450 . PMC 10325056. PMID 37410755 .
- ^ Koçer ZA, Jones JC, Webster RG (декабрь 2013 г.). Atlas RM, Maloy S (ред.). «Возникновение вирусов гриппа и преодоление видового барьера». Microbiology Spectrum . 1 (2). doi :10.1128/microbiolspec.OH-0010-2012. PMID 26184958.
- ^ Bertram S, Glowacka I, Steffen I, Kühl A, Pöhlmann S (сентябрь 2010 г.). «Новые идеи протеолитического расщепления гемагглютинина вируса гриппа». Reviews in Medical Virology . 20 (5): 298– 310. doi :10.1002/rmv.657. PMC 7169116. PMID 20629046. HA
вируса гриппа связывается с альфа-2–3-связанными (вирусы птиц) или альфа-2–6-связанными (вирусы человека) сиаловыми кислотами, представленными белками или липидами на поверхности клетки-хозяина.
- ^ Кучипуди С.В., Нелли Р.К., Гонту А., Сатьякумар Р., Сурендран Наир М., Суббия М. (февраль 2021 г.). «Рецепторы сиаловой кислоты: ключ к разгадке загадки распространения зоонозного вируса». Вирусы . 13 (2): 262. дои : 10.3390/v13020262 . ПМЦ 7915228 . ПМИД 33567791.
- ^ Long JS, Mistry B, Haslam SM, Barclay WS (январь 2019 г.). «Хост и вирусные детерминанты видовой специфичности вируса гриппа А». Nature Reviews. Microbiology . 17 (2): 67– 81. doi :10.1038/s41579-018-0115-z. PMID 30487536.
- ^ "Как вирусы гриппа могут меняться". Центры по контролю и профилактике заболеваний США (CDC) . 2022-12-12 . Получено 2024-05-22 .
- ^ Steel J, Lowen AC (2014), Compans RW, Oldstone MB (ред.), «Реассортация вируса гриппа», Патогенез гриппа и контроль – Том I , Текущие темы микробиологии и иммунологии, т. 385, Cham: Springer International Publishing, стр. 377–401 , doi :10.1007/82_2014_395, ISBN 978-3-319-11155-1, PMID 25007845.
- ^ Schnitzler SU, Schnitzler P (декабрь 2009 г.). «Обновление о вирусе гриппа свиного происхождения A/H1N1: обзор». Virus Genes . 39 (3): 279– 292. doi :10.1007/s11262-009-0404-8. PMC 7088521 . PMID 19809872.
Если птичий вирус мутирует или перестраивается и приобретает способность связываться с α2,6-связанными сиаловыми кислотами, он может преодолеть видовой барьер и заразить людей. Ткани свиней экспрессируют обе формы сиаловой кислоты и могут быть коинфицированы человеческими и птичьими вирусами. Таким образом, свиньи служат плавильным сосудом для штаммов человеческого, птичьего и свиного гриппа.
- ^ Томпсон Д., Биркьедал И. (2001). Кулики . Colin Baxter Photography Ltd. ISBN 978-1841070759.
- ^ «Стратегия смягчения последствий птичьего гриппа у диких птиц в Англии и Уэльсе». GOV.UK – Департамент по охране окружающей среды, продовольствия и сельским делам . 18 марта 2024 г. Получено 25 июля 2024 г.
- ^ ab "Передача вирусов птичьего гриппа между животными и людьми". Центры США по контролю и профилактике заболеваний (CDC) . 2024-05-15 . Получено 2024-06-10 .
- ^ ab "Птичий грипп". WOAH – Всемирная организация по охране здоровья животных . Получено 2024-06-10 .
- ^ «Профилактика и контроль птичьего гриппа H5 и H7 в системе сбыта живой птицы». Министерство сельского хозяйства США . Август 2020 г. Получено 15 июня 2024 г.
- ^ ab "Вопросы и ответы по птичьему гриппу". Официальный сайт Европейской комиссии . 11 июня 2024 г. Получено 2024-06-11 .
- ^ "Инфекции вируса птичьего гриппа А у людей". Центры по контролю и профилактике заболеваний США (CDC) . 2024-05-30 . Получено 2024-06-11 .
- ^ "Сообщенные случаи заражения людей вирусами птичьего гриппа А". Центры по контролю и профилактике заболеваний . 2024-02-01 . Получено 2024-06-11 .
- ^ "Зоонозный грипп". Всемирная организация здравоохранения . Получено 2024-06-16 .
- ^ «Следующая пандемия: грипп H5N1 и H7N9?». Gavi, Vaccine Alliance . Получено 2024-06-16 .
- ^ "Высокопатогенный вирус птичьего гриппа A(H5N1) у животных: временные рекомендации по профилактике, мониторингу и расследованиям в области общественного здравоохранения". Центры США по контролю и профилактике заболеваний . 2024-06-05 . Получено 2024-06-13 .
- ^ "Птичий грипп "перекинулся" на выдр и лисиц в Великобритании". BBC News . 2023-02-02 . Получено 2024-06-11 .
- ^ "Исследование смертности тюленей от птичьего гриппа H5N1 выявило множественные линии". Центр исследований и политики в области инфекционных заболеваний . 2023-03-15 . Получено 2024-06-13 .
- ^ Козлов М (июнь 2024 г.). «Огромное количество вируса птичьего гриппа обнаружено в сыром молоке инфицированных коров». Nature . doi :10.1038/d41586-024-01624-1. PMID 38840011.
- ^ Санхуан Р., Небот М.Р., Кирико Н., Мански Л.М., Белшоу Р. (октябрь 2010 г.). «Уровни вирусных мутаций». Журнал вирусологии . 84 (19): 9733–9748 . doi :10.1128/JVI.00694-10. ПМЦ 2937809 . ПМИД 20660197.
- ^ Коу Z, Лэй FM, Ю Дж, Фань ZJ, Инь ZH, Цзя CX и др. (декабрь 2005 г.). «Новый генотип вирусов птичьего гриппа H5N1, выделенный от древесных воробьев в Китае». Журнал вирусологии . 79 (24): 15460–15466 . doi :10.1128/JVI.79.24.15460-15466.2005. ПМК 1316012 . ПМИД 16306617.
- ^ Глобальная сеть наблюдения за программой по гриппу Всемирной организации здравоохранения (октябрь 2005 г.). «Эволюция вирусов птичьего гриппа H5N1 в Азии». Emerging Infectious Diseases . 11 (10): 1515– 1521. doi :10.3201/eid1110.050644. PMC 3366754. PMID 16318689 . На рисунке 1 показано схематическое изображение генетического родства генов гемагглютинина азиатского вируса H5N1 из различных изолятов вируса.
- ^ Таубенбергер Дж. К., Моренс Д. М. (апрель 2010 г.). «Грипп: пандемия прошлого и будущего». Отчеты общественного здравоохранения . 125 (Приложение 3): 16–26 . doi :10.1177/00333549101250S305. PMC 2862331. PMID 20568566 .
- ^ Webster RG, Bean WJ, Gorman OT, Chambers TM, Kawaoka Y (март 1992). «Эволюция и экология вирусов гриппа А». Microbiological Reviews . 56 (1): 152– 179. doi :10.1128/mr.56.1.152-179.1992. PMC 372859 . PMID 1579108.
- ^ "Информационный бюллетень о свином гриппе у людей и свиней". Европейский центр по контролю и профилактике заболеваний . 2017-06-15 . Получено 2024-06-13 .
- ^ "Глобальный вирус гриппа с зоонозным потенциалом". Продовольственная и сельскохозяйственная организация Объединенных Наций (ФАО) . 29 июля 2020 г. Получено 24 июня 2024 г.
- ^ Ли К, Фанг Дж (2013). Исторический словарь Всемирной организации здравоохранения. Rowman & Littlefield. ISBN 9780810878587.
- ^ "70 лет GISRS – Глобальной системе надзора за гриппом и реагирования на него". Всемирная организация здравоохранения . 19 сентября 2022 г. Получено 13 июня 2024 г.
- ^ «Вакцинация домашней птицы против высокопатогенного птичьего гриппа — Доступные вакцины и стратегии вакцинации». efsa.europa.eu . 2023-10-10 . Получено 2024-05-09 .
- ^ "Создание вируса-кандидата на вакцину (CVV) для вируса HPAI (птичьего гриппа)". Центры США по контролю и профилактике заболеваний (CDC) . 2024-06-03 . Получено 2024-06-15 .
- ^ "Вакцины от пандемического гриппа". Европейское агентство по лекарственным средствам . Получено 2024-06-15 .
- ^ Keown A (4 февраля 2020 г.). «FDA одобряет препарат Audenz компании Seqirus в качестве вакцины против потенциальной пандемии гриппа». BioSpace . Архивировано из оригинала 5 февраля 2020 г. Получено 5 февраля 2020 г.
- ^ "Audenz". Управление по контролю за продуктами и лекарствами США (FDA). 31 января 2020 г. STN: 125692. Архивировано из оригинала 6 августа 2020 г. Получено 5 февраля 2020 г.
 В данной статье использован текст из этого источника, находящегося в общественном достоянии .
В данной статье использован текст из этого источника, находящегося в общественном достоянии . - ^ Zheng D, Gao F, Zhao C, Ding Y, Cao Y, Yang T и др. (2018-09-14). «Сравнительная эффективность вакцин H7N9 у здоровых людей». Human Vaccines & Immunotherapeutics . 15 (1): 80–90 . doi :10.1080/21645515.2018.1515454. PMC 6363152. PMID 30148691 .
- ^ "Создание вируса-кандидата на вакцину (CVV) для вируса HPAI (птичьего гриппа)". Центры США по контролю и профилактике заболеваний (CDC) . 2024-06-03 . Получено 2024-06-22 .
- ^ ab "Zoonotic Influenza Vaccine Seqirus EPAR". Европейское агентство по лекарственным средствам (EMA) . 9 октября 2023 г. Получено 26 сентября 2024 г.
- ^ Poovorawan Y, Pyungporn S, Prachayangprecha S, Makkoch J (июль 2013 г.). «Глобальное оповещение об инфекции вируса птичьего гриппа: от H5N1 до H7N9». Патогены и глобальное здравоохранение . 107 (5): 217– 223. doi :10.1179/2047773213Y.0000000103. PMC 4001451. PMID 23916331 .
- ^ "1880-1959 Основные моменты в истории птичьего гриппа (Bird Flu) Timeline". Центры по контролю и профилактике заболеваний . 2024-06-10 . Получено 2024-07-14 .
- ^ Weston P (2024-03-26). «Осторожный оптимизм», поскольку пингвины дали положительный результат на птичий грипп, но не проявили никаких симптомов». The Guardian . ISSN 0261-3077 . Получено 2024-07-14 .
- ^ Sencer DJ (2024). "Вспышка в Гонконге, 1997 · Грипп: сложный вирус/сложная история · Цифровые экспозиции музея CDC". Музей CDC . Получено 2024-07-14 .
- ^ "Рекомендации по защите работников и использованию средств индивидуальной защиты (СИЗ) для снижения воздействия высокопатогенных вирусов птичьего гриппа A H5: Птичий грипп (грипп)". Центры по контролю и профилактике заболеваний . Получено 25 июля 2015 г.
- ^ Адитама Т.Ю., Самаан Г., Кусриастути Р., Сампурно О.Д., Пурба В., Сантосо Х. и др. (04.01.2012). «Передача птичьего гриппа H5N1 в домашних хозяйствах, Индонезия». ПЛОС ОДИН . 7 (1): e29971. Бибкод : 2012PLoSO...729971A. дои : 10.1371/journal.pone.0029971 . ПМК 3251608 . ПМИД 22238686.
- ^ "Вирус птичьего гриппа A(H5N1)". www.who.int . Получено 2024-05-28 .
- ^ Li FC, Choi BC, Sly T, Pak AW (июнь 2008 г.). «Определение реального уровня летальности птичьего гриппа H5N1». J Epidemiol Community Health . 62 (6): 555– 9. doi :10.1136/jech.2007.064030. PMID 18477756. S2CID 34200426.
- ^ ab "Информационный листок по A(H7N9)". Европейский центр профилактики и контроля заболеваний . 2017-06-15 . Получено 2024-07-15 .
- ^ Li Q, Zhou L, Zhou M, Chen Z, Li F, Wu H и др. (24 апреля 2013 г.). «Предварительный отчет: эпидемиология вспышки птичьего гриппа A (H7N9) в Китае». New England Journal of Medicine . 370 (6): 520– 532. doi :10.1056/NEJMoa1304617. PMC 6652192. PMID 23614499 .
- ^ abcd "Оценка риска птичьего гриппа A(H7N9) – восьмое обновление". Агентство безопасности здравоохранения Великобритании . 8 января 2020 г. Получено 15 июля 2024 г.
- ^ ab Liu Y, Chen Y, Yang Z, Lin Y, Fu S, Chen J, et al. (Июнь 2024 г.). «Эволюция и антигенная дифференциация вируса птичьего гриппа A(H7N9), Китай». Emerging Infectious Diseases . 30 (6): 1218– 1222. doi :10.3201/eid3006.230530. ISSN 1080-6040. PMC 11138980. PMID 38640498 .
- ^ "Вирус птичьего гриппа A(H7N9)". Продовольственная и сельскохозяйственная организация Объединенных Наций . 1 июня 2022 г. Получено 2024-07-15 .
- ^ CDC (2024-06-03). "2010-2019 Основные моменты в истории птичьего гриппа (Bird Flu) Хронология". Птичий грипп (Bird Flu) . Получено 2024-07-16 .
- ^ "USGS National Wildlife Health Center – Avian Influenza Wildlife Chart". Архивировано из оригинала 2018-02-06 . Получено 2010-10-06 .
- ^ Thacker E, Janke B (февраль 2008 г.). «Вирус свиного гриппа: зоонозный потенциал и стратегии вакцинации для контроля птичьего и свиного гриппа». Журнал инфекционных заболеваний . 197 (Приложение 1): S19 – S24 . doi : 10.1086/524988 . PMID 18269323.
- ^ Томас П. «Птичий грипп распространяется на крупный рогатый скот, вызывая страх на фермах». WSJ . Архивировано из оригинала 2024-04-04 . Получено 2024-04-04 .
- ^ Burrough E, Magstadt D, Main R (29 апреля 2024 г.). "Высокопатогенная инфекция вируса птичьего гриппа A(H5N1) Clade 2.3.4.4b у домашнего молочного скота и кошек, США, 2024 г.". Emerging Infectious Diseases . 30 (7): 1335– 1343. doi :10.3201/eid3007.240508. PMC 11210653 . PMID 38683888. Архивировано из оригинала 29 апреля 2024 г. Получено 30 апреля 2024 г.
- ^ Caserta L, Frye E, Butt S, Dimitrov K, Diel D (25 июля 2024 г.). "Распространение высокопатогенного вируса птичьего гриппа H5N1 на молочный скот". Nature . doi : 10.1038/s41586-024-07849-4 . PMC 11485258 . Получено 27 июля 2024 г. .
- ^ Schnirring L (24 мая 2024 г.). «Вирусы птичьего гриппа H5N1 могут сохраняться на поверхностях доильного оборудования». Университет Миннесоты . CIDRAP. Архивировано из оригинала 23 мая 2024 г. Получено 24 мая 2024 г.
- ^ Goodman B (2024-10-08). «Поскольку вспышка птичьего гриппа распространяется в Калифорнии, молочные фермы сообщают, что ситуация хуже, чем они ожидали». CNN . Получено 2024-10-10 .
- ^ Mellis AM (2024). «Серологическое подтверждение недавнего заражения высокопатогенным вирусом птичьего гриппа A(H5) среди работников молочной промышленности — Мичиган и Колорадо, июнь–август 2024 г.». MMWR. Еженедельный отчет о заболеваемости и смертности . 73. doi : 10.15585/mmwr.mm7344a3. ISSN 0149-2195. PMC 11542770 .
- ^ Lee CT (28 июля 2017 г.). «Вспышка гриппа A(H7N2) среди кошек в приюте для животных с передачей от кошки к человеку — Нью-Йорк, 2016 г.». academic.oup.com . Получено 16 мая 2024 г.
- ^ Thiry E, Addie, Diane, Belák, Sándor, Boucraut-Baralon, Corine, Egberink, Herman, Frymus, Tadeusz, et al. (1 июля 2009 г.). "H5N1 avian influenza in cats. Руководство ABCD по профилактике и лечению". Journal of Feline Medicine & Surgery . 11 (7): 615– 618. doi :10.1016/j.jfms.2009.05.011. PMC 7128855. PMID 19481042 .
- ^ Маршалл Дж., Хартманн К. (1 августа 2008 г.). «Инфекции птичьего гриппа A H5N1 у кошек». Журнал Feline Medicine & Surgery . 10 (4): 359– 365. doi :10.1016/j.jfms.2008.03.005. PMC 10832898. PMID 18619884. S2CID 29347001 .
- ^ «Птичий и пандемический грипп: глобальный ответ». Группа действий по борьбе с птичьим гриппом, Государственный департамент США. Октябрь 2008 г.
- ^ Хамейри С. (2014). «Птичий грипп, «вирусный суверенитет» и политика безопасности здравоохранения в Индонезии». The Pacific Review . 27 (3): 333–356 . doi :10.1080/09512748.2014.909523. S2CID 154302060.
- ^ abc Porter N (2012). «Рискованные зоографии: ограничения места в управлении птичьим гриппом». Environmental Humanities . 1 (1): 103– 121. doi : 10.1215/22011919-3609994 .
- ^ abc Олдерс Р., Авуни Дж. А., Баньол Б., Фаррелл П., де Хаан Н. (2014). «Влияние птичьего гриппа на сельское птицеводство во всем мире». ЭкоЗдоровье . 11 (1): 63–72 . doi :10.1007/s10393-013-0867-x. PMID 24136383. S2CID 6701416.
- ^ Портер Н. (2013). «Биоэнергетика птичьего гриппа: стратегии многовидового сосуществования во Вьетнаме». Американский этнолог . 40 (1): 132– 148. doi :10.1111/amet.12010.
- ^ ab Маклеод А., Морган Н., Пракаш А., Хинрихс Дж. (2005). Экономические и социальные последствия птичьего гриппа. Продовольственная и сельскохозяйственная организация (отчет).
- ^ https://www.silive.com/politics/2025/01/in-warning-to-feds-schumer-says-keep-funding-bird-flu-fight-or-else-grocery-costs-could-rise .html
Дальнейшее чтение
- Orent W (20 февраля 2006 г.). «Наука о птичьем гриппе. Ответы на девять часто задаваемых вопросов». Discover Magazine Health & Medicine . стр. 59–61 .
- Haugan S, Bjornson W, ред. (2009). Птичий грипп: этиология, патогенез и вмешательства . Hauppauge, Нью-Йорк: Nova Science Publishers. ISBN 978-1607418467.
- Сигер Р.М., Хагерман А.Д., Джонсон К.К., Пенделл Д.Л., Марш Т.Л. (июль 2021 г.). «Когда домашняя птица уходит на больничный: расходы на ответные меры на эпидемию высокопатогенного птичьего гриппа в США в 2014–2015 гг.». Продовольственная политика . 102 : 102068. doi : 10.1016/j.foodpol.2021.102068.
Внешние ссылки
Всемирная организация здравоохранения (ВОЗ)
- Ресурс ВОЗ по птичьему гриппу
- Информационный бюллетень Всемирной организации здравоохранения о птичьем гриппе за 2006 год
- Углубленный анализ птичьего гриппа. Симптомы и углубленный анализ птичьего гриппа
Продовольственная и сельскохозяйственная организация ООН (ФАО)
- Портал FAO по птичьему гриппу. Информационные ресурсы, анимация, видео, фотографии
- Карточка заболевания птичьим гриппом ФАО. Архивировано 16.03.2005 на Wayback Machine
Всемирная организация охраны здоровья животных (МЭБ)
- Текущее состояние HPAI во всем мире в OIE. Интерфейс WAHID – Всемирная база данных информации о здоровье животных OIE
- Карточка болезни
- Ресурс по птичьему гриппу. Автор: д-р Нати Элкин – Атласы, вакцины и информация
Соединенные Штаты
- PandemicFlu.Gov. Информация правительства США о птичьем и пандемическом гриппе
- Обзор CIDRAP по птичьему гриппу. «Птичий грипп: аспекты сельского хозяйства и дикой природы»
- Ответ США на птичий грипп. Агентство США по международному развитию (USAID)
- Исследования и рекомендации по птичьему гриппу. Национальный институт охраны труда и здоровья
- База данных исследований гриппа. База данных последовательностей вируса гриппа и сопутствующей информации.
- Профиль вида – птичий грипп (Orthomyxoviridae Influenza Type A, subtype H5N1), Национальный центр информации об инвазивных видах, Национальная сельскохозяйственная библиотека США . Перечисляет общую информацию и ресурсы по птичьему гриппу
- Стратегическая коммуникация в области здравоохранения для профилактики птичьего и пандемического гриппа [узурпировано] . Центр коммуникационных программ Школы общественного здравоохранения имени Блумберга при Университете Джонса Хопкинса Глобальная программа по птичьему и пандемическому гриппу
- Предупреждение NIOSH: Защита работников птицеводства от птичьего гриппа. Рекомендации CDC/NIOSH для работников птицеводства
Европа
- Европейская комиссия. Меры по контролю птичьего гриппа
- Птичий грипп: вопросы и ответы. Европейский центр профилактики и контроля заболеваний – Официальный сайт
- FluTrop: Исследование птичьего гриппа в тропических странах. Французский центр сельскохозяйственных исследований для развивающихся стран (CIRAD), веб-сайт по птичьему гриппу

