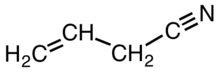
Аллилцианид
 | |
 | |
| Имена | |
|---|---|
| Предпочтительное название ИЮПАК Бут-3-еннитрил | |
| Идентификаторы | |
3D модель ( JSmol ) |
|
| 605352 | |
| ЧЭБИ |
|
| ChemSpider |
|
| Информационная карта ECHA | 100.003.366 |
| Номер ЕС |
|
CID PubChem |
|
| УНИИ | |
Панель инструментов CompTox ( EPA ) |
|
| |
| |
| Характеристики | |
| С4Н5Н | |
| Молярная масса | 67,091 г·моль −1 |
| Появление | бесцветная жидкость |
| Плотность | 0,834 г/см 3 [1] |
| Температура плавления | −87 °C (−125 °F; 186 K) |
| Точка кипения | 116–121 °C (241–250 °F; 389–394 K) [1] |
| Опасности | |
| Охрана труда и техника безопасности (OHS/OSH): | |
Основные опасности | Легковоспламеняющийся, ядовитый, раздражает кожу и глаза. |
Опасности проглатывания | Токсично при проглатывании. |
Опасности при вдыхании | Может быть смертельным при вдыхании. Вызывает раздражение дыхательных путей. |
Опасность для глаз | Вызывает раздражение глаз. |
Опасности для кожи | Вызывает раздражение кожи. |
| Маркировка СГС : | |
  | |
| Опасность | |
| Х226 , Х301 , Х311 , Х312 , Х315 , Х319 | |
| П261 , П280 , П301+П310 , П305+П351+П338 , П311 | |
| NFPA 704 (огненный алмаз) | |
| точка возгорания | 24 °C (75 °F; 297 К) [1] |
| 455 °C (851 °F; 728 К) [1] | |
| Паспорт безопасности (SDS) | ПБМ |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |
Аллилцианид — это органическое соединение с формулой CH2CHCH2CN . Как и другие малые алкилнитрилы, аллилцианид бесцветен и растворим в органических растворителях. Аллилцианид встречается в природе как антифидант и используется в качестве сшивающего агента в некоторых полимерах. [2]
Синтез
Аллилцианид получают реакцией аллилацетата с цианистым водородом. [2]
Лабораторный способ получения аллилцианида включает обработку аллилбромида цианидом меди (I) . [3]
- CH 2 =CHCH 2 Br + CuCN → CH 2 =CHCH 2 CN + CuBr
Для этой реакции можно использовать и другие аллилгалогениды, включая аллилйодид, как это сделали А. Ринне и Б. Толленс в 1871 году, где йодид является лучшей уходящей группой, чем его эквивалент бромида, и, следовательно, увеличивает выход. [4]
Природные явления
Аллилцианид был открыт в 1863 году Х. Виллом и В. Кернером; в 1863 году они обнаружили, что это соединение присутствует в горчичном масле . [5] О первом синтезе аллилцианида сообщил А. Клаус в 1864 году. [6]
Аллилцианид вырабатывается в крестоцветных овощах мирозиназой , ферментом, который гидролизует глюкозинолаты с образованием нитрилов и других продуктов. [7] Мирозиназа активируется L-аскорбиновой кислотой (витамином С) под влиянием pH, [8] и более высокая активность мирозиназы была показана в поврежденных листьях капусты, в то время как ее активность снижается при приготовлении листьев, хотя глюкозинолаты затем могут быть преобразованы в аллилцианид микрофлорой в кишечнике. [9] Поскольку крестоцветные овощи, такие как капуста, брокколи, цветная капуста и проростки, являются частью рациона человека, аллилцианид обычно потребляется перорально. Показано, что нормальная доза аллилцианида, содержащаяся в еде, намного ниже доз, используемых в исследованиях на животных. [7] Ежедневный уровень, при котором были продемонстрированы поведенческие эффекты, составляет 500 мкг/кг веса тела, тогда как суточное потребление человеком составляет 0,12 мкг/кг. Хотя зависимость «доза-реакция» еще предстоит изучить, считается, что цианистый аллил не обладает нейротоксическим действием при употреблении в овощах.
Приложения
Аллилцианид может использоваться в качестве добавки в электролитах на основе пропиленкарбоната для графитовых анодов, предотвращая отслоение анода из-за образования пленки. Предполагается, что лежащий в основе механизм — это механизм восстановительной полимеризации. [10]
Нейротоксичность
Исследования, проведенные на крысах, показали, что аллилцианид вызывает потерю волосковых клеток в слуховой системе и нарушение роговицы. [11] Это же исследование также показало, что активность крыс при вставании на задние лапы была снижена при пероральном приеме аллилцианида. Он имеет эти нейротоксические симптомы, общие с другими алифатическими мононитрилами, такими как 2-бутеннитрил и 3,3'-иминопропионитрил. Было также показано, что аллилцианид вызывает отек аксонов. [12] Исследования, проведенные на мышах, показали, что однократная (хотя и довольно высокая) доза аллилцианида может вызвать постоянные изменения поведения. [13] Эти изменения включают подергивание головы, повышенную двигательную активность и кружение. Кроме того, было показано, что эти мыши страдают от сокращений нейронов, что может привести к гибели клеток. Овцы гораздо более устойчивы к токсическому воздействию аллилцианида, чем крысы. Исследования показывают, что эта детоксикация происходит из-за предварительного переваривания в рубце . [14]
Токсикокинетика
Известно, что аллилцианид метаболизируется в печени ферментной системой цитохрома P-450 (в основном CYP2E1) в цианид. [15] Абсорбция и распределение аллилцианида у крыс происходит необычайно быстро. Самые высокие концентрации аллилцианида были измерены в тканях желудка и содержимом желудка из-за того, что желудок является основным местом абсорбции после перорального приема. Следующие по величине уровни концентрации были обнаружены в костном мозге с пиком концентрации между 0 и 3 часами после приема. Печень, почки, селезенка и легкие также накапливали аллилцианид в течение 48 часов. Самая высокая концентрация в почках наблюдалась между 3 и 6 часами после приема. Это наблюдение указывает на быстрое выведение аллилцианида. Основным путем детоксикации является преобразование цианида в тиоцианат. [16] Основные пути выведения — через мочу и выдыхаемый воздух.
Системы серотонина и дофамина, как полагают, участвуют в поведенческих аномалиях, вызванных аллилцианидом. Лечение антагонистами серотонина и дофамина привело к уменьшению поведенческих аномалий. [17] Атаксия, дрожь, судороги, диарея, слюнотечение, слезотечение и нерегулярное дыхание — известные эффекты, которые вызываются пероральным приемом аллилцианида.
Ссылки
- ^ abcd ПБМ
- ^ аб Людгер Крелинг; Юрген Крей; Джеральд Джейкобсон; Иоганн Гролиг; Леопольд Микше (2002). «Аллиловые соединения». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. дои : 10.1002/14356007.a01_425. ISBN 9783527303854.
- ^ JV Supniewski; PL Salzberg (1928). "Аллилцианид". Org. Synth . 8 : 4. doi :10.15227/orgsyn.008.0004.
- ^ А. Ринне, Б. Толленс: «Ueber das Allylcyanür oder Crotonitril», в: Юстус Либигс Annalen der Chemie, 1871, 159 (1), S. 105–109; doi:10.1002/jlac.18711590110
- ^ К. Померанц: «Ueber Allylcyanid und Allylsenföl», в: Justus Liebigs Annalen der Chemie, 1906, 351 (1–3), стр. 354–362: doi: 10.1002/jlac.19073510127.
- ^ А. Клаус: «Ueber Crotonsäure», в: Justus Liebigs Annalen der Chemie, 1864, 131 (1), стр. 58–66; doi: 10.1002/jlac.18641310106
- ^ ab H. Tanii и др. Аллилнитрил: образование из крестоцветных овощей и поведенческие эффекты у мышей при повторном воздействии / Пищевая и химическая токсикология, 42, (2004), 453-458
- ^ LG West и др. Производство аллилизотиоцианата и аллилцианида в экстрактах листьев капусты без клеток, измельченной капусте и салате из капусты коул-слоу / J. Agric. Food Chem. Т. 25, № 6, (1997), 1234-1238
- ^ C. Krul и др. Метаболизм синигрина (2-пропенилглюкозинолата) микрофлорой толстой кишки человека в динамической модели толстой кишки in vitro / Канцерогенез, т. 24, № 6, (2002), 1009-1016
- ^ Л. Чжан и др. Аллилцианид как новая функциональная добавка в электролите на основе пропиленкарбоната для литий-ионных аккумуляторов Iconics Август 2013, Том 19, Выпуск 8, стр. 1099-1103
- ^ Э. Бальбуэна, Х. Льоренс Поведенческие нарушения и сенсорная патология после воздействия аллилнитрила на крыс / Исследования мозга 904 (2001) 298-306
- ^ C. Soler-Martín et al. Бутеннитрилы имеют низкий аксонопатический потенциал у крыс / Toxicology Letters 200 (2011) 187-193
- ^ Сяо-пин Занг и др. Поведенческие аномалии и апоптотические изменения в нейронах мозга мышей после однократного введения аллилнитрила / Arch Toxicol 73 (1999) 22-32
- ^ Дункан, А. Дж. и Милн, Дж. А. (1992), Микробная деградация аллилцианида в рубце как возможное объяснение толерантности овец к глюкозинолатам, полученным из капусты. J. Sci. Food Agric., 58: 15–19.
- ^ AE Ahmed и MYH Farooqui: Сравнительная токсичность алифатических нитрилов. Toxicol. Len. 12, 157-163 (1982)
- ^ E. Ahmed, MYH Farooqui и NM Tneff: Нитрилы. В:"Биотрансформация инородных соединений" (ред. MW Anders), стр. 485-510. Academic Press, Нью-Йорк, 1985.
- ^ H. Tanii, Y. Kurosaka, M. Hayashi и K. Hashimoto: Аллилнитрил: соединение, вызывающее длительную дискинезию у мышей после однократного введения. Exp. Neurol. 103, 64-67 (1989)

