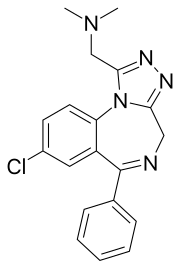
Адиназолам
 | |
 | |
| Клинические данные | |
|---|---|
| Торговые наименования | Дерацин |
| Пути введения | Оральный |
| код АТС |
|
| Правовой статус | |
| Правовой статус |
|
| Фармакокинетические данные | |
| Метаболизм | Печеночный |
| Метаболиты | N-десметиладиназолам N, N-дидесметиладиназолам эстазолам альфа-гидрокси-алпразолам |
| Период полувыведения | < 3 часов |
| Выделение | Почечный |
| Идентификаторы | |
| |
| Номер CAS | |
| CID PubChem |
|
| DrugBank | |
| ChemSpider | |
| УНИИ |
|
| КЕГГ | |
| ЧЭБИ | |
| ChEMBL | |
| Панель инструментов CompTox ( EPA ) |
|
| Химические и физические данные | |
| Формула | C19H18ClN5 |
| Молярная масса | 351,84 г·моль −1 |
| 3D модель ( JSmol ) |
|
| Температура плавления | 171–172,5 °C (339,8–342,5 °F) |
| Растворимость в воде | ЛогП: 4.16 Растворим в дихлорметане и метаноле. Соль (мезилат), растворимая в воде мг/мл (20 °C) |
| |
| (проверять) | |
Адиназолам [1] (продается под торговой маркой Deracyn ) — транквилизатор класса триазолобензодиазепинов (TBZD), которые представляют собой бензодиазепины (BZD), соединенные с триазольным кольцом. Он обладает анксиолитическими , [2] противосудорожными , седативными и антидепрессантными [3] [4] свойствами. Адиназолам был разработан Джексоном Б. Хестером, который стремился усилить антидепрессантные свойства алпразолама , который он также разработал. [5] Адиназолам никогда не был одобрен FDA и никогда не был доступен на открытом рынке; однако он продавался как дизайнерский наркотик . [6]
Химическая информация
Реактивность
Адиназолам содержит несколько реакционноспособных частей в своей структуре. Первая — это диметиламин, который является слабощелочным с pKa 6,30, что делает более 5% соединения протонированным при физиологическом pH. Третичный амин также может быть важен для связывания белка со способностью образовывать водородные мостики и также, вероятно, является целью для метаболизма посредством деметилирования. Диметиламин также лабилен для окислительного разложения, что приводит к потере одной метильной группы, образуя N- десметиладиназолам. Потеря всего диметилметанамина также возможна посредством окислительного разложения, образуя эстазолам. Вторая реакционноспособная группа — это азот в 4-м положении. С pKa 5,09 он протонируется только при уровнях pH ниже физиологического. После протонирования группа лабильна для гидратации, что приводит к раскрытию диазепинового кольца. После этого этиламин расщепляется или кольцо снова замыкается, что приводит к другим структурам.
Синтез
Один из логичных способов синтеза адиназолама — это реакция с предшественниками бензодиазепина. Один из путей, которому следуют Хестер и др. , начинается с 7-хлор-2-гидразинил-5-фенил-3H-бензо[e][1,4]диазепина. Сначала N -фталимидоил-β-аланин образуется in situ из β-аланина с фталевым ангидридом. Раствор охлаждают и обрабатывают карбонилдиимидазолом. Затем к раствору добавляют 7-хлор-2-гидразинил-5-фенил-3H-бензо[e][1,4]диазепин и оставляют реагировать при комнатной температуре в течение 18 ч. После процедуры был получен сольват этилацетата, в результате чего был получен 2-(2-(8-хлор-6-фенил-4H-бензо[f][1,2,4]триазоло[4,3-a][1,4]диазепин-1-ил)этил)изоиндолин-1,3-дион. Последующая обработка 2-(2-(8-хлор-6-фенил-4H-бензо[f][1,2,4]триазоло[4,3-a][1,4]диазепин-1-ил)этил)изоиндолин-1,3-диона раствором 88% муравьиной кислоты и 37% водн. формальдегид (3:2 моль/моль) при 100 °C в течение 1 ч в атмосфере азота приводит к образованию 2-(2-(4-(2-бензоил-4-хлорфенил)-5-(диметиламино)метил)-4H-1,2,4-триазол-3-ил)этил)изоиндолин-1,3-диона. Диазепиновое кольцо расщепляется на этом этапе, и фталат переносится. На последнем этапе диазепиновое кольцо формируется обратно с использованием гидразингидрата при 70 °C в течение 1 ч 30 мин в атмосфере азота, образуя адиназолам. [7]
Другой путь синтеза адиназолама — через эстазолам, как это сделали Галл и др. Во время синтеза бис-(диметиламино)метан растворяют в ДМФА и охлаждают до 0 °C. Затем раствор обрабатывают ацетилхлоридом в ДМФА, образуя соль хлорида диметил(метилен)аммония. Затем к раствору добавляют K2CO3 , а затем раствор эстазолама в ДМФА. Затем смесь нагревают до 60 ° C в течение 3 часов, что приводит к получению адиназолама после обработки. [8]
Использование и цель
This section needs additional citations for verification. (March 2024) |
Адиназолам в первую очередь используется из-за его анксиолитических свойств. Как упоминалось во Введении и будет более подробно объяснено в Молекулярном механизме действия, адиназолам является производным бензодиазепина, он действует на рецепторы ГАМК в центральной нервной системе, способствуя ингибирующему эффекту ГАМК. Это приводит к успокаивающему эффекту, что делает его пригодным для лечения тревожных расстройств, панических расстройств и в качестве антидепрессантов. [9]
В статье Амстердама и др. [10] было проведено исследование с участием 43 амбулаторных пациентов, соответствующих критериям диагностики большой депрессии. Они были рандомизированы для приема либо адиназолама, либо имипрамина. Дозы лекарств корректировались на основе переносимости и потребностей, с еженедельными клиническими оценками и рейтингами с использованием различных шкал.
Было обнаружено, что адиназолам был столь же эффективен, как имипрамин, при лечении тяжелой депрессии, с аналогичной эффективностью при меланхолической депрессии. Адиназолам имел некоторые побочные эффекты, такие как сонливость/седация, сухость во рту, запор, нечеткость зрения, тошнота/рвота/диарея, нервозность и головные боли. Однако все они показали меньше побочных эффектов, чем имипрамин, за исключением сонливости/седации. Исследование предполагает, что адиназолам может быть многообещающей альтернативой с потенциальными терапевтическими преимуществами, но необходимы дальнейшие исследования для уточнения его клинического профиля и безопасности.
Доступность
Адиназолам был разработан и испытан как антидепрессант в 1980-х и 1990-х годах, но после первоначального периода оценки его исследования и испытания пошли на спад. Существует ограниченная информация относительно дальнейшего изучения его фармацевтических свойств. Отклонение адиназолама FDA в 1990-х годах привело к его отсутствию в основном медицинском использовании.
После этого отклонения адиназолам вновь появился около 2015 года, и его стали использовать на рынке как дизайнерский препарат. Это изменение статуса и функции поднимает вопросы о его применении в немедицинском контексте. Дизайнерские препараты часто представляют собой проблемы для регулирующих органов из-за их измененного химического состава и подверженности неправильному использованию.
Побочные эффекты
При использовании адиназолама у людей могут возникнуть различные побочные эффекты, как в краткосрочной, так и в долгосрочной перспективе. Первоначально распространенные побочные эффекты в краткосрочной перспективе могут включать сонливость, седацию и легкие когнитивные нарушения. [10] [11]
Передозировка может вызвать мышечную слабость , атаксию , дизартрию и, особенно у детей, парадоксальное возбуждение, а также снижение рефлексов, спутанность сознания и кому, которые могут возникнуть в более тяжелых случаях. [12]
Исследование на людях, сравнивающее субъективные эффекты и потенциал злоупотребления адиназоламом (30 мг и 50 мг) с диазепамом , лоразепамом и плацебо, показало, что адиназолам вызывает наибольшую «психическую и физическую седацию» и самые большие «психические неприятные ощущения». [13]
В долгосрочной перспективе длительное применение адиназолама может привести к развитию толерантности, когда для достижения тех же терапевтических эффектов требуются более высокие дозы. Следовательно, увеличение доз может повысить риск побочных эффектов и потенциальных осложнений. Длительное применение адиназолама также несет в себе возможность зависимости, когда люди могут стать психологически и физически зависимыми от лекарства для управления симптомами тревоги. [14] [15] Зависимость создает значительные проблемы, поскольку быстрое снижение дозы может вызвать симптомы отмены, начиная от рикошетной тревоги и бессонницы и заканчивая более серьезными проявлениями, такими как судороги. Кроме того, длительное применение адиназолама может способствовать когнитивным нарушениям, влияя на память, концентрацию и общую когнитивную функцию. [16] [11]
Фармакодинамика и фармакокинетика
Адиназолам является пролекарством для метаболита N-деметил-адиназолама (NDMAD), поскольку он является основным активным метаболитом у людей. [17] Однако адиназолам и его другие метаболиты ди-N-деметил-адиназолам, ⍺-гидрокси-алпразолам и эстразолам сами по себе являются активными соединениями. [17] Они действуют на центральную нервную систему (ЦНС), связываясь положительно аллостерически с (центральными) бензодиазепиновыми рецепторами (BzR), которые являются подмножеством рецептора ГАМК A. [9] [18] [19] Адиназолам имеет высокое сродство к рецептору ГАМК A , однако его метаболиты в 20–40 раз более эффективны в ингибировании связывания [ 3 H]флунитразепама (используется радиоактивная метка). [17]
Рецептор (ГАМК) А реагирует на высвобождение γ-аминомасляной кислоты (ГАМК), которая является основным тормозным нейромедиатором в мозге и играет важную роль в модуляции активности нейронов. [9] Рецептор ГАМК А представляет собой белковый комплекс, расположенный в синапсах; этот белок является лиганд-управляемым ионным каналом (ионотропным рецептором), который проводит ионы хлора через мембраны нейронных клеток. [9] Комплекс состоит из пяти субъединиц: двух ⍺, двух β и одной γ. ГАМК связывается с интерфейсом между субъединицами ⍺ и β (2 участка связывания), тогда как бензодиазепины связываются с интерфейсом субъединиц ⍺ и γ, однако связывание бензодиазепина возможно только при наличии остатка гистидина в разновидностях ⍺ 1 , ⍺ 2 , ⍺ 3 и ⍺ 5 , которые называются бензодиазепиновыми рецепторами. [9] [20] Связывание адиназолама или других бензодиазепинов действует как агонист, вызывая конформационное изменение в бензодиазепиновом рецепторе, что увеличивает сродство к ГАМК, в свою очередь снижая нейронную активность. Это снижение нейронной активности объясняет наблюдаемые клинические эффекты. Различные фармакологические свойства бензодиазепинов можно отнести к разнообразию субъединиц ⍺. Субъединица ⍺ 1 необходима для седативного, антероградного амнестического и противосудорожного действия; субъединицы ⍺ 2 для анксиолитического эффекта и миорелаксирующего действия опосредуются рецепторами ГАМК A, содержащими субъединицы ⍺ 2 , ⍺ 3 и ⍺ 5. [20]
Возбуждение нейрона происходит, когда его мембранный потенциал, который отрицателен в состоянии покоя, увеличивается или деполяризуется до тех пор, пока не будет достигнут порог или потенциал действия. Когда этот потенциал достигается, открывается потенциалзависимый натриевый канал, позволяющий натрию устремляться в клетку. Связывание ГАМК с рецептором ГАМК-А предотвращает это, пропуская ионы хлора в клетку, что снижает или поляризует мембранный потенциал. [21] [22] Связывание адиназолама или других бензодиазепинов увеличивает приток ионов хлора и, следовательно, увеличивает поляризацию мембранного потенциала. [9] [18] [19]
Метаболизм
В выпуске журнала The Journal of Pharmacy and Pharmacology за август 1984 г. сообщалось, что адиназолам имеет активные метаболиты . [17] Основным метаболитом является N -десметиладиназолам. [23] NDMAD имеет примерно в 25 раз более высокое сродство к бензодиазепиновым рецепторам по сравнению с его предшественником, что объясняет бензодиазепиноподобные эффекты после перорального приема. [1] Многочисленные N -деалкилирования приводят к удалению боковой цепи диметиламинометила, что приводит к разнице в его силе действия. [23] Два других метаболита — альфа-гидроксиалпразолам и эстазолам . [24] В выпуске того же журнала за август 1986 г. Сети, Фрэнсис и Дэй сообщили, что проадифен ингибирует образование N-десметиладиназолама. [25]
Адиназолам после приема внутрь в первую очередь метаболизируется путем N-деалкилирования печеночным путем и энтеральным путем. Адиназолам может подвергаться энтеральной и печеночной конверсии в свой активный метаболит после перорального приема, поскольку этот препарат является субстратом CYP3A4, хотя энтеральный метаболизм играет важную роль перед печеночным метаболизмом. CYP3A4 — это фермент в кишечнике и печени, который играет решающую роль в метаболизме лекарств. Поэтому изучение энтерального метаболического пути адиназолама также важно для понимания общей фармакологии этого вещества. [2] [6] [24] [26]
Согласно нескольким исследованиям, основными метаболитами адиназолама, также известными как метаболиты фазы 1, которые включают окислительные реакции, катализируемые ферментами цитохрома P450, такими как CYP3A4, являются моно-N-десметиладиназолам (активный метаболит) и (N, N-ди)десметиладиназолам. Моно-N-десметиладиназолам образуется в результате трансформации адиназолама, где метильная группа, присоединенная к азоту, удаляется путем N-деалкилирования, и этот активный метаболит далее метаболизируется в десметиладиназолам, где другая метильная группа удаляется и заменяется атомом водорода. Дезаминирование десметиладиназолама приводит к образованию промежуточного метаболита, который подвергается альфа-гидроксилированию с образованием альфа-гидрокси-алпразолама или расщеплению боковой цепи с образованием эстазолама, которые являются второстепенными метаболитами. [2] [24] [26] [27] [6] [17] [28] Метаболизм адиназолама и его метаболитов.
Смотрите также
Ссылки
- ^ ab FR 2248050, «4,5-дигидро-4h-s-триазоло (4,3-a) (1,4) бензодиазепин — депрессанты центральной нервной системы, противосудорожные, противоагрессивные и соматорелаксирующие средства», выдан 21 января 1977 г., передан Ciba-Geigy AG и Novartis AG.
- ^ abc Venkatakrishnan K, von Moltke LL, Duan SX, Fleishaker JC, Shader RI, Greenblatt DJ (март 1998). "Кинетическая характеристика и идентификация ферментов, ответственных за печеночную биотрансформацию адиназолама и N-десметиладиназолама у человека". Журнал фармации и фармакологии . 50 (3): 265– 274. doi : 10.1111/j.2042-7158.1998.tb06859.x . PMID 9600717. S2CID 33656240.
- ^ Даннер Д., Майерс Дж., Хан А., Эйвери Д., Ишики Д., Пайк Р. (июнь 1987 г.). «Адиназолам — новый антидепрессант: результаты плацебо-контролируемого двойного слепого исследования у амбулаторных пациентов с тяжелой депрессией». Журнал клинической психофармакологии . 7 (3): 170– 172. doi :10.1097/00004714-198706000-00010. PMID 3298327.
- ^ Lahti RA, Sethy VH, Barsuhn C, Hester JB (ноябрь 1983 г.). «Фармакологический профиль антидепрессанта адиназолама, триазолобензодиазепина». Neuropharmacology . 22 (11): 1277– 1282. doi :10.1016/0028-3908(83)90200-9. PMID 6320036. S2CID 667962.
- ^ "Discovers Award 2004" (PDF) . Специальные публикации . Pharmaceutical Research and Manufacturers of America. Апрель 2004 г. стр. 39. Архивировано из оригинала (PDF) 24 августа 2006 г. . Получено 18 августа 2006 г. .
- ^ abc Moosmann B, Bisel P, Franz F, Huppertz LM, Auwärter V (ноябрь 2016 г.). «Характеристика и in vitro фаза I микросомального метаболизма дизайнерских бензодиазепинов — обновление, включающее адиназолам, клонипразепам, фоназепам, 3-гидроксифеназепам, метизолам и нитразолам». Журнал масс-спектрометрии . 51 (11): 1080– 1089. Bibcode : 2016JMSp...51.1080M. doi : 10.1002/jms.3840. PMID 27535017.
- ^ Хестер Дж. Б., Рудзик АД., Фон Фойгтландер П. Ф. (апрель 1980 г.). «1-(Аминоалкил)-6-арил-4-Hs-триазоло[4,3-a][1,4]бензодиазепины с противотревожной и антидепрессивной активностью». Журнал медицинской химии . 23 (4): 392– 402. doi :10.1021/jm00178a009. PMID 6103958.
- ^ Gall M, Kamdar BV, Lipton MF, Chidester CG, Duchamp DJ (ноябрь 1988 г.). «Реакции Манниха гетероциклов с диметил(метилен)аммонийхлоридом: высоковыходное одностадийное превращение эстазолама в адиназолам». Журнал гетероциклической химии . 25 (6): 1649– 1661. doi :10.1002/jhet.5570250610. ISSN 0022-152X.
- ^ abcdef Seeman P (март 2009). «Компоненты глутамата и дофамина при шизофрении». Журнал психиатрии и нейронауки . 34 (2): 143– 149. doi : 10.4103/0973-1229.58825 . PMC 3043325 .
- ^ ab Amsterdam JD, Kaplan M, Potter L, Bloom L, Rickels K (апрель 1986 г.). «Адиназолам, новый триазолобензодиазепин, и имипрамин в лечении большого депрессивного расстройства». Психофармакология . 88 (4): 484– 488. doi :10.1007/BF00178511. PMID 3085137.
- ^ ab Linnoila M, Stapleton JM, Lister R, Moss H, Lane E, Granger A, et al. (апрель 1990 г.). «Влияние адиназолама и диазепама, отдельно и в сочетании с этанолом, на психомоторную и когнитивную деятельность и на реактивность автономной нервной системы у здоровых добровольцев». European Journal of Clinical Pharmacology . 38 (4): 371– 377. doi :10.1007/BF00315578. PMID 2344860.
- ^ "Адиназолам". DrugBank.
- ^ Bird M, Katz D, Orzack M, Friedman L, Dessain E, Beake B, et al. (1987). "Потенциал злоупотребления адиназоламом: сравнение с диазепамом, лоразепамом и плацебо" (PDF) . Исследовательская монография NIDA № 81. Архивировано из оригинала (PDF) 22.12.2016 . Получено 17.12.2015 .
- ^ Brunetti P, Giorgetti R, Tagliabracci A, Huestis MA, Busardò FP (июнь 2021 г.). «Дизайнерские бензодиазепины: обзор токсикологии и рисков для общественного здравоохранения». Pharmaceuticals . 14 (6): 560. doi : 10.3390/ph14060560 . PMC 8230725 . PMID 34208284.
- ^ Owen RT, Tyrer P (апрель 1983). «Зависимость от бензодиазепинов. Обзор доказательств». Drugs . 25 (4): 385–398 . doi :10.2165/00003495-198325040-00003. PMID 6133736.
- ^ Стюарт СА (2005). «Влияние бензодиазепинов на когнитивные функции». Журнал клинической психиатрии . 66 (Приложение 2): 9–13 . PMID 15762814.
- ^ abcde Sethy VH, Collins RJ, Daniels EG (август 1984). «Определение биологической активности адиназолама и его метаболитов». Журнал фармации и фармакологии . 36 (8): 546– 548. doi :10.1111/j.2042-7158.1984.tb04449.x. PMID 6148400. S2CID 21094654.
- ^ ab Tamama K, Lynch MJ (2019). «Новые появляющиеся наркотики, вызывающие злоупотребление». В Nader MA, Hurd YL (ред.). Расстройства, вызванные употреблением веществ . Справочник по экспериментальной фармакологии. Том 258. Cham: Springer International Publishing. стр. 463–502 . doi :10.1007/164_2019_260. ISBN 978-3-030-33678-3. PMID 31595417.
- ^ ab Hayhoe B, Lee-Davey J (июль 2018 г.). «Борьба со злоупотреблением бензодиазепинами». BMJ . 362 : k3208. doi :10.1136/bmj.k3208. PMC 6065205 . PMID 30054270.
- ^ ab Tan KR, Rudolph U, Lüscher C (апрель 2011 г.). «Пристрастие к бензодиазепинам: подтипы рецепторов ГАМК-А и зависимость». Trends in Neurosciences . 34 (4): 188– 197. doi :10.1016/j.tins.2011.01.004. PMC 4020178. PMID 21353710 .
- ^ Бен-Ари Ю, Хазипов Р, Лейнекугель X, Кайлард О, Гайарса Дж. Л. (ноябрь 1997 г.). «рецепторы GABAA, NMDA и AMPA: регулируемый процесс развития «ménage à trois»". Тенденции в нейронауках . 20 (11): 523– 529. doi :10.1016/S0166-2236(97)01147-8. PMID 9364667.
- ^ Taketo M, Yoshioka T (март 2000). «Изменение в развитии тока, опосредованного рецептором ГАМК(А) в гиппокампе крысы». Neuroscience . 96 (3): 507– 514. doi :10.1016/s0306-4522(99)00574-6. PMID 10717431.
- ^ ab Peng GW (август 1984). «Анализ адиназолама в плазме методом жидкостной хроматографии». Журнал фармацевтических наук . 73 (8): 1173– 1175. doi :10.1002/jps.2600730840. PMID 6491930.
- ^ abc Fraser AD, Isner AF, Bryan W (ноябрь–декабрь 1993 г.). «Скрининг мочи на адиназолам и его основные метаболиты с помощью анализов Emit dau и FPIA бензодиазепина с подтверждением с помощью ВЭЖХ». Журнал аналитической токсикологии . 17 (7): 427– 431. doi :10.1093/jat/17.7.427. PMID 8309217.
- ^ Sethy VH, Francis JW, Day JS (август 1986). «Влияние проадифена на метаболизм адиназолама». Журнал фармации и фармакологии . 38 (8): 631– 632. doi :10.1111/j.2042-7158.1986.tb03099.x. PMID 2876087. S2CID 9394686.
- ^ ab Fleishaker JC, Phillips JP, Smith TC, Smith RB (май 1989). «Многодозовая фармакокинетика и фармакодинамика адиназолама у пожилых субъектов». Pharmaceutical Research . 6 (5): 379– 386. doi :10.1023/A:1015975214070. PMID 2748528.
- ^ Аджир К, Смит М, Лин КМ, Флейшакер Дж. К., Чемберс Дж. Х., Андерсон Д. и др. (февраль 1997 г.). «Фармакокинетика и фармакодинамика адиназолама: многоэтнические сравнения». Психофармакология . 129 (3): 265– 270. doi :10.1007/s002130050189. PMID 9084065.
- ^ Wu D, Fu L (декабрь 2023 г.). «Последние результаты и достижения в обнаружении дизайнерских бензодиазепинов: краткий обзор». Архив Хирургии Рады и Токсикологии . 74 (4): 224–231 . doi :10.2478/aiht-2023-74-3771. PMC 10750316. PMID 38146763 .

