Нитрофенол
Нитрофенолы — это соединения формулы HOC 6 H 5−x (NO 2 ) x . Сопряженные основания называются нитрофенолятами. Нитрофенолы более кислотны, чем сам фенол . [1]
Мононитрофенолы
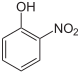 2-Нитрофенол ( о- ) | |
 3-Нитрофенол ( м- ) | |
 4-Нитрофенол ( п- ) | |
| Идентификаторы | |
|---|---|
| |
3D модель ( JSmol ) |
|
| ЧЭБИ |
|
| ChEMBL |
|
| ChemSpider |
|
| DrugBank |
|
| КЕГГ |
|
CID PubChem |
|
| УНИИ | |
| |
| |
| Характеристики | |
| С6Н5НО3 | |
| Молярная масса | 139,110 г·моль −1 |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |
с формулой HOC 6 H 4 NO 2. Существуют три изомерных нитрофенола:
- о -Нитрофенол (2-нитрофенол; группы ОН и NO 2 расположены рядом, желтое твердое вещество.
- м -Нитрофенол (3-нитрофенол, номер CAS: 554-84-7), желтое твердое вещество (т.пл. 97 °C) и предшественник препарата месалазин (5-аминосалициловая кислота). Его можно получить путем нитрования анилина с последующей заменой аминогруппы через его производное диазония. [2]
- п -Нитрофенол , желтое твердое вещество, является предшественником гербицида для риса фтордифена, пестицида паратиона и анальгетика для человека парацетамола (также известного как ацетаминофен).
Мононитрированные фенолы часто гидрогенизируют до соответствующих аминофенолов , которые также полезны в промышленности. [1]
Ди- и тринитрофенолы


- 2,4-Динитрофенол (т.пл. 83 °C) — умеренно сильная кислота (pKa = 4,89).
- 2,4,6-Тринитрофенол более известен как пикриновая кислота , которая имеет хорошо развитую химию.
Безопасность
Нитрофенолы ядовиты. Иногда нитрофенолы загрязняют почву вблизи бывших взрывчатых веществ или фабрик тканей и военных заводов, и текущие исследования направлены на рекультивацию. [3]
Ссылки
- ^ ab Gerald Booth (2007). "Нитросоединения, ароматические". Энциклопедия промышленной химии Ульмана . Weinheim: Wiley-VCH. doi :10.1002/14356007.a17_411. ISBN 978-3527306732.
- ^ RHF Manske (1928). "м-Нитрофенол". Органические синтезы . 8 : 80. doi :10.15227/orgsyn.008.0080.
- ^ Информационный листок на atsdr.cdc.gov
