11-Дезоксикортизол
 | |
 | |
| Имена | |
|---|---|
| Название ИЮПАК 17α,21-Дигидроксипрегн-4-ен-3,20-дион | |
| Систематическое название ИЮПАК (1 R ,3a S ,3b R ,9a R ,9b S ,11a S )-1-Гидрокси-1-(2-гидрокси-1-оксоэтил)-9a,11a-диметил-1,2,3,3a,3b,4,5,8,9,9a,9b,10,11,11a-тетрадекагидро-7 H -циклопента[ a ]фенантрен-7-он | |
| Другие имена 11-Дезоксикортизол; 11-Дезоксикортизон; Кортокселон; 17α,21-дигидроксипрогестерон; 11-Дезоксикортизол; 11-Дезоксигидрокортизон; 11-Дезоксигидрокортизон; 17α-Гидрокси-11-дезоксикортикостерон; Вещество Рейхштейна S; Соединение S; Кортодоксон; Кортексолон, | |
| Идентификаторы | |
3D модель ( JSmol ) |
|
| ЧЭБИ | |
| ChEMBL | |
| ChemSpider | |
| Информационная карта ECHA | 100.005.279 |
| |
| КЕГГ | |
CID PubChem |
|
| УНИИ | |
Панель инструментов CompTox ( EPA ) |
|
| |
| |
| Характеристики | |
| С21Н30О4 | |
| Молярная масса | 346,467 г·моль −1 |
| Температура плавления | 215 °C (419 °F; 488 К) |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |
11-Дезоксикортизол , также известный как кортодоксон ( INN ), кортексолон [1] [2] [3] [4], а также 17α,21-дигидроксипрогестерон или 17α,21-дигидроксипрегн-4-ен-3,20-дион , [5] является эндогенным глюкокортикоидным стероидным гормоном и метаболическим промежуточным продуктом по отношению к кортизолу . Впервые он был описан Тадеушем Райхштейном в 1938 году как Вещество S, [6] поэтому его также называют Веществом S Райхштейна [5] или Соединением S. [ 7] [8]
Функция
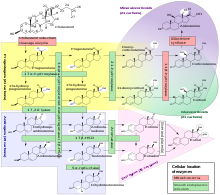
11-Дезоксикортизол действует как глюкокортикоид , хотя и менее мощный, чем кортизол . [10]
11-дезоксикортизол синтезируется из 17α-гидроксипрогестерона под действием 21-гидроксилазы и преобразуется в кортизол под действием 11β-гидроксилазы .
11-дезоксикортизол у млекопитающих имеет ограниченную биологическую активность и в основном действует как метаболический промежуточный продукт в глюкокортикоидном пути, приводя к кортизолу . [11] Однако у морских миног , ранних видов бесчелюстных рыб, которые возникли более 500 миллионов лет назад, 11-дезоксикортизол играет решающую роль в качестве первичного и конечного глюкокортикоидного гормона с минералокортикоидными свойствами; 11-дезоксикортизол также участвует, связываясь со специфическими кортикостероидными рецепторами, в кишечной осморегуляции у морских миног в период метаморфоза , во время которого они развивают толерантность к морской воде перед миграцией вниз по течению. [12] Морские миноги не обладают ферментом 11β-гидроксилазой ( CYP11B1 ), ответственным за преобразование 11-дезоксикортизола в кортизол и 11-дезоксикортикостерона в кортикостерон , как это наблюдается у млекопитающих. Отсутствие этого фермента у морских миног указывает на существование сложного и высокоспецифичного кортикостероидного сигнального пути, который возник по крайней мере 500 миллионов лет назад с появлением ранних позвоночных. Отсутствие кортизола и кортикостерона у морских миног предполагает, что присутствие фермента 11β-гидроксилазы могло отсутствовать на ранних стадиях эволюции позвоночных. [13] Отсутствие кортизола и кортикостерона у морских миног предполагает, что фермент 11β-гидроксилазы мог отсутствовать на ранних стадиях эволюции позвоночных. [14]
Клиническое значение
11-дезоксикортизол у млекопитающих имеет ограниченную глюкокортикоидную активность, но он является прямым предшественником основного глюкокортикоида млекопитающих, кортизола. [15] В результате уровень 11-дезоксикортизола измеряется для диагностики нарушения синтеза кортизола, для выявления дефицита фермента, который вызывает нарушение на пути к кортизолу, и для дифференциации заболеваний надпочечников. [16]
При дефиците 11β-гидроксилазы уровни 11-дезоксикортизола и 11-дезоксикортикостерона увеличиваются, а избыток 11-дезоксикортикостерона приводит к гипертонии на основе минералокортикоидов [17] (в отличие от дефицита 21-гидроксилазы , при котором у пациентов наблюдается низкое кровяное давление из-за недостатка минералокортикоидов ). Низкий уровень кортизола может влиять на кровяное давление, вызывая снижение задержки натрия и увеличение объема. Это связано с тем, что кортизол играет роль в регулировании баланса воды и электролитов в организме. Когда уровень кортизола низкий, почки меньше реабсорбируют натрий, что приводит к увеличению выведения натрия с мочой. Это в конечном итоге уменьшает объем крови и снижает кровяное давление. С другой стороны, высокий уровень кортизола также может влиять на кровяное давление, вызывая увеличение задержки натрия и увеличение объема. Гипертония, вызванная кортизолом, сопровождается значительной задержкой натрия, что приводит к увеличению объема внеклеточной жидкости и обменного натрия. Это приводит к увеличению объема крови и, следовательно, повышению артериального давления. Основные механизмы этих эффектов включают различные факторы, такие как подавление системы оксида азота, изменения в сосудистой реакции на прессорные агонисты, такие как адреналин, увеличение сердечного выброса или ударного объема из-за увеличения объема плазмы и потенциальное нарушение регуляции глюкокортикоидных рецепторов или активности фермента 11β-гидроксилазы . Важно отметить, что эти механизмы могут быть актуальны не только для гипертонии, вызванной кортизолом, но и для таких состояний, как синдром Кушинга (избыточная продукция кортизола), кажущийся избыток минералокортикоидов (связанный с дефектами ферментов 11β-гидроксилазы ), злоупотребление солодкой ( глицирретиновая кислота влияет на рецептор глицирретиновой кислоты), [18] хроническая почечная недостаточность (увеличение периода полувыведения кортизола из-за снижения активности 11β-гидроксилазы ) и даже эссенциальная гипертония, при которой могут быть нарушения активности 11β-гидроксилазы или вариации глюкокортикоидных рецепторов. [19] [20] [21] Низкий уровень кортизола приводит к снижению сосудистого тонуса.так как кортизол помогает поддерживать нормальный сосудистый тонус, способствуя сужению сосудов. Низкий уровень кортизола может привести к снижению сужения сосудов, что приводит к расслаблению кровеносных сосудов и снижению общего артериального давления. Кроме того, низкий уровень кортизола приводит к нарушению баланса жидкости, так как кортизол влияет на баланс жидкости, влияя на реабсорбцию натрия и воды в почках. Когда уровень кортизола низкий, абсорбция натрия может быть снижена, что приводит к увеличению выделения натрия с мочой и последующему снижению объема крови и артериального давления. Кроме того, низкий уровень кортизола вызывает нарушение регуляции ренин-ангиотензиновой системы, так как кортизол взаимодействует с ренин-ангиотензиновой системой, которая регулирует артериальное давление посредством сужения сосудов и баланса жидкости. Низкий уровень кортизола может нарушить эту систему, что приводит к изменению выработки ангиотензина, снижению секреции альдостерона и, следовательно, снижению артериального давления. И наоборот, высокий уровень кортизола приводит к повышению сосудистого тонуса, усилению задержки натрия и повышению симпатической активности. Вызванное стрессом высвобождение глюкокортикоидов высокого уровня, таких как кортизол, активирует симпатическую нервную систему (СНС). СНС контролирует частоту сердечных сокращений, сердечный выброс и вазомоторный тонус, вызывая сужение и тем самым увеличивая периферическое артериальное сопротивление, что приводит к повышению артериального давления. [22] При дефиците 11β-гидроксилазы 11-дезоксикортизол также может преобразовываться в андростендион по пути, который может объяснить повышение уровня андростендиона при этом состоянии. [23]
При дефиците 21-гидроксилазы уровень 11-дезоксикортизола низкий. [24]
История
В 1934 году биохимик Тадеус Райхштейн , работавший в Швейцарии , начал исследования экстрактов из надпочечников животных с целью выделения физиологически активных соединений. [25] По ходу дела он публиковал результаты своих открытий. К 1944 году он уже выделил и выяснил химическую структуру 29 чистых веществ. [26] Он давал названия, состоящие из слова «Вещество» и буквы латинского алфавита, вновь обнаруженным веществам. В 1938 году он опубликовал статью о «Веществе R» и «Веществе S», описывающую их химическую структуру и свойства. [6] Вещество S примерно с 1955 года стало известно как 11-дезоксикортизол. [27]
В 1949 году американский химик-исследователь Перси Лавон Джулиан , ища способы получения кортизона , объявил о синтезе Соединения S из дешевого и легкодоступного прегненолона (синтезированного из стерола соевого масла стигмастерола ). [28] [29]
5 апреля 1952 года биохимик Дьюри Петерсон и микробиолог Герберт Мюррей из Upjohn опубликовали первый отчет о революционном процессе ферментации для микробной 11α-оксигенации стероидов (например, прогестерона ) в один этап с помощью обычных плесневых грибов порядка Mucorales . [30] 11α-оксигенация соединения S приводит к образованию 11α-гидрокортизона, который может быть химически окислен до кортизона или преобразован в ходе дальнейших химических реакций в 11β-гидрокортизон ( кортизол ).
Смотрите также
Ссылки
- ^ Rosette C, Agan FJ, Rosette N, Mazzetti A, Moro L, Gerloni M (август 2020 г.). «Двойной антагонист андрогеновых рецепторов и глюкокортикоидных рецепторов CB-03-10 как потенциальное лечение опухолей, которые приобрели опосредованную GR устойчивость к блокаде AR». Molecular Cancer Therapeutics . 19 (11): 2256– 2266. doi : 10.1158/1535-7163.MCT-19-1137 . PMID 32847976. S2CID 221345484.
- ^ Ядерец В.В., Андрюшина В.А., Бартошевич И.Е., Домрачева А.Г., Новак М.И., Стиценко Т.С., Войшвилло Н.Е. (2007). «[Исследование стероидной гидроксилирующей активности мицелия Curvularia lunata]». Прикладная биохимия и микробиология . 43 (6): 695–700 . PMID 18173113.
- ^ Manosroi J, Chisti Y, Manosroi A (2006). «Биотрансформация кортексолона в гидрокортизон плесенью с использованием быстрого анализа развития цвета». Прикладная биохимия и микробиология . 42 (5): 547–51 . PMID 17066954.
- ^ Lisowska K, Długoński J (май 2003). «Одновременная трансформация кортикостероидов и фенантрена нитчатым грибом Cunninghamella elegans». Журнал стероидной биохимии и молекулярной биологии . 85 (1): 63– 9. doi :10.1016/s0960-0760(03)00136-5. PMID 12798358. S2CID 384672.
- ^ ab RA Hill, HLJ Makin, DN Kirk, GM Murphy (23 мая 1991 г.). Словарь стероидов. CRC Press. стр. 338–. ISBN 978-0-412-27060-4.
- ^ аб Райхштейн Т (1938). «Über Bestandteile der Nebennierenrinde. 21. Mitteilung. Die Konstitution der Substanzen R und S» . Helvetica Chimica Acta . 21 : 1490–1497 . doi : 10.1002/hlca.193802101183. Архивировано из оригинала 10 октября 2020 года . Проверено 5 октября 2020 г.
- ^ Wudy SA, Hartmann M, Homoki J (сентябрь 2002 г.). «Определение 11-дезоксикортизола (соединения S Рейхштейна) в плазме человека методом клинической масс-спектрометрии с изотопным разбавлением с использованием настольной газовой хроматографии с селективным масс-детектированием». Steroids . 67 (10): 851– 7. doi :10.1016/s0039-128x(02)00052-1. PMID 12231120. S2CID 29970823.
- ^ Berneis K, Staub JJ, Gessler A, Meier C, Girard J, Müller B (декабрь 2002 г.). «Комбинированная стимуляция адренокортикотропина и соединения S с помощью теста с однократной дозой метирапона в качестве амбулаторной процедуры для оценки функции гипоталамуса, гипофиза и надпочечников». Журнал клинической эндокринологии и метаболизма . 87 (12): 5470– 5. doi : 10.1210/jc.2001-011959 . PMID 12466339.
- ^ Häggström M, Richfield D (2014). «Схема путей стероидогенеза человека». WikiJournal of Medicine . 1 (1). doi : 10.15347/wjm/2014.005 . ISSN 2002-4436.
- ↑ Энгельс М., Пейненбург-Кляйзен К.Дж., Утари А., Фарадз С.М., Оуде-Алинк С., ван Херваарден А.Е., Спан ПН, Sweep FC, Клаахсен-ван дер Гринтен HL (ноябрь 2019 г.). «Глюкокортикоидная активность предшественников стероидов надпочечников у нелеченых пациентов с врожденной гиперплазией надпочечников». Журнал клинической эндокринологии и метаболизма . 104 (11): 5065–5072 . doi : 10.1210/jc.2019-00547 . ПМИД 31090904.
- ^ "Врожденная гиперплазия надпочечников, вызванная дефицитом 11бета-гидроксилазы". Merck Manuals Professional Edition . Архивировано из оригинала 25 сентября 2020 г. Получено 3 октября 2020 г.
- ^ Barany A, Shaughnessy CA, McCormick SD (март 2021 г.). «Кортикостероидный контроль Na+/K+-АТФазы в кишечнике морской миноги (Petromyzon marinus)». Общая и сравнительная эндокринология . 307 : 113756. doi : 10.1016/j.ygcen.2021.113756. PMID 33741310. S2CID 232296805.
- ^ Shaughnessy CA, Barany A, McCormick SD (июль 2020 г.). "11-Дезоксикортизол контролирует гидроминеральный баланс у самого базального осморегулятора позвоночного, морской миноги (Petromyzon marinus)". Scientific Reports . 10 (1): 12148. Bibcode :2020NatSR..1012148S. doi :10.1038/s41598-020-69061-4. PMC 7376053 . PMID 32699304.
- ^ Close DA, Yun SS, McCormick SD, Wildbill AJ, Li W (август 2010 г.). «11-дезоксикортизол — кортикостероидный гормон у миноги». Труды Национальной академии наук Соединенных Штатов Америки . 107 (31): 13942– 7. Bibcode : 2010PNAS..10713942C. doi : 10.1073/pnas.0914026107 . PMC 2922276. PMID 20643930 .
- ^ Zöllner A, Kagawa N, Waterman MR, Nonaka Y, Takio K, Shiro Y, Hannemann F, Bernhardt R (февраль 2008 г.). «Очистка и функциональная характеристика человеческой 11бета-гидроксилазы, экспрессируемой в Escherichia coli». Журнал FEBS . 275 (4): 799– 810. doi :10.1111/j.1742-4658.2008.06253.x. PMID 18215163. S2CID 45997341.
- ^ "Уровни стероидов в сыворотке могут помочь дифференцировать нарушения надпочечников". Архивировано из оригинала 7 ноября 2020 г. Получено 3 октября 2020 г.
- ^ Гупта V (октябрь 2011 г.). «Минералокортикоидная гипертензия». Индийский журнал эндокринологии и метаболизма . 15 (Приложение 4): S298-312. doi : 10.4103/2230-8210.86972 . PMC 3230101. PMID 22145132 .
- ^ Li YL, Zhu XM, Liang H, Orvig C, Chen ZF (2021). «Последние достижения в области опосредованной рецептором азиалогликопротеина и рецептором глицирретиновой кислоты и/или чувствительной к pH гепатоцеллюлярной карциномы — направленная доставка лекарств». Curr Med Chem . 28 (8): 1508–1534 . doi :10.2174/0929867327666200505085756. PMID 32368967.
- ^ Келли Дж. Дж., Мангос Г., Уильямсон П. М., Уитворт Дж. А. (ноябрь 1998 г.). «Кортизол и гипертония». Clin Exp Pharmacol Physiol Suppl . 25 : S51–6. doi :10.1111/j.1440-1681.1998.tb02301.x. PMID 9809193. S2CID 13428727.
- ^ van Uum SH, Lenders JW, Hermus AR (май 2004 г.). «Кортизол, 11-бета-гидроксистероиддегидрогеназы и гипертония». Semin Vasc Med . 4 (2): 121– 8. doi :10.1055/s-2004-835369. PMID 15478032. S2CID 260371999.
- ^ Стюарт П.М. (1998). «Кортизол, гипертония и ожирение: роль 11 бета-гидроксистероиддегидрогеназы». JR Coll Physicians Lond . 32 (2): 154–9 . PMC 9663025. PMID 9597634 .
- ^ Lewandowski KC, Tadros-Zins M, Horzelski W, Krekora M, Lewinski A (апрель 2023 г.). «Ренин, альдостерон и кортизол при гипертензии, вызванной беременностью». Exp Clin Endocrinol Diabetes . 131 (4): 222– 227. doi :10.1055/a-2025-0510. PMC 10101736. PMID 36807213 .
- ^ Auzéby A, Bogdan A, Touitou Y (январь 1991 г.). «Доказательства нового биологического пути синтеза андростендиона из 11-дезоксикортизола». Стероиды . 56 (1): 33– 6. doi :10.1016/0039-128X(91)90112-9. PMID 2028480. S2CID 6261965.
- ^ Essential Endocrinology: A Primer for Nonspecialists . Springer Science & Business Media. 2013. стр. 263. ISBN 978-1-4899-1692-1.
- ^ "Химия гормонов коры надпочечников". Архивировано из оригинала 10 октября 2020 г. Получено 5 октября 2020 г.
- ^ Grzybowski A, Pietrzak K (2012). «Тадеуш Райхштейн (1897-1996): соучредитель современного лечения стероидами в дерматологии». Клиники дерматологии . 30 (2): 243– 7. doi :10.1016/j.clindermatol.2011.09.003. PMID 22435119.
- ^ Forchielli E, Rosenkrantz H, Dorfman RI (1 августа 1955 г.). «Метаболизм 11-дезоксикортизола in vitro». The Journal of Biological Chemistry . 215 (2): 713– 22. doi : 10.1016/S0021-9258(18)65996-4 . PMID 13242571. Архивировано из оригинала 17 ноября 2020 г. Получено 9 ноября 2020 г.
- ^ "Наука получает синтетический ключ к редкому лекарству; открытие сделано в Чикаго". Chicago Tribune . 30 сентября 1949 г. стр. 1. Архивировано из оригинала 31 января 2013 г.
Новый метод доктора Джулиана по синтезу противоартритного соединения, кортизона, менее затратен, чем существующие методы, поскольку он устраняет необходимость использования тетроксида осмия, редкого и дорогостоящего химиката, заявила компания Glidden... Но ни он, ни компания Glidden не раскрывают, синтезировал ли доктор Джулиан также кортизон из соевых бобов.
- ^ "Новости недели: Новый синтез кортизона". Chemical & Engineering News . 27 (41): 2936– 2942. 10 октября 1949 г. doi :10.1021/cen-v027n041.p2936.
Цитата: Новый синтез кортизона, устраняющий необходимость в дорогостоящем тетроксиде осмия, и синтез трех других соединений, связанных с кортизоном, которые могут быть полезны при лечении артрита, были объявлены Перси Л. Джулианом, директором по исследованиям подразделения соевых продуктов компании Glidden Co., Чикаго. Не было сделано никаких заявлений относительно дальнейших подробностей нового синтеза, но было обнаружено, что соевые продукты не были задействованы... все три [других соединения] были получены из соевых стеролов.
- ^ Peterson DH, Murray, HC (1952). «Микробиологическое окисление стероидов у углерода 11». J Am Chem Soc . 74 (7): 1871– 2. Bibcode : 1952JAChS..74.1871P. doi : 10.1021/ja01127a531.



