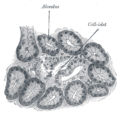
Панкреатические островки
| Панкреатические островки | |
|---|---|
 Панкреатические островки — это группы клеток, находящихся в поджелудочной железе , которые выделяют гормоны. | |
 Островок поджелудочной железы мыши в типичном положении, рядом с кровеносным сосудом; инсулин обозначен красным, ядра — синим. | |
| Подробности | |
| Часть | Поджелудочная железа |
| Система | Эндокринная |
| Идентификаторы | |
| латинский | островок поджелудочной железы |
| МеШ | Д007515 |
| ТА98 | А05.9.01.019 |
| ТА2 | 3128 |
| ФМА | 16016 |
| Анатомические термины микроанатомии [править на Wikidata] | |
Островки поджелудочной железы или островки Лангерганса — это области поджелудочной железы , содержащие ее эндокринные (гормонпродуцирующие) клетки, открытые в 1869 году немецким патологоанатомом Паулем Лангергансом . [1] Островки поджелудочной железы составляют 1–2% от объема поджелудочной железы и получают 10–15% ее кровотока. [2] [3] Островки поджелудочной железы расположены в плотных маршрутах по всей поджелудочной железе человека и играют важную роль в метаболизме глюкозы . [4]
Структура
Около 1 миллиона островков распределены по всей поджелудочной железе здорового взрослого человека. Хотя островки различаются по размеру, средний диаметр составляет около 0,2 мм. [5] :928 Каждый островок отделен от окружающей ткани поджелудочной железы тонкой, волокнистой, соединительнотканной капсулой, которая является продолжением волокнистой соединительной ткани, которая переплетена по всей остальной части поджелудочной железы. [5] :928
Микроанатомия
Гормоны, вырабатываемые в панкреатических островках, секретируются непосредственно в кровоток (по крайней мере) пятью типами клеток. В островках крысы типы эндокринных клеток распределены следующим образом: [6]
- Альфа-клетки, продуцирующие глюкагон (20% от общего числа островковых клеток)
- Бета-клетки, вырабатывающие инсулин и амилин (≈70%)
- Клетки PP (гамма-клетки или F-клетки), продуцирующие панкреатический полипептид (<5%)
- Дельта-клетки, продуцирующие соматостатин (<10%)
- Эпсилон-клетки, продуцирующие грелин (<1%)
Было признано, что цитоархитектура островков поджелудочной железы различается у разных видов. [7] [8] [9] В частности, в то время как островки грызунов характеризуются преобладающей долей инсулин-продуцирующих бета-клеток в ядре кластера и редкими альфа-, дельта- и PP-клетками на периферии, человеческие островки демонстрируют альфа- и бета-клетки, находящиеся в тесной взаимосвязи друг с другом по всему кластеру. [7] [9]
Доля бета-клеток в островках варьируется в зависимости от вида, у человека она составляет около 40–50%. Помимо эндокринных клеток, существуют стромальные клетки (фибробласты), сосудистые клетки (эндотелиальные клетки, перициты), иммунные клетки (гранулоциты, лимфоциты, макрофаги, дендритные клетки) и нервные клетки. [10]
Через островки протекает большое количество крови — 5–6 мл/мин на 1 г островка. Это в 15 раз больше, чем в экзокринной ткани поджелудочной железы. [10]
Островки могут влиять друг на друга через паракринную и аутокринную связь, а бета-клетки электрически связаны с шестью-семью другими бета-клетками, но не с другими типами клеток. [11] Панкреатические островки характеризуются богатой иннервацией и васкуляризацией, хотя между островками грызунов и людей имеются заметные различия. Исследования показывают, что плотность сосудов в человеческих островках примерно в пять раз ниже, чем в островках грызунов. [12] [13] Сосудистая сеть внутри островков напоминает клубочковую структуру, состоящую из сильно фенестрированных эндотелиальных клеток, расположенных близко к каждой эндокринной клетке. [14] [15] Следовательно, напряжение кислорода внутри панкреатических островков значительно выше, чем в окружающей экзокринной ткани. [16]
- Окрашенный островок поджелудочной железы.
- Островок поджелудочной железы, на котором видны альфа-клетки.
- Островок поджелудочной железы, на котором видны бета-клетки.
Функция
Паракринная система обратной связи панкреатических островков имеет следующую структуру: [17 ]
- Глюкоза/инсулин: активирует бета-клетки и подавляет альфа-клетки.
- Гликоген/глюкагон: активирует альфа-клетки, которые активируют бета-клетки и дельта-клетки.
- Соматостатин: ингибирует альфа-клетки и бета-клетки. Также ингибирует секрецию панкреатического полипептида . [18]
Большое количество рецепторов, сопряженных с G-белком (GPCR), регулируют секрецию инсулина, глюкагона и соматостатина из островков поджелудочной железы [19] , и некоторые из этих GPCR являются мишенями препаратов, используемых для лечения диабета 2 типа (см. агонисты рецепторов GLP-1, ингибиторы DPPIV).
- Иммуноокрашивание мышиных островков на панкреатический полипептид
- Иммуноокрашивание островков поджелудочной железы мыши на инсулин
- Иммуноокрашенные островки поджелудочной железы мыши на глюкагон
Электрическая активность
Электрическая активность панкреатических островков изучалась с помощью метода пэтч-кламп . Оказалось, что поведение клеток в интактных островках существенно отличается от поведения рассеянных клеток. [20]
Клиническое значение
Диабет
Бета-клетки островков поджелудочной железы секретируют инсулин , и поэтому играют важную роль в диабете . Считается, что они разрушаются иммунными атаками.
Поскольку бета-клетки в островках поджелудочной железы избирательно разрушаются аутоиммунным процессом при диабете 1 типа , врачи и исследователи активно изучают трансплантацию островков как способ восстановления физиологической функции бета-клеток, что могло бы стать альтернативой полной трансплантации поджелудочной железы или искусственной поджелудочной железе . [21] [22] Трансплантация островков появилась как жизнеспособный вариант лечения инсулинозависимого диабета в начале 1970-х годов с устойчивым прогрессом в течение последующих трех десятилетий. [23] Клинические испытания по состоянию на 2008 год [обновлять]показали, что независимость от инсулина и улучшенный метаболический контроль могут быть воспроизводимо получены после трансплантации островков трупного донора пациентам с нестабильным диабетом 1 типа . [22] В качестве альтернативы ежедневные инъекции инсулина являются эффективным лечением для пациентов с диабетом 1 типа, которые не являются кандидатами на трансплантацию островков.
Люди с высоким индексом массы тела (ИМТ) не подходят в качестве доноров поджелудочной железы из-за больших технических осложнений во время трансплантации. Однако возможно выделить большее количество островков из-за их большей поджелудочной железы, и поэтому они являются более подходящими донорами островков. [24]
Трансплантация островков включает в себя только перенос ткани, состоящей из бета-клеток, которые необходимы для лечения этого заболевания. Таким образом, это представляет собой преимущество перед трансплантацией всей поджелудочной железы, которая технически более сложна и несет риск, например, панкреатита, приводящего к потере органа. [24] Еще одним преимуществом является то, что пациентам не требуется общая анестезия. [25]
Трансплантация островков при диабете 1 типа (по состоянию на 2008 год [обновлять]) требует мощной иммуносупрессии для предотвращения отторжения донорских островков хозяином. [26]
Островки трансплантируются в воротную вену , которая затем имплантируется в печень. [24] Существует риск тромбоза воротной вены и низкого значения выживаемости островков через несколько минут после трансплантации, поскольку плотность сосудов в этом месте после операции на несколько месяцев ниже, чем в эндогенных островках. Таким образом, неоваскуляризация является ключом к выживанию островков, которое поддерживается, например, VEGF, вырабатываемым островками и сосудистыми эндотелиальными клетками. [10] [25] Однако интрапортальная трансплантация имеет некоторые другие недостатки, и поэтому изучаются другие альтернативные места, которые могли бы обеспечить лучшую микросреду для имплантации островков. [24] Исследования по трансплантации островков также фокусируются на инкапсуляции островков, иммуносупрессии без CNI ( ингибитор кальциневрина ), биомаркерах повреждения островков или дефиците доноров островков. [27]
Альтернативный источник бета-клеток, такие инсулин-продуцирующие клетки, полученные из взрослых стволовых клеток или клеток-предшественников, могли бы способствовать преодолению нехватки донорских органов для трансплантации. Область регенеративной медицины быстро развивается и подает большие надежды на ближайшее будущее. Однако диабет 1 типа является результатом аутоиммунного разрушения бета-клеток поджелудочной железы. Поэтому эффективное лечение потребует последовательного, комплексного подхода, который сочетает адекватные и безопасные иммунные вмешательства с подходами к регенерации бета-клеток. [28] Также было продемонстрировано, что альфа-клетки могут спонтанно менять судьбу и трансдифференцироваться в бета-клетки как в здоровых, так и в диабетических панкреатических островках человека и мыши, что является возможным будущим источником регенерации бета-клеток. [29] Фактически, было обнаружено, что морфология островков и эндокринная дифференцировка напрямую связаны. [30] Эндокринные клетки-предшественники дифференцируются, мигрируя в связке и формируя похожие на почки островковые предшественники, или «полуострова», в которых альфа-клетки составляют полуостровной наружный слой, а бета-клетки формируются позже под ними. Криоконсервация показала перспективу улучшения цепочки поставок панкреатических островков для лучших результатов трансплантации. [31]
Дополнительные изображения
- Островки поджелудочной железы, более светлая ткань среди более темной, ацинарной ткани поджелудочной железы, окраска гемалюмо- эозином .
- Иллюстрация поджелудочной железы собаки. 250x.
- Структурные различия между островками крысы (вверху) и человека (внизу), а также вентральной частью (слева) и дорсальной частью (справа) поджелудочной железы . Различные типы клеток имеют цветовую кодировку. Островки грызунов, в отличие от человеческих, показывают характерное инсулиновое ядро.
Исследовать
Каннабиноидные рецепторы широко экспрессируются в островках Лангерганса, и в нескольких исследованиях изучалось специфическое распределение и механизмы рецепторов CB1 и CB2 в связи с эндокринными функциями поджелудочной железы , где они играют важную гомеостатическую роль, поскольку эндоканнабиноиды модулируют функцию, пролиферацию и выживание β-клеток поджелудочной железы , а также выработку, секрецию и резистентность инсулина . [32] [33] [34] [35]
Смотрите также
- Бетатрофин
- Нейроэндокринная опухоль
- Нейроэндокринная опухоль поджелудочной железы
- «Дрейфуя недалеко от островков Лангерганса» , повесть Харлана Эллисона
Ссылки
- ^ Лангерганс П (1869). «Beitrage zur microscopischen anatomie der bauchspeichel druse». Инаугурационная диссертация. Берлин: Густав Ланге .
- ^ Barrett KE, Boitano S, Barman SM, Brooks HL (2009-07-22). Обзор медицинской физиологии Ганонга (23-е изд.). McGraw Hill Medical. стр. 316. ISBN 978-0-07-160568-7.
- ^ Функциональная анатомия эндокринной части поджелудочной железы
- ^ Pour PM, Standop J, Batra SK (январь 2002 г.). «Являются ли островковые клетки привратниками поджелудочной железы?». Панкреатология . 2 (5): 440– 448. doi :10.1159/000064718. PMID 12378111. S2CID 37257345.
- ^ ab Feldman M, Friedman LS, Brandt LJ, ред. (2015). Патофизиология, диагностика, лечение желудочно-кишечных и печеночных заболеваний Sleisenger & Fordtran (10-е изд.). Сент-Луис, Миссури: Elsevier Health Sciences. ISBN 978-1-4557-4989-8.
- ^ Elayat AA, el-Naggar MM, Tahir M (июнь 1995). «Иммуноцитохимическое и морфометрическое исследование островков поджелудочной железы крысы». Журнал анатомии . 186. 186 (Pt 3): 629–637 . PMC 1167020. PMID 7559135 .
- ^ ab Brissova M, Fowler MJ, Nicholson WE, Chu A, Hirshberg B, Harlan DM и др. (сентябрь 2005 г.). «Оценка архитектуры и состава островков поджелудочной железы человека с помощью лазерной сканирующей конфокальной микроскопии». Журнал гистохимии и цитохимии . 53 (9): 1087–1097 . doi : 10.1369/jhc.5C6684.2005 . PMID 15923354.
- ^ Ichii H, Inverardi L, Pileggi A, Molano RD, Cabrera O, Caicedo A и др. (Июль 2005 г.). «Новый метод оценки клеточного состава и жизнеспособности бета-клеток в препаратах островков человека». American Journal of Transplantation . 5 (7): 1635– 1645. CiteSeerX 10.1.1.578.5893 . doi :10.1111/j.1600-6143.2005.00913.x. PMID 15943621. S2CID 234176.
- ^ ab Cabrera O, Berman DM, Kenyon NS, Ricordi C, Berggren PO, Caicedo A (февраль 2006 г.). «Уникальная цитоархитектура островков поджелудочной железы человека имеет значение для функции островковых клеток». Труды Национальной академии наук Соединенных Штатов Америки . 103 (7): 2334– 2339. Bibcode : 2006PNAS..103.2334C. doi : 10.1073/pnas.0510790103 . PMC 1413730. PMID 16461897 .
- ^ abc Jansson L, Barbu A, Bodin B, Drott CJ, Espes D, Gao X и др. (май 2016 г.). «Кровоток в островках поджелудочной железы и его измерение». Upsala Journal of Medical Sciences . 121 (2): 81– 95. doi :10.3109/03009734.2016.1164769. PMC 4900068. PMID 27124642 .
- ^ Келли С, МакКленаган NH, Флэтт PR (2011). «Роль структуры островков и клеточных взаимодействий в контроле секреции инсулина». Islets . 3 (2): 41– 47. doi : 10.4161/isl.3.2.14805 . PMID 21372635.
- ^ Cohrs CM, Chen C, Jahn SR, Stertmann J, Chmelova H, Weitz J и др. (Май 2017). «Архитектура сосудистой сети островков взрослого человека способствует различным межклеточным взаимодействиям in situ и изменяется после трансплантации». Эндокринология . 158 (5): 1373– 1385. doi :10.1210/en.2016-1184. PMID 28324008.
- ^ Brissova M, Shostak A, Fligner CL, Revetta FL, Washington MK, Powers AC и др. (август 2015 г.). «У человеческих островков меньше кровеносных сосудов, чем у мышиных, и плотность сосудистых структур островков увеличивается при диабете 2 типа». Журнал гистохимии и цитохимии . 63 (8): 637– 645. doi :10.1369/0022155415573324. PMC 4530394 . PMID 26216139.
- ^ Bonner-Weir S, Orci L (октябрь 1982 г.). «Новые перспективы микроциркуляторного русла островков Лангерганса у крыс». Диабет . 31 (10): 883–889 . doi :10.2337/diab.31.10.883. PMID 6759221.
- ^ Кабрера О., Берман Д.М., Кеньон Н.С., Рикорди К., Берггрен П.О., Кайседо А. (февраль 2006 г.). «Уникальная цитоархитектура островков поджелудочной железы человека имеет значение для функции островковых клеток». Труды Национальной академии наук Соединенных Штатов Америки . 103 (7): 2334– 2339. Bibcode : 2006PNAS..103.2334C. doi : 10.1073/pnas.0510790103 . PMC 1413730. PMID 16461897 .
- ^ Карлссон PO, Лисс П, Андерссон А, Янссон Л (июль 1998 г.). «Измерения напряжения кислорода в нативных и трансплантированных панкреатических островках крыс». Диабет . 47 (7): 1027–1032 . doi :10.2337/diabetes.47.7.1027. PMID 9648824.
- ^ Wang MB, Bullock J, Boyle JR (2001). Физиология . Hagerstown, MD: Lippincott Williams & Wilkins. стр. 391. ISBN 978-0-683-30603-3.
- ^ Marques JM, Nunes R, Florindo H, Ferreira D, Sarmento B (2021). «Требовательный путь от iPSCs к панкреатическим β- и α-клеткам». Последние достижения в области типов клеток, полученных из IPSC . Достижения в области биологии стволовых клеток. 4 : 227– 256. doi :10.1016/B978-0-12-822230-0.00002-8. ISBN 9780128222300. S2CID 234135648 . Получено 18 января 2023 г. .
- ^ Амистен С, Салехи А, Рорсман П, Джонс ПМ, Персо СДж (сентябрь 2013 г.). «Атлас и функциональный анализ рецепторов, сопряженных с G-белком, в островках Лангерганса человека». Фармакология и терапия . 139 (3): 359– 391. doi :10.1016/j.pharmthera.2013.05.004. PMID 23694765.
- ^ Pérez-Armendariz M, Roy C, Spray DC, Bennett MV (январь 1991). «Биофизические свойства щелевых контактов между свежедисперсными парами бета-клеток поджелудочной железы мыши». Biophysical Journal . 59 (1): 76– 92. Bibcode :1991BpJ....59...76P. doi :10.1016/S0006-3495(91)82200-7. PMC 1281120 . PMID 2015391.
- ^ Meloche RM (декабрь 2007 г.). «Трансплантация для лечения диабета 1 типа». World Journal of Gastroenterology . 13 (47): 6347– 6355. doi : 10.3748/wjg.13.6347 . PMC 4205453. PMID 18081223 .
- ^ ab Hogan A, Pileggi A, Ricordi C (январь 2008 г.). «Трансплантация: текущие разработки и будущие направления; будущее клинической трансплантации островков как средства лечения диабета». Frontiers in Bioscience . 13 (13): 1192– 1205. doi : 10.2741/2755 . PMID 17981623.
- ^ Piemonti L, Pileggi A (2013). «25 лет автоматизированному методу Ricordi для изоляции островков». CellR4-- Ремонт, замена, регенерация и перепрограммирование . 1 (1): 8–22 . PMC 6267808. PMID 30505878 .
- ^ abcd Никлаусс Н., Мейер Р., Бедат Б., Беришвили Э., Берни Т. (27 января 2016 г.). Стеттлер С., Крист Э., Дим П. (ред.). «Замена бета-клеток: трансплантация поджелудочной железы и островковых клеток». Эндокринное развитие . 31 . С. Каргер АГ: 146–162 . doi : 10.1159/000439412. ISBN 978-3-318-05638-9. PMID 26824893.
- ^ ab Gamble A, Pepper AR, Bruni A, Shapiro AM (март 2018 г.). «Путь трансплантации островковых клеток и будущее развитие». Islets . 10 (2): 80– 94. doi :10.1080/19382014.2018.1428511. PMC 5895174 . PMID 29394145.
- ^ Chatenoud L (март 2008 г.). «Химическая иммуносупрессия при трансплантации островков — друг или враг?». The New England Journal of Medicine . 358 (11): 1192– 1193. doi :10.1056/NEJMcibr0708067. PMID 18337609.
- ^ Chang CA, Lawrence MC, Naziruddin B (октябрь 2017 г.). «Актуальные вопросы аллогенной трансплантации островков». Current Opinion in Organ Transplantation . 22 (5): 437– 443. doi :10.1097/MOT.00000000000000448. PMID 28692442. S2CID 37483032.
- ^ Пиледжи А., Кобьянки Л., Инверарди Л., Рикорди К. (октябрь 2006 г.). «Преодоление проблем, которые в настоящее время ограничивают трансплантацию островков: последовательный, комплексный подход». Анналы Нью-Йоркской академии наук . 1079 (1): 383–398 . Bibcode : 2006NYASA1079..383P. doi : 10.1196/annals.1375.059. PMID 17130583. S2CID 33009393.
- ^ van der Meulen T, Mawla AM, DiGruccio MR, Adams MW, Nies V, Dólleman S и др. (апрель 2017 г.). «Девственные бета-клетки сохраняются на протяжении всей жизни в неогенной нише в панкреатических островках». Cell Metabolism . 25 (4): 911–926.e6. doi : 10.1016/j.cmet.2017.03.017 . PMC 8586897 . PMID 28380380.
- ^ Sharon N, Chawla R, Mueller J, Vanderhooft J, Whitehorn LJ, Rosenthal B и др. (февраль 2019 г.). «Полуостровная структура координирует асинхронную дифференциацию с морфогенезом для генерации панкреатических островков». Cell . 176 (4) (опубликовано в 2019 г.): 790–804.e13. doi :10.1016/j.cell.2018.12.003. PMC 6705176 . PMID 30661759.
- ^ Zhan L, Rao JS, Sethia N, Slama MQ, Han Z, Tobolt D и др. (апрель 2022 г.). «Криоконсервация островков поджелудочной железы путем витрификации обеспечивает высокую жизнеспособность, функциональность, восстановление и клиническую масштабируемость для трансплантации». Nature Medicine . 28 (4): 798– 808. doi :10.1038/s41591-022-01718-1. PMC 9018423 . PMID 35288694.
- ^ Бермудес-Сильва Ф.Дж., Суарес Дж., Байшерас Э., Кобо Н., Баутиста Д., Куэста-Муньос А.Л. и др. (март 2008 г.). «Наличие функциональных каннабиноидных рецепторов в эндокринной поджелудочной железе человека». Диабетология . 51 (3): 476–487 . doi : 10.1007/s00125-007-0890-y . ПМИД 18092149.
- ^ Flores LE, Alzugaray ME, Cubilla MA, Raschia MA, Del Zotto HH, Román CL и др. (октябрь 2013 г.). «Islet cannabinoid receptors: cellular distribution and biology function» (островковые каннабиноидные рецепторы: клеточное распределение и биологическая функция). Pancreas . 42 (7): 1085– 1092. doi :10.1097/MPA.0b013e31828fd32d. PMID 24005231. S2CID 36905885.
- ^ Хуан-Пико П., Фуэнтес Э., Бермудес-Сильва Ф.Дж., Хавьер Диас-Молина Ф., Риполь С., Родригес де Фонсека Ф. и др. (февраль 2006 г.). «Каннабиноидные рецепторы регулируют сигналы Ca (2+) и секрецию инсулина в бета-клетках поджелудочной железы». Клеточный кальций . 39 (2): 155–162 . doi :10.1016/j.ceca.2005.10.005. ПМИД 16321437.
- ^ Farokhnia M, McDiarmid GR, Newmeyer MN, Munjal V, Abulseoud OA, Huestis MA и др. (февраль 2020 г.). «Влияние перорального, курительного и испаряемого каннабиса на эндокринные пути, связанные с аппетитом и метаболизмом: рандомизированное, двойное слепое, плацебо-контролируемое, лабораторное исследование на людях». Трансляционная психиатрия . 10 (1): 71. doi : 10.1038 /s41398-020-0756-3. PMC 7031261. PMID 32075958.
Внешние ссылки
- Поджелудочная железа в Атласе белков человека