Мифамуртид
 | |
| Клинические данные | |
|---|---|
| Торговые наименования | Мепакт |
| Данные лицензии |
|
Категория беременности |
|
| Пути введения | внутривенная липосомальная инфузия в течение одного часа |
| код АТС |
|
| Правовой статус | |
| Правовой статус |
|
| Фармакокинетические данные | |
| Биодоступность | Н/Д |
| Период полувыведения | минут (в плазме) 18 часов (терминальный) |
| Идентификаторы | |
| |
| Номер CAS | |
| CID PubChem |
|
| ChemSpider | |
| УНИИ |
|
| КЕГГ | |
| Химические и физические данные | |
| Формула | С 59 Н 109 Н 6 О 19 П |
| Молярная масса | 1 237 .518 г·моль −1 |
| 3D модель ( JSmol ) |
|
| |
| |
 Н Н И (что это?) (проверить) И (что это?) (проверить) | |
Мифамуртид (торговое название Mepact , продается компанией Takeda ) — это препарат против остеосаркомы , вида рака костей , поражающего в основном детей и молодых людей, который приводит к летальному исходу более чем в половине случаев. Препарат был одобрен в Европе в марте 2009 года.
Медицинское применение
Мифамуртид показан для лечения высокозлокачественной, неметастазирующей , резектабельной остеосаркомы после полного хирургического удаления у детей, подростков и молодых людей в возрасте от двух до 30 лет. [1] [2] [3] Остеосаркома диагностируется примерно у 1000 человек в Европе и США в год, большинство из которых моложе 30 лет. [4] Препарат используется в сочетании с послеоперационной многокомпонентной химиотерапией для уничтожения оставшихся раковых клеток и повышения шансов пациента на общую выживаемость. [2]
В клиническом исследовании фазы III, в котором приняли участие около 800 пациентов с впервые диагностированной остеосаркомой, мифамуртид сочетался с химиотерапевтическими средствами доксорубицином и метотрексатом , с цисплатином и ифосфамидом или без них . Смертность могла быть снижена на 30% по сравнению с химиотерапией плюс плацебо . Через шесть лет после лечения 78% пациентов были еще живы. Это соответствует абсолютному снижению риска на 8%. [1]
Побочные эффекты
В клиническом исследовании мифамуртид был назначен 332 субъектам (половина из которых были моложе 16 лет), и большинство побочных эффектов были признаны легкими или умеренными по своей природе. Большинство пациентов испытывают меньше побочных эффектов при последующем приеме. [5] [6] Распространенные побочные эффекты включают лихорадку (около 90%), рвоту, усталость и тахикардию (около 50%), инфекции , анемию , анорексию , головную боль, диарею и запор (>10%). [1] [7]
Взаимодействия
- Теоретические соображения предполагают, что ингибиторы кальциневрина, такие как циклоспорин и такролимус, могут взаимодействовать с мифамуртидом из-за их воздействия на макрофаги.
- Высокие дозы НПВП блокируют механизм действия мифамуртида in vitro .
Следовательно, сочетание мифамуртида с этими типами препаратов противопоказано. Однако мифамуртид можно назначать совместно с низкими дозами НПВП. Нет никаких доказательств, что мифамуртид взаимодействует с изученными химиотерапевтическими средствами или с системой цитохрома P450 . [8]
Фармакология
Механизм действия
Мифамуртид — полностью синтетическое производное мурамилдипептида (МДП), наименьшего естественного иммуностимулирующего компонента клеточных стенок видов Mycobacterium . Он обладает схожим иммуностимулирующим эффектом с природным МДП, но имеет преимущество в виде более длительного периода полураспада в плазме.
NOD2 — это рецептор распознавания образов , который находится в нескольких видах белых кровяных клеток , в основном в моноцитах и макрофагах . Он распознает мурамилдипептид, компонент клеточной стенки бактерий . Мифамуртид имитирует бактериальную инфекцию, связываясь с NOD2, активируя белые клетки. Это приводит к увеличению продукции TNF-α , интерлейкина 1 , интерлейкина 6 , интерлейкина 8 , интерлейкина 12 и других цитокинов , а также ICAM-1 . Активированные белые клетки атакуют раковые клетки, но не, по крайней мере in vitro , другие клетки. [9]
Фармакокинетика
После применения липосомальной инфузии препарат выводится из плазмы в течение нескольких минут и концентрируется в легких, печени, селезенке , носоглотке и щитовидной железе . Конечный период полувыведения составляет 18 часов. У пациентов, получавших повторное лечение через 11–12 недель, никаких эффектов накопления не наблюдалось. [10]
Химия

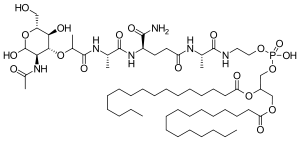
Мифамуртид — это мурамилтрипептидфосфатидилэтаноламин (MTP-PE), синтетический аналог мурамилдипептида. Боковые цепи молекулы обеспечивают ему более длительный период полувыведения, чем природное вещество. Вещество применяется инкапсулированным в липосомы (L-MTP-PE). Будучи фосфолипидом , он накапливается в липидном бислое липосом в инфузии. [11]
Синтез
Один из методов синтеза (показан первым) основан на этерификации N -ацетилмурамил- L -аланил- D -изоглутаминил - L -аланина с N -гидроксисукцинимидом с последующей конденсацией с 2-аминоэтил-2,3-дипальмитоилглицерилфосфорной кислотой в триэтиламине ( Et 3 N ). [12] Другой подход (показан вторым) использует N -ацетилмурамил- L -аланил- D -изоглутамин, гидроксисукцинимид и аланил-2-аминоэтил-2,3-дипальмитоилглицерилфосфорную кислоту; [13] то есть аланин вводится на втором этапе вместо первого.
 |  |
История
Препарат был изобретен Ciba-Geigy (теперь Novartis ) в начале 1980-х и продан Jenner Biotherapies в 1990-х. В 2003 году IDM Pharma выкупила права и продолжила его разработку. [1] IDM Pharma была приобретена Takeda вместе с мифамуртидом в июне 2009 года. [14]
Мифамуртид уже получил статус орфанного препарата от Управления по контролю за продуктами и лекарствами США (FDA) в 2001 году, а Европейское агентство по лекарственным средствам (EMA) последовало за ним в 2004 году. Он был одобрен в 27 государствах-членах Европейского союза , а также Исландии, Лихтенштейне и Норвегии централизованным разрешением на продажу в марте 2009 года. Препарату было отказано в одобрении FDA в 2007 году. [15] [16] Мифамуртид был лицензирован EMA с марта 2009 года. [17]
Ссылки
- ^ abcd "Мифамуртид: CGP 19835, CGP 19835A, L-MTP-PE, липосомальный MTP-PE, MLV 19835A, MTP-PE, мурамилтрипептид фосфатидилэтаноламин". Лекарственные препараты в исследованиях и разработках . 9 (2): 131– 5. 2008. doi :10.2165/00126839-200809020-00007. PMID 18298131.
- ^ ab EMA (2009-03-06). "Mepact: Информация о продукте. Приложение I: Краткое описание характеристик продукта" (PDF) . стр. 2 . Получено 2009-11-12 .[ мертвая ссылка ]
- ^ EMA (2009-05-06). "Mepact: Европейский общественный оценочный отчет. Резюме для общественности" (PDF) . стр. 1. Получено 2016-10-06 .
- ^ Meyers PA (август 2009 г.). «Мурамилтрипептид (мифамуртид) для лечения остеосаркомы». Expert Review of Anticancer Therapy . 9 (8): 1035– 49. doi :10.1586/era.09.69. PMID 19671023. S2CID 29512704.
- ^ Meyers PA, Schwartz CL, Krailo MD, Healey JH, Bernstein ML, Betcher D и др. (Февраль 2008 г.). «Остеосаркома: добавление мурамилтрипептида к химиотерапии улучшает общую выживаемость — отчет Детской онкологической группы». Журнал клинической онкологии . 26 (4): 633– 8. doi : 10.1200/JCO.2008.14.0095 . PMID 18235123.
- ^ Meyers PA, Schwartz CL, Krailo M, Kleinerman ES, Betcher D, Bernstein ML и др. (март 2005 г.). «Остеосаркома: рандомизированное проспективное исследование добавления ифосфамида и/или мурамилтрипептида к цисплатину, доксорубицину и метотрексату в высоких дозах». Журнал клинической онкологии . 23 (9): 2004–11 . doi : 10.1200/JCO.2005.06.031 . PMID 15774791.
- ^ (EMA & 06.03.2009, стр. 5–7)
- ^ (EMA & 2009-03-06, стр. 4)
- ^ (EMA & 06.03.2009, стр. 7–8)
- ^ (EMA & 2009-03-06, стр. 8)
- ^ Fidler IJ, Sone S, Fogler WE, Smith D, Braun DG, Tarcsay L, Gisler RH, Schroit AJ (1982). «Эффективность липосом, содержащих липофильное производное мурамилдипептида, для активации противоопухолевых свойств альвеолярных макрофагов in vivo». Журнал иммунотерапии . 1 (1): 43–55 .
- ^ Prous J, Castaner J (1989). "ENV 2-3/MTP-PE". Лекарства будущего . 14 (3): 220. doi :10.1358/dof.1989.014.03.85085.
- ^ Brundish DE, Wade R (1985). «Синтез N-[2-3H]ацетил-D-мурамил-L-аланил-D-изо-глутаминил-L-аланил-2-(1',2'-дипальмитоил-sn-глицеро-3'-фосфорил)этиламида высокой удельной радиоактивности». J Label Compd Radiopharm . 22 (1): 29– 35. doi :10.1002/jlcr.2580220105.
- ^ "Первое лечение, повышающее выживаемость за 20 лет, теперь доступно для пациентов с остеосаркомой (раком костей)". Takeda. Ноябрь 2009 г. Получено 23 марта 2010 г.
- ^ "Препарат MEPACT (Mifamurtide, L-MTP-PE) компании IDM Pharma получил одобрение в Европе для лечения пациентов с неметастатической резектабельной остеосаркомой" (пресс-релиз). PR Newswire. 2009-03-09 . Получено 2009-11-12 .
- ^ "IDM Pharma получает неодобрительное письмо на Mifamurtide для лечения остеосаркомы". The Medical News. 2007-08-28 . Получено 2009-11-12 .
- ^ Mepact для специалистов здравоохранения , получено 12 ноября 2009 г.