Низкобарьерная водородная связь
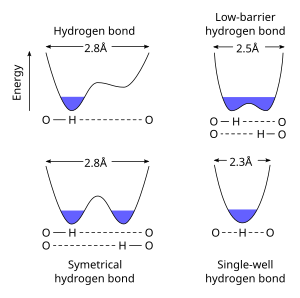
Низкобарьерная водородная связь ( LBHB ) — это особый тип водородной связи . LBHB могут возникать, когда pKa двух гетероатомов близко совпадают, что позволяет водороду распределяться между ними более равномерно. Такое распределение водорода приводит к образованию особенно коротких и прочных водородных связей. [1]
Описание

Стандартные водородные связи длиннее (например, 2,8 Å для связи O···O h), и ион водорода явно принадлежит одному из гетероатомов . Когда pKa гетероатомов близко соответствует, LBHB становится возможным на более коротком расстоянии (~2,55 Å). Когда расстояние еще больше уменьшается (< 2,29 Å), связь характеризуется как одноямная или короткая-сильная водородная связь. [3]
Белки
Водородные связи с низким барьером возникают в среде белков, исключающей воду. [4] Несколько остатков действуют вместе в системе передачи заряда, чтобы контролировать значения pKa задействованных остатков. LBHB также возникают на поверхности белков, но они нестабильны из-за их близости к объемной воде и противоречивых требований сильных солевых мостиков в интерфейсах белок-белок. [4]
Ферментативный катализ
Низкобарьерные водородные связи были предложены как имеющие отношение к ферментативному катализу в двух типах обстоятельств. [5] Во-первых, низкобарьерная водородная связь в сети передачи заряда в активном центре может активировать каталитический остаток (например, между кислотой и основанием в каталитической триаде ). Во-вторых, LBHB может образовываться во время катализа для стабилизации переходного состояния (например, с переходным состоянием субстрата в оксианионном отверстии ). Оба эти механизма являются спорными, и теоретические и экспериментальные данные о том, происходят ли они, разделились. [6] [7] С 2000-х годов общее согласие заключалось в том, что LBHB не используются ферментами для содействия катализу. [7] [8] Однако в 2012 году было предложено, что низкобарьерная водородная связь участвует в фосфатно-арсенатной дискриминации для белка-транспортера фосфата. [9] Это открытие может указывать на возможность того, что низкобарьерные водородные связи играют каталитическую роль в выборе размера иона в некоторых очень редких случаях.
Ссылки
- ^ Джилли, Г.; Джилли, П. (2000-09-26). «К единой теории водородной связи». Журнал молекулярной структуры . 552 ( 1–3 ): 1–15 . Bibcode : 2000JMoSt.552....1G. doi : 10.1016/S0022-2860(00)00454-3.
- ^ Day, Victor W.; Hossain, Md. Alamgir; Kang, Sung Ok; Powell, Douglas; Lushington, Gerald; Bowman-James, Kristin (2007). «Encircled Proton». J. Am. Chem. Soc. 129 (28): 8692– 3. doi :10.1021/ja0724745. PMID 17585768.
- ^ Schiøtt B, Iversen BB, Madsen GK, Larsen FK, Bruice TC (октябрь 1998 г.). «Об электронной природе водородных связей с низким барьером в ферментативных реакциях». Proc. Natl. Acad. Sci. USA . 95 (22): 12799– 802. Bibcode :1998PNAS...9512799S. doi : 10.1073/pnas.95.22.12799 . PMC 23598 . PMID 9788994.
- ^ ab Ishikita, Hiroshi; Saito, Keisuke (2014-02-06). "Реакции переноса протонов и сети водородных связей в белковых средах". Journal of the Royal Society Interface . 11 (91): 20130518. doi :10.1098/rsif.2013.0518. ISSN 1742-5689. PMC 3869154. PMID 24284891 .
- ^ Cleland, WW; Frey, PA; Gerlt, JA (2 октября 1998 г.). «Низкобарьерная водородная связь в ферментативном катализе». Журнал биологической химии . 273 (40): 25529– 25532. doi : 10.1074/jbc.273.40.25529 . PMID 9748211.
- ^ Эш, EL (7 ноября 1997 г.). «Низкобарьерная водородная связь в каталитической триаде сериновых протеаз? Теория против эксперимента». Science . 278 (5340): 1128– 1132. Bibcode :1997Sci...278.1128A. doi :10.1126/science.278.5340.1128. PMID 9353195.
- ^ ab Schutz, Claudia N.; Warshel, Arieh (1 апреля 2004 г.). «Повторное рассмотрение предложения о водородной связи с низким барьером (LBHB): случай пары Asp ··· His в сериновых протеазах». Белки: структура, функция и биоинформатика . 55 (3): 711– 723. doi :10.1002/prot.20096. PMID 15103633. S2CID 34229297.
- ^ Warshel, Arieh; Sharma, Pankaz K.; Kato, Mitsunori; Xiang, Yun; Liu, Hanbin; Olsson, Mats HM (август 2006 г.). «Электростатическая основа ферментативного катализа». Chemical Reviews . 106 (8): 3210– 3235. doi :10.1021/cr0503106. PMID 16895325.
- ^ Элиас, Микаэль; Веллнер, Алон; Голдин-Азулай, Корина; Шабриер, Эрик; Ворхольт, Джулия А.; Эрб, Тобиас Дж.; Тауфик, Дэн С. (1 ноября 2012 г.). «Молекулярная основа дискриминации фосфатов в средах, богатых арсенатом». Природа . 491 (7422): 134–137 . Бибкод : 2012Natur.491..134E. дои : 10.1038/nature11517. ISSN 0028-0836. PMID 23034649. S2CID 205230854.