- Преобладающие виды мышьяка выщелачиваются при высоком pH как . Константа диссоциации: см. Свойства мышьяковой кислоты .
- Преобладающие виды свинца выщелачиваются при низком pH как . Pb(OH) 2 Pb 2+ (водн.) + 2OH − (водн.) : Ksp = 2,8* 10 −16
- Сурьма не показывает большой зависимости от pH. Преобладающим выщелачиваемым видом является форма. Растворимость Sb(V) = 20 г/л
Разметка дорожного покрытия стеклянными шариками
Примеры и точка зрения в этой статье могут не отражать всемирный взгляд на предмет . ( Май 2022 ) |


Стеклянные шарики, состоящие из натриево-кальциевого стекла, необходимы для обеспечения световозвращающей способности во многих видах дорожной разметки . [1] Световозвращающая способность возникает, когда падающий свет от транспортных средств преломляется в стеклянных шариках, которые встроены в дорожную разметку , а затем отражаются обратно в поле зрения водителя. [2] В Северной Америке ежегодно для дорожной разметки используется около 227 миллионов килограммов стеклянных шариков. [3] Примерно 520 килограммов стеклянных шариков используется на милю при разметке пятиполосной автомагистрали, [4] а разметка дорог может проводиться каждые два-пять лет. [4] В Соединенных Штатах огромный спрос на стеклянные шарики привел к импорту из стран, использующих устаревшие производственные правила и технологии.
Эти методы включают использование тяжелых металлов, таких как мышьяк , сурьма и свинец, в процессе производства в качестве обесцвечивающих и осветляющих агентов. Было обнаружено, что тяжелые металлы включаются в стеклянную матрицу шарика и могут выщелачиваться в условиях окружающей среды, в которых находятся дороги. [5]
Состав и производство

Синтез этих гранул начинается при нагревании карбоната кальция до температуры от 800 до 1300 °C. Нагревание вызывает реакцию разложения, в результате которой образуется твердый оксид кальция и выделяется углекислый газ.
Аналогично карбонат натрия разлагается до оксида натрия и выделяет углекислый газ.
Затем оксид натрия реагирует с кремнием, образуя жидкое стекло из силиката натрия.
Наконец, для завершения общей структуры натриево-кальциевого стекла, оксид кальция растворяется в растворе с натриево-силикатным стеклом, что в конечном итоге снижает температуру размягчения стекла. [6] Дополнительные металлы и ионы добавляются к этому расплавленному стеклу для улучшения его свойств, а затем соединение распыляется и формируется в шарики с использованием либо прямого, либо косвенного метода.
В целом, процентный состав основных соединений, обнаруженных в конечном продукте из стеклянных шариков, показан ниже. [3]
| Сложный | % Состав |
| 70-75% | |
| 11-15% | |
| 2-4% | |
| 6-10% | |
| 1-2% |
В дополнение к этим основным компонентам натриево-кальциевого стекла производители включают тяжелые металлы мышьяк, сурьму и свинец для очистки и улучшения свойств стеклянных шариков. Свинец в форме PbO добавляется для повышения прочности стекла и его способности выдерживать суровые дорожные условия. [8] Мышьяк и сурьма используются в качестве осветлителей, которые облегчают удаление пузырьков газа из расплавленной смеси. [9] Диоксид углерода, образующийся при разложении карбоната кальция и карбоната натрия, удаляется для получения требуемых световозвращающих свойств стекла. Кроме того, как мышьяк, так и сурьма используются в качестве обесцвечивателей. Наличие бесцветного стекла имеет решающее значение для максимального увеличения световозвращающей способности. Мышьяк в своей неорганической форме способствует обесцвечиванию стекла, контролируя степень окисления железа. [3] Мышьяк окисляет оксид железа до его менее красочного аналога, оксида железа.
Сурьма в форме Sb 2 O 5 осуществляет реакцию, похожую на реакцию мышьяка, окисляя оксид железа до оксида железа.
Хотя эти три тяжелых металла обычно можно найти как в отечественных, так и в импортных стеклянных шариках, их концентрация различается. Согласно Агентству по охране окружающей среды США , Закон о сохранении и восстановлении ресурсов ограничивает уровни содержания тяжелых металлов в соответствии с их токсичностью. [11] Однако из-за растущего спроса на размеченные дороги большинство стеклянных шариков, используемых в США, импортируется из стран, где практически нет регулирования содержания тяжелых металлов. Например, шарики, полученные из Северной Америки, содержат приблизительно 15 мг мышьяка на кг шариков, в то время как некоторые из Китая имеют концентрацию до 1000 мг/кг. [3] Концентрации импортируемых шариков каждого из этих металлов указаны в таблице ниже.
| Металл/Металлоид | Концентрация (мг/кг) |
| 103-683 | |
| 23-179 | |
| 62-187 |
Деградация стеклянных шариков
Условия окружающей среды могут вызвать деградацию стеклянных шариков, что приведет к выбросу включенных в них тяжелых металлов в окружающую среду. [3] Хотя истирание может привести к смещению этих шариков с дорожной разметки, реакция этих шариков с водной средой значительно ускоряет их разложение и выброс тяжелых металлов.
В коррозии диоксида кремния участвуют три реакции. Первая — это реакция ионного обмена, в которой подвижные ионы раствора обмениваются на ионы с аналогичным зарядом в твердом теле. В частности, эта реакция включает катионообменный материал, где отрицательно заряженный структурный остов позволяет заменять положительно заряженные катионы. [12] Эта реакция, участвующая в деградации гранул натронной извести, показывает, что различные ионы, которые взаимодействуют с кремниево-кислородной сетью (например , , , , ), заменяются ионом водорода.
В дополнение к этой реакции гидроксильный ион может атаковать связь, вызывая растворение матрицы и создавая силанольные и немостиковые кислородные группы.
По мере растворения немостиковые кислородные группы могут отрывать ионы водорода от раствора.
Увеличение концентрации гидроксильных ионов сопровождается повышением щелочности водного раствора. Это увеличение pH, как показали различные исследования выщелачивания в колонках, увеличивает восстановительный потенциал и концентрацию DOC (растворенного органического углерода) в растворе. Это в конечном итоге приводит к повышению подвижности многих металлов, включая мышьяк, медь и никель.
Таким образом, подвижность этих тяжелых металлов зависит от присутствия щелочных оксидов. Ионы , , , и могут связываться с тетраэдрическими сетками кремния и кислорода, образуя тригональную антипризменную сетку. При образовании тригональной антипризмы ионы координируются с тремя атомами кислорода на расстоянии 2,3 ангстрема, а затем еще с тремя атомами кислорода на несвязывающем расстоянии 3 ангстрема. По мере увеличения концентрации щелочных оксидов в металлических шариках вероятность химической атаки увеличивается из-за более открытой и доступной химической сети и структуры стекла. [3]
Видообразование и выщелачивание тяжелых металлов
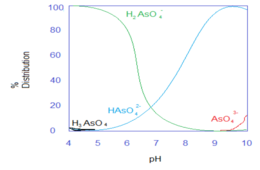
Как при обычном удалении дорожной разметки, так и в суровых условиях окружающей среды эти стеклянные шарики могут разлагаться и выщелачивать включенные тяжелые металлы. Хотя точный механизм включения тяжелых металлов в стеклянные шарики неизвестен, в современной литературе выдвигается гипотеза, что тяжелые металлы связаны со щелочными и щелочноземельными металлами на поверхности стеклянных шариков. Экологические условия, имеющие отношение к дорожным покрытиям, такие как pH, различные соли и ионная сила, сильно влияют на процесс выщелачивания. В частности, pH определяет видообразование тяжелого металла, что имеет решающее значение для растворимости в водной фазе. На следующих графиках показано видообразование тяжелых металлов в зависимости от pH. [3]
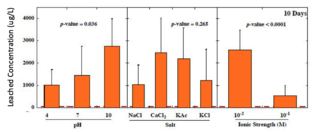
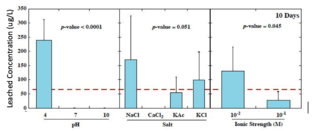
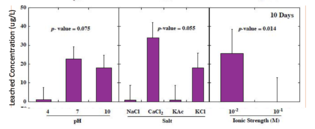
В немногих штатах существуют правила по выщелоченным концентрациям тяжелых металлов. Например, в Нью-Джерси мышьяк ограничен 3 мкг/л, свинец — 65 мкг/л, а сурьма — 78 мкг/л. В исследованиях, в которых партии стеклянных шариков подвергались воздействию условий окружающей среды в лабораторных условиях, 96% выщелоченных концентраций мышьяка превысили 3 мкг/л, 75% выщелоченного свинца превысили 65 мкг/л, а 27% выщелоченных концентраций сурьмы превысили критерий 78 мкг/л. [13] На следующих графиках показаны общие концентрации тяжелых металлов, выщелоченных из стеклянных шариков через 160 дней, в зависимости от pH, типа соли и ионной силы. [3]
- Концентрации выщелоченного мышьяка значительно выше при низкой ионной силе и хлоридных солях. Незначительная разница на основе pH.
- Концентрации выщелоченного свинца значительно выше при низком pH, низкой ионной силе и хлоридных солях.
- Концентрации выщелоченной сурьмы значительно выше при низкой ионной силе. Незначительная разница в зависимости от pH или типа соли.
Взаимодействие с придорожной почвой
После того, как мышьяк мобилизуется в водной форме, гуминовые вещества взаимодействуют с мышьяком. Было показано, что, особенно в кислых средах, гуминовые кислоты вносят огромный вклад в удержание мышьяка в почвенной матрице. [14] Хотя точный механизм этого не был подтвержден, была выдвинута гипотеза, что гуминовые кислоты действуют как анионообменные фрагменты, потенциально через взаимодействие амина в гуминовом материале с мышьяком. Это вероятно только в том случае, если амин является четвертичным, что оправдывает заявление о низком pH, поскольку для разделения As(III) и As(V) используются похожие смолы. Другой возможный механизм взаимодействия мышьяка с гуминовыми веществами - через комплексы металлов. Потенциально адсорбция мышьяка может происходить как связующий лиганд гуминовая кислота-металл-As или, возможно, адсорбироваться на глине, которая также связана с самой гуминовой кислотой. [15]
Свинец, с другой стороны, как было показано, увеличивает связывание с гуминовыми веществами с ростом pH и снижением ионной силы. Исследования показали, что монодентатный свинец связывается в относительно высокой степени с группами карбоксильного типа, присутствующими в гуминовых материалах. Также имеются данные о бидентатной форме связывания свинца с группами фенольного типа в орто-положении в гуминовом материале, когда концентрации свинца высоки, как в случае почв вблизи размеченных дорог. [16]
В случае антиномии качественные исследования ее связи с гуминовыми веществами редки и редко дают окончательные результаты. Однако во многих случаях было показано, что pH мало указывает на эти взаимодействия. Одно исследование показало, что органические лиганды, которые обладают карбоксильными группами или гидроксильными группами, создают стабильные бидентатные хелаты в его виде As(III) и As(V). Другое показало, что As(III) при связывании с гуминовым материалом легко окисляется и может быть высвобождаем обратно в водный раствор в виде (SbOH)6-, тем самым показывая, что As(V) чаще связывается с гуминовым материалом. Детали того, как это связывание происходит механически, остаются относительно нерешенными, но знание первичной формы его связывания важно для дальнейшего исследования. [17]
Альтернатива использованию тяжелых металлов
Световозвращаемость имеет важное значение для безопасных условий вождения. Хотя металлы необходимы для достижения этих целей, существуют и другие, нетоксичные металлы, которые могут достичь тех же результатов. К ним могут относиться цирконий, вольфрам, титан и барий. [18] Количество этих металлов, которые могут быть включены в стекло, варьируется в зависимости от страны его происхождения и правил, установленных в этих странах, но дальнейшие исследования альтернатив использованию тяжелых металлов в дорожной разметке помогут сократить выщелачивание тяжелых металлов вблизи придорожных почв.
Смотрите также
Ссылки
- ^ Mangalgirl, KP (2012). Тяжелые металлы в стеклянных шариках, используемых в дорожной разметке. Диссертация на степень магистра наук, Техасский университет A&M, Колледж-Стейшн, Техас.
- ^ dos Santos, EJ; Hermann, AB; Prado, SK; Fantin, EB; dos Santos, VW; de Oliveira, AVM; Curtius, AJ (2013). Определение токсичных элементов в стеклянных шариках, используемых для разметки дорожного покрытия, методом ICP OES. Microchemical Journal. 108: 233-238.
- ^ abcdefgh Sandhu, NK (2012). Выщелачивание металлов и металлоидов из стеклянных шариков для разметки автомагистралей и потенциальное воздействие на окружающую среду. Докторская диссертация, Технологический институт Нью-Джерси, Ньюарк, Нью-Джерси.
- ^ ab Буланже, Б.; Карлсон, П.; Фаткин, Х.; и Раут-Десаи, А. (2014). Оценка уровня скрининга концентраций мышьяка и свинца в стеклянных шариках, используемых в дорожной разметке. Министерство транспорта США. Публикация № FHWA-HRT-14-021.
- ^ Джахан, К., НК Сандху, Л.Б. Экс, П.К. Ндиба, К.В. Рамануджачари и Т.Ф. Магделано. 2010. Загрязнение тяжелыми металлами стеклянных шариков для разметки автомагистралей. Нью-Джерси: Департамент транспорта Нью-Джерси.
- ^ Уэллер, М., Овертон, Т., Рурк, Дж. и Армстронг, Ф. (2014). Неорганическая химия. Оксфорд, Великобритания. Oxford University Press.
- ^ Ducheyne, P., Healy, K., Hutmacher, D., Grainger, DW, and Kirkpatrick, CJ (2015). Comprehensive Biomaterials . Амстердам, Нидерланды. Elsevier.
- ^ Sidek, HAA, El-Mallawany, R., Matori, KA, & Halimah, MK (2016). Влияние PbO на упругое поведение стеклянных систем ZnO-P2O5. Результаты по физике . 6: 449-455.
- ^ Хуёва, М. и Вернерова, М. (2017). Влияние осветляющих веществ на плавление стекла: обзор, часть I. Керамика-Силикаты. 61(2): 119-126.
- ^ ab P. Stone, E. Egan и J. Lehr. Диоксид церия как осветляющий агент и обесцвечиватель для стекла. Журнал Американского керамического общества . 39, № 3 (1956).
- ^ US EPA (1991b). Процедура выщелачивания характеристик токсичности (TCLP). Метод 1311, Федеральный регистр , 55 (29 марта), Вашингтон, округ Колумбия
- ^ Кумар, С. и Джейн, С. (2013). История, введение и кинетика ионообменных материалов. Журнал химии. 2013: 1-13.
- ^ Сандху, НК; Акс, Л.; Джахан, К.; Рамануджачари, К.В., Кулахан, К. (2013). Влияние на окружающую среду выщелачивания металлов и металлоидов из стеклянных шариков для дорожной разметки. ACS Environmental Science Technology. 47:4383-4391.
- ^ Бушманн, Дж., Каппелер, А., Линдауэр, У., Кистлер, Д., Берг, М. и Сигг, Л. (2006). Связывание арсенита и арсената с растворенными гуминовыми кислотами: влияние pH, типа гуминовой кислоты и алюминия. Наука об окружающей среде и технология . 40(19): 6015-6020.
- ^ Наиду, Рави (2006). Управление мышьяком в окружающей среде: от почвы до здоровья человека . Коллингвуд, Австралия: CSIRO Publishing. С. 120–124.
- ^ Xiong, J., Koopal, LK, Tan, W., Fang, L., Wang, M., Zhao, W., Liu, F., Zhang, J., & Weng, L. (2013). Связывание свинца с фульвокислотами и гуминовыми кислотами почвы: моделирование NICA-Donnan и спектроскопия XAFS. Наука об окружающей среде и технологии . 47(20): 11634-11642.
- ^ Хокманн, К. (2014). «Выщелачивание сурьмы из загрязненной нефти при изменяющихся окислительно-восстановительных условиях». Исследовательская коллекция ETH Zurich . 21685 .
- ^ Хейден, Дж. С. (2004). «Экологически чистые оптические стекла». Optics and Photonics News , 15 (8), 36-41.
Внешние ссылки
- Федеральное управление автомобильных дорог США — Узнайте больше о дорожной разметке


![{\displaystyle {\ce {CaCO3 ->[{800-1300C}]{CaO(т)}+ CO2(г)}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/b5cb484d3646dade0e69a0ab3d7a7c8e687c4f54)
![{\displaystyle {\ce {Na2CO3 -> [{800-1300C}] {Na2O(тв)}+ CO2(г)}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/fed65d1f113f3b74aea0724141253e1786d3f9a6)