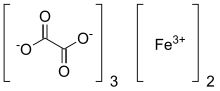
Оксалат железа
 | |
| Имена | |
|---|---|
| Систематическое название ИЮПАК железа(3+) этандиоат (2:3) | |
| Другие имена Оксалат железа(III) | |
| Идентификаторы | |
3D модель ( JSmol ) |
|
| ChemSpider |
|
| Информационная карта ECHA | 100.019.047 |
| Номер ЕС |
|
CID PubChem |
|
| УНИИ | |
Панель инструментов CompTox ( EPA ) |
|
| |
| |
| Характеристики | |
| С6Фе2О12 | |
| Молярная масса | 375,747 г/моль |
| Появление | Бледно-желтое твердое вещество (безводное) Лаймово-зеленое твердое вещество (гексагидрат) |
| Запах | без запаха |
| Температура плавления | 365,1 °C (689,2 °F) |
| слабо растворимый | |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |
Оксалат железа , также известный как оксалат железа(III) , относится к неорганическим соединениям с формулой Fe2 ( C2O4 ) 3 ( H2O ) x , но также может относиться к солям [Fe( C2O4 ) 3 ] 3- . Fe2 ( C2O4 ) 3 ( H2O ) x являются координационными полимерами с различной степенью гидратации. Координационный комплекс с формулой [Fe( C2O4 ) 3 ] 3- образует различные соли, хорошо известным примером которых является ферриоксалат калия . В этой статье особое внимание уделяется координационным полимерам.
Структура
Тетрагидрат
3hydrate.jpg/440px-Fe2(ox)3hydrate.jpg)

Согласно рентгеновской кристаллографии тетрагидрата Fe 2 (C 2 O 4 ) 3 · 4 H 2 O , железо является октаэдрическим. Оксалатные лиганды являются мостиковыми . Некоторые через все четыре атома кислорода, некоторые через два атома кислорода. Половина воды является решеточной водой , находясь между цепями оксалатов Fe. Мессбауэровский спектр Fe 2 (C 2 O 4 ) 3 · 4 H 2 O показывает изомерный сдвиг 0,38 мм/с и квадрупольное расщепление 0,40 мм/с, что предполагает высокий спин Fe 3+ в октаэдрической координации. [1] [2]
Производство
Оксалат железа может быть получен реакцией гидроксида железа (III) и раствора щавелевой кислоты :
- 2Fe ( OH ) 3 + 3H2C2O4 → Fe2 ( C2O4 ) 3 + 6H2O
Использует
Стоматология
Как и многие оксалаты, оксалат железа исследовался в качестве краткосрочного средства для лечения гиперчувствительности дентина . [3] Он используется в некоторых составах зубных паст; однако его эффективность подвергается сомнению. [4]
Фотография
Оксалат железа используется в качестве светочувствительного элемента в процессе фотографической печати Каллитип , а также в процессе платинотипной печати Платина/Палладий.
Аккумуляторы
Тетрагидрат оксалата железа исследовался как возможный дешевый материал для положительного электрода литий-железных аккумуляторов. Он может интеркалировать ионы лития при среднем потенциале 3,35 В и показал устойчивую емкость 98 мАч/г. [1]
Органический синтез
Гексагидрат оксалата железа используется с боргидридом натрия для радикальных реакций гидрофункционализации алкенов по Марковникову . [5]
Смотрите также
Известен ряд других оксалатов железа:
Ссылки
- ^ аб Ахуари, Ханья; Русе, Гвеналь; Родригес-Карвахаль, Хуан; Суграти, Мулай-Тахар; Собанер, Матье; Корти, Матье; Рехам, Надир; Тараскон, Жан-Мари (2015). «Раскрытие структуры тетрагидрата оксалата железа (III) и его способности к обратимому внедрению лития». Химия материалов . 27 (5): 1631–1639. дои : 10.1021/см5043149.
- ^ Русс, Г.; Родригес-Карвахаль, Х. (2016). «Оксалатно-опосредованный дальний антиферромагнетизм в Fe2 ( C2O4 ) 3 · 4H2O » . Dalton Transactions . 45 (36): 14311–14319. doi : 10.1039 /C6DT02740G. PMID 27539964 .
- ^ Gillam, DG; Newman, HN; Davies, EH; Bulman, JS; Troullos, ES; Curro, FA (2004). «Клиническая оценка оксалата железа для снятия гиперчувствительности дентина». Журнал оральной реабилитации . 31 (3): 245–250. doi :10.1046/j.0305-182X.2003.01230.x. PMID 15025657.
- ^ Cunha-Cruz, J.; Stout, JR; Heaton, LJ; Wataha, JC (29 декабря 2010 г.). «Гиперчувствительность дентина и оксалаты: систематический обзор». Journal of Dental Research . 90 (3): 304–310. doi :10.1177/0022034510389179. PMC 3144108. PMID 21191127 .
- ^ Баркер, Тимоти (2001-04-15). "Гексагидрат оксалата железа". Энциклопедия реагентов для органического синтеза (1-е изд.). Wiley. стр. 1–4. doi :10.1002/047084289X.rn02346. ISBN 978-0-471-93623-7. S2CID 225482606.
