Дэвид Э. Клеммер
Дэвид Э. Клеммер | |
|---|---|
 | |
| Рожденный | ( 1965-02-23 )23 февраля 1965 г. |
| Альма-матер | |
| Известный | Спектрометрия подвижности ионов , масс-спектрометрия |
| Награды | Медаль Биемана , премия Американского химического общества за достижения в области химического приборостроения |
| Научная карьера | |
| Поля | Аналитическая химия , масс-спектрометрия |
| Учреждения | Университет Индианы в Блумингтоне |
| научный руководитель | Питер Б. Арментроут |
| Веб-сайт | www.indiana.edu/~clemmer/home.htm |
Дэвид Э. Клеммер (23 февраля 1965 г., Аламоса, Колорадо ) — химик-аналитик, заслуженный профессор и заведующий кафедрой химии Роберта и Марджори Манн в Индианском университете в Блумингтоне, штат Индиана , где он возглавляет группу Клеммера. [1] Клеммер разрабатывает новые научные приборы для масс-спектрометрии подвижности ионов (IMS/MS), включая первый прибор для вложенной времяпролетной масс- спектрометрии подвижности ионов. [2] Он получил ряд наград, включая медаль Бимана в 2006 году «за его новаторский вклад в интеграцию разделения подвижности ионов с различными технологиями масс-спектрометрии». [3]
Ранняя жизнь и образование
Клеммер родился 23 февраля 1965 года в семье художника Эда Клеммера и его жены Мэри-Энн, учительницы, в Аламосе, штат Колорадо . [4] Он учился в Adams State College , где изначально специализировался на музыке, а затем перешел на науку. [4] Он получил степень бакалавра по химии с отличием в 1987 году. Затем он поступил в Университет Юты , где в 1992 году получил степень доктора философии по физической химии. [5] Его научным руководителем был Питер Б. Арментроут , [2] с которым он изучал ионы переходных металлов в газообразных реакциях. [3]
Карьера
В 1992–1993 годах Клеммер был постдокторантом в Японии, поддерживаемым стипендией Японского общества содействия развитию науки в Технологическом институте Химедзи . Он работал с Кэндзи Хонмой над механизмами переноса электронов [6] и реакциями атомов металлов в возбужденном состоянии и газообразных молекул. [3] С 1993 по 1995 год Клеммер был постдокторантом в Северо-Западном университете , где он работал с Мартином Ф. Джарролдом [3] , изучая сворачивание и конформацию белков в газовой фазе, используя такие методы, как спектрометрия ионной подвижности . [7] [8]
В 1995 году Клеммер присоединился к химическому факультету Индианского университета. [3] Он занимал должность заведующего химическим факультетом с 2002 по 2006 год. [9] Он является полным профессором и занимает кафедру химии Роберта и Марджори Манн, на которую он был назначен в 2002 году. [3] [5] Он опубликовал более 230 статей. [1]
Среди тех, кто оказал на него влияние, он называет Майкла Т. Бауэрса , Джесси Л. Бошампа , Р. Грэма Кукса , Скотта А. Маклаки , Фреда Маклафферти , Эвана Р. Уильямса, Джозефа А. Лу, Вики Высоцки и Джули А. Лири . [2] Среди его аспирантов были Рена А. С. Робинсон , Стивен Валентайн, Чероки Хоаглунд-Хайзер [10] и Кэтрин Сребалус Барнс. [11]
Исследовать
Клеммер особенно заинтересован в изучении структурной характеристики и конформационной динамики сложных низкосимметричных систем. Клеммер разрабатывает научные приборы и методы для исследования биомолекулярной структуры и сложных биомолекулярных смесей в газовой фазе с использованием спектрометрии ионной подвижности. [11]
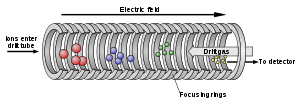
Методы ионной подвижности разделяют ионы на различные группы на основе их способности перемещаться через электрически заряженный буферный газ. Это позволяет дифференцировать сложные смеси способами, которые не могут быть достигнуты только с помощью масс-спектрометрии. Даже мельчайшие количества соединений могут быть различены и дифференциально исследованы в соответствии с такими характеристиками, как размер, форма и заряд, а также масса. [2]
Клеммер помог установить подвижность ионов как мощный инструмент и область исследований посредством своих «тщательных исследований» и «революционных инструментальных методов». [3] В ранних работах Клеммер и Джарролд использовали длинные дрейфовые трубки с некластеризованными газовыми атмосферами для увеличения разрешающей способности спектрометрии ионной подвижности. [12] Работа Клеммера по методам разделения газовой фазы для масс-спектрометрии ионной подвижности (IM-MS) и их применение к структурному анализу интактных белков считается «особенно важной вехой» в применении IM-MS к исследованию биомолекулярных структур. [13] [14] [15] Клеммер и его коллеги разработали по меньшей мере дюжину различных конфигураций, объединяющих модульные компоненты для подвижности ионов с приборами масс-спектрометрии. [2] [16] К ним относится объединение подвижности ионов с времяпролетной масс-спектрометрией (TOF). [17] [18] [19] Они также разработали первый прибор для вложенной ионной подвижности масс -спектрометрии времени пролета . [2] [5]
Такое оборудование позволяет исследователям больше узнать как о структурах, так и о конформационной динамике систем. [20] Клеммер определил фундаментальные связи между зарядовыми состояниями и структурами и показал, что одно зарядовое состояние может существовать в более чем одной конформации в газообразных состояниях. [3] Такие методы можно использовать для изучения как белков, так и пептидов. [21] [3] В ранних работах Клеммер показал, что множественные конформации цитохрома c гемпротеина можно дифференцировать на основе их подвижности. [22] Кроме того, подвижность различных хиральных изомеров была связана с их белковым сворачиванием. [23] Более поздние методы позволяют исследователям отслеживать переходы в конформациях макромолекулярных ионов во время газовой фазы. Короткий импульс ионов вводится в дрейфовую трубку с помощью электрораспылительной ионизации. Структуры разделяются на основе различий в их подвижностях. Подвергая определенные состояния энергетическим столкновениям, можно устанавливать новые структуры и отслеживать их через различные конформационные изменения. Изменения в конформации во время данных газовой фазы затем могут быть сопоставлены с исходными популяциями структур. Таким образом, исследователи могут понять возможные пути между структурами. [24]
Понимание того, как происходит сворачивание белка в трехмерных молекулах, является одной из постоянных проблем биологии. Белки с различной формой часто имеют очень разную биологическую активность и медицинскую полезность. [5] Работа Клеммера имеет применение в науках о жизни для понимания конформации структур в больших белковых комплексах, [5] профилирования протеома плазмы, [13] изучения роли белков и сворачивания белка при нейродегенеративных заболеваниях, [5] выявления возможных маркеров, связанных с раком, в крови, моче или слюне, [4] и повышения эффективности открытия лекарств. [25] Методы масс-спектрометрии ионной подвижности также позволяют измерять и коррелировать широкий спектр различных характеристик одновременно в одном анализе. Исследователи могут использовать эти методы для изучения сложных биологических образцов для получения информации о липидомике , протеомике , гликомике и метаболомике . [13]
Компании
Клеммер является соучредителем Beyond Genomics , компании, занимающейся системной биологией, и основателем Predictive Physiology and Medicine , биотехнологической компании, специализирующейся на персонализированной медицине . [4]
Увлечения
Помимо игры на нескольких инструментах, Клеммер любит бегать марафоны. [2]
Награды и почести
- 2023, Премия Филда и Франклина за выдающиеся достижения в области масс-спектрометрии [26]
- 2022, Медаль Уайли за инновации [27]
- 2020, Лауреат медали Двухсотлетия [27]
- 2018, выдающийся вклад Джона Б. Фенна, совместно с Мартином Ф. Джарролдом [28] и Гертом фон Хельденом [29] , Американское общество масс-спектрометрии [30]
- 2017, член Национальной академии изобретателей [31]
- 2014–2015, Премия АНАКЕМ [32]
- 2014 г., заслуженный профессор, Университет Индианы в Блумингтоне [5]
- 2014 г., выдающийся выпускник факультета химии, Университет Юты [9]
- 2012, Премия Американского химического общества (ACS) за достижения в области химического приборостроения [33]
- 2011, член Американской ассоциации содействия развитию науки (AAAS) [34]
- 2011–2012 гг. — член Японского общества содействия науке (JSPS)
- 2010, выдающийся выпускник университета Адамса [4]
- 2009, Премия Трейси М. Зоннеборн, Университет Индианы в Блумингтоне [11]
- 2007, премия Американского химического общества (ACS) в Акроне [35]
- 2006, Медаль Бимана, Американское общество масс-спектрометрии [3]
- 2005 г. — действительный член Королевского химического общества.
- 2003–2005, Специальная творческая премия Национального научного фонда
- 2002, Премия Питткона за достижения [36]
- 2002, назван одним из 10 самых выдающихся людей по версии журнала Popular Science [10]
- 2002 г. — назначен заведующим кафедрой химии имени Роберта и Марджори Манн в Университете Индианы в Блумингтоне [5]
- 2000–2002, премия Eli Lilly по аналитической химии
- 1998–2001, научный сотрудник, Alfred P. Sloan Research [37]
- 2000, Национальная премия Фрезениуса, Phi Lambda Upsilon [38]
- 1999–2000, Американское химическое общество (ACS), Отделение аналитической химии, Премия Артура Ф. Финдейса
- 1999, Премия имени Камиля Дрейфуса для преподавателей и ученых, Фонд Камиля и Генри Дрейфуса [39]
- 1999, «Новаторы до 35», MIT Technology Review [25]
- 1996–2000, Премия Национального научного фонда за раннюю карьеру
Ссылки
- ^ ab "Группа Клеммера, профессор Дэвид Э. Клеммер" . Университет Индианы в Блумингтоне . Проверено 26 апреля 2017 г. .
- ^ abcdefg "Профессор Дэвид Клеммер, Университет Индианы". Уотерс Наука о том, что возможно . Архивировано из оригинала 23 июня 2013 года . Получено 26 апреля 2017 года .
- ^ abcdefghij Бирбаум, Вероника М.; Фред В. Маклафферти (2007). «Фокус в честь Дэвида Э. Клеммера, лауреата медали Биемана 2006 года». Журнал Американского общества масс-спектрометрии . 18 (7): 1161–1162. Bibcode : 2007JASMS..18.1161B. doi : 10.1016/j.jasms.2007.05.004. PMID 17555983. S2CID 10308685.
- ^ abcde Relyea, Linda (26 августа 2010 г.). «Clemmer makes science an art form». Adams State University . Архивировано из оригинала 7 сентября 2015 г. Получено 28 апреля 2017 г.
- ^ abcdefgh "University Honors & Awards: Honoree David E. Clemmer". Indiana University Bloomington . Архивировано из оригинала 27 апреля 2015 года . Получено 28 апреля 2017 года .
- ^ Хонма, Кенджи; Клеммер, Дэвид Э. (1995). «Важность механизма переноса электронов в реакциях нейтральных атомов переходных металлов». Лазерная химия . 15 (2–4): 209–220. doi : 10.1155/1995/25319 .
- ^ Клеммер, Дэвид Э.; Джарролд, Мартин Ф. (июнь 1997 г.). «Измерения подвижности ионов и их применение к кластерам и биомолекулам». Журнал масс-спектрометрии . 32 (6): 577–592. Bibcode :1997JMSp...32..577C. doi :10.1002/(SICI)1096-9888(199706)32:6<577::AID-JMS530>3.0.CO;2-4. S2CID 16681465.
- ^ Clemmer, David E.; Hudgins, Robert R.; Jarrold, Martin F. (октябрь 1995 г.). "Naked Protein Conformations: Cytochrome c in the Gas Phase" (PDF) . Journal of the American Chemical Society . 117 (40): 10141–10142. doi :10.1021/ja00145a037. Архивировано из оригинального (PDF) 21 апреля 2016 г. . Получено 1 мая 2017 г. .
- ^ ab "Премии выдающимся выпускникам факультета химии 2014 года". Университет Юты . Получено 1 мая 2017 г.
- ^ ab Hinnefeld, Steve (2002). "Ученый из 10 лучших ученых университета Айова" (PDF) . Hoosier Times . Архивировано из оригинала (PDF) 1 мая 2016 года . Получено 2 мая 2017 года .
- ^ abc Connelley-Eskine, Cyndi (20 апреля 2009 г.). "Объявлен лауреат премии Tracy M. Sonneborn Award и профессор Provost's". IU News Room . Получено 28 апреля 2017 г. .
- ^ Эйсман, Джорджия; Карпас, З.; Хилл-младший, HH (2014). Спектрометрия ионной подвижности (Третье изд.). Бока-Ратон, Флорида: CRC. стр. 30–31. ISBN 9781439859971.
- ^ abc Маклин, Джон А. (октябрь 2009 г.). «Корреляция массы и подвижности: конформационный ландшафт безводных биомолекул». Журнал Американского общества масс-спектрометрии . 20 (10): 1775–1781. Bibcode :2009JASMS..20.1775M. doi :10.1016/j.jasms.2009.06.016. PMID 19646898. S2CID 205703562.
- ^ Шелимов, КБ; Клеммер, Д.Е.; Хадгинс, Р.Р.; Джарролд, М.Ф. (1997). «Структура белка в вакууме: конформации газовой фазы BPTI и цитохрома c». J. Am. Chem. Soc . 119 (9): 2240–2248. doi :10.1021/ja9619059. S2CID 9163743.
- ^ Ибрагим, Йехия М.; Бейкер, Эрин С.; Дэниелсон, Уильям Ф.; Норхейм, Рэндольф В.; Прайор, Дэвид К.; Андерсон, Гордон А.; Белов, Михаил Э.; Смит, Ричард Д. (февраль 2015 г.). «Разработка нового времяпролетного масс-спектрометра для измерения подвижности ионов». Международный журнал масс-спектрометрии . 377 : 655–662. Bibcode :2015IJMSp.377..655I. doi :10.1016/j.ijms.2014.07.034. PMC 4501404 . PMID 26185483.
- ^ "Разработка новой аппаратуры для измерения подвижности ионов группой Clemmer". Университет Индианы . Получено 2 мая 2017 г.
- ^ Hoaglund, Cherokee S.; Valentine, Stephen J.; Sporleder, C. Ray; Reilly, James P.; Clemmer, David E. (1998). "Трехмерная ионная подвижность/TOFMS анализ электрораспыленных биомолекул" (PDF) . Anal. Chem . 70 (11): 2236–2242. doi :10.1021/ac980059c. PMID 9624897. Архивировано из оригинала (PDF) 10 августа 2017 г. . Получено 1 мая 2017 г. .
- ^ Хендерсон, Шейла К.; Валентайн, Стивен Дж.; Каунтерман, Энн Э.; Клеммер, Дэвид Э. (1999). "ESI/Ионная ловушка/Ионная подвижность/Времяпролетная масс-спектрометрия для быстрого и чувствительного анализа биомолекулярных смесей" (PDF) . Anal. Chem . 71 (2): 291–301. doi :10.1021/ac9809175. PMID 9949724. Архивировано из оригинала (PDF) 10 августа 2017 г. . Получено 1 мая 2017 г. .
- ^ Myung, Sunnie; Lee, Young Jin; Moon, Myeong Hee; Taraszka, John; Sowell, Rena; Koeniger, Stormy; Hilderbrand, Amy E.; Valentine, Stephen J.; Cherbas, Lucy; Cherbas, Peter; Kaufmann, Thomas C.; Miller, David F.; Mechref, Yehia; Novotny, Milos V.; Ewing, Michael A.; Sporleder, C. Ray; Clemmer, David E. (октябрь 2003 г.). «Разработка высокочувствительных методов спектрометрии ионной подвижности с использованием ионной ловушки и времени пролета: высокопроизводительное разделение пептидов, полученных из белкового экстракта с помощью нано-ЖХ-ИМС-TOF». Аналитическая химия . 75 (19): 5137–5145. doi :10.1021/ac030107f. PMID 14708788 . Получено 1 мая 2017 г. .
- ^ Ланукара, Франческо; Холман, Стивен В.; Грей, Кристофер Дж.; Айерс, Клэр Э. (21 марта 2014 г.). «Мощь ионной подвижности-масс-спектрометрии для структурной характеристики и изучения конформационной динамики». Nature Chemistry . 6 (4): 281–294. Bibcode :2014NatCh...6..281L. doi :10.1038/nchem.1889. PMID 24651194. S2CID 2512242.
- ^ Гросс, Майкл Л.; Чен, Годонг; Праманик, Бирендра Н. (2012). Масс-спектрометрия белков и пептидов в разработке лекарств. Хобокен, Нью-Джерси: Wiley. С. 202–203. ISBN 978-0-470-25817-0.
- ^ Hoaglund-Hyzer, Cherokee S.; Counterman, Anne E.; Clemmer, David E. (1999). "Безводные ионы белка" (PDF) . Chem. Rev . 99 (10): 3037–3079. doi :10.1021/cr980139g. PMID 11749510. Архивировано из оригинального (PDF) 9 февраля 2018 г. . Получено 1 мая 2017 г. .
- ^ Шварцбург, Александр А. (2008). Дифференциальная спектрометрия подвижности ионов: нелинейный транспорт ионов и основы FAIMS . Бока-Ратон, Флорида: CRC Press. С. 25–26.
- ^ "Январское собрание общества спектроскопии Питтсбурга, 2013 г.". Общество спектроскопии Питтсбурга . Архивировано из оригинала 4 июля 2020 г. Получено 2 мая 2017 г.
- ^ ab "David Clemmer, 34 Indiana University". Innovators Under 35: 1999. MIT Technology Review. Архивировано из оригинала 15 марта 2016 года . Получено 28 апреля 2017 года .
- ^ "Профессор Дэвид Клеммер награжден премией Филда и Франклина 2023 года за выдающиеся достижения в области масс-спектрометрии: химический факультет". www.chem.indiana.edu . Получено 30 сентября 2022 г.
- ^ ab "Дэвид Э. Клеммер: Почести и награды университета: Университет Индианы". Почести и награды университета . Получено 30 сентября 2022 г.
- ^ "MFJ Research Group". Архивировано из оригинала 2008-05-26 . Получено 2018-07-16 .
- ^ «Группа Герта фон Хельдена».
- ^ «Выдающийся вклад Джона Б. Фенна в ASMS».
- ^ "Страница стипендиатов Национальной академии изобретателей". Архивировано из оригинала 2013-01-28 . Получено 2017-12-13 .
- ^ "Награды АНАХЕМ".
- ^ "DAC Award in Chemical Instrumentation". Американское химическое общество (ACS) . Отдел аналитической химии ACS. Архивировано из оригинала 24 апреля 2017 г. Получено 26 апреля 2017 г.
- ^ "Рекордные 10 преподавателей получили звание члена AAAS, крупнейшего в мире научного общества". Inside IU . 1 декабря 2011 г. Архивировано из оригинала 2017-06-04 . Получено 2017-05-02 .
- ^ "Akron Section Award". Архивировано из оригинала 2013-08-02 . Получено 2017-11-27 .
- ^ "Питткон 2002".
- ^ «Исследовательские стипендии Слоуна».
- ^ "Национальная премия Фрезениуса". Северо-Западный университет . Получено 1 мая 2017 г.
- ^ "Программа награждения преподавателей и ученых имени Камиллы Дрейфус" (PDF) . Фонд Камиллы Дрейфус . Получено 28 апреля 2017 г. .
Внешние ссылки
- http://www.indiana.edu/~clemmer/home.htm Архивировано 08.01.2012 на Wayback Machine
- Публикации Дэвида Э. Клеммера, проиндексированные Google Scholar