Спиролигомер

Молекулы спиролигомеров (также известные как бис-пептиды ) представляют собой синтетические олигомеры , полученные путем соединения пар бис-аминокислот в конденсированную кольцевую систему. [1] Молекулы спиролигомеров обладают богатой стереохимией и функциональностью из-за разнообразия бис-аминокислот, которые могут быть включены в процессе синтеза. [2] Благодаря жесткости конденсированной кольцевой системы [3] трехмерная форма молекулы спиролигомера, а также отображение любых функциональных групп, могут быть предсказаны, что позволяет проводить молекулярное моделирование и динамику.
Синтез

Молекулы спиролигомера синтезируются поэтапно путем добавления одной бис-аминокислоты на каждом этапе синтеза. Это поэтапное удлинение позволяет полностью контролировать стереохимию, поскольку любая бис-аминокислота может быть включена для удлинения; или любая моно-аминокислота может быть добавлена для завершения цепи. Это может быть достигнуто с помощью реакций в растворе или твердофазных реакций. [4] Первоначальный синтез молекулы спиролигомера допускал функционализацию на концах олигомеров, но не допускал включения функциональности на внутренних дикетопиперазиновом (DKP) азоте. [5] Была проделана большая работа, чтобы обеспечить функционализацию всей молекулы спиролигомера, а не только концов. [2] Используя эффект соседней группы, [6] молекула спиролигомера может быть синтезирована с различными функциональными группами по длине молекулы.
Структура
Молекулы спиролигомеров могут быть синтезированы в любом направлении и между любой парой бис-аминокислот. Спиролигомерные дикетопиперазины могут быть созданы между любым концом бис-аминокислоты. Известно, что молекулы спиролигомеров являются конформационно жесткими из-за конденсированного кольцевого остова. [3]

Химические характеристики
Молекулы спиролигомеров являются пептидомиметиками , полностью устойчивыми к протеазам и вряд ли вызывающими иммунный ответ.
Использует
Молекулы спиролигомеров использовались в различных областях, включая катализ, связывание белков, связывание металлов, молекулярные каркасы, исследования переноса заряда и др.
Катализ
Разработаны два уникальных типа катализаторов спиролигомеров (спиролигозимов): имитатор эстеразы и катализатор Кляйзена.
Переэтерификация
Первый катализатор спиролигомера был имитатором эстеразы , который катализировал перенос трифторацетатной группы. [7]

Ароматическая перегруппировка Клайзена
Второй катализатор спиролигомер ускорил ароматическую перегруппировку Кляйзена с каталитической диадой, аналогичной той, что обнаружена в кетостероидизомеразе. [8]

Связывание с белками
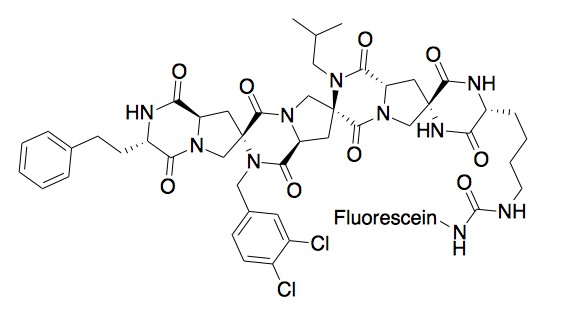
Пептидомиметик Spiroligomer был разработан для имитации P53 и связывания HDM2. Молекула проникает в клетки посредством пассивной диффузии, и было показано, что этот имитатор стабилизирует HDM2 в клеточной культуре. [9]
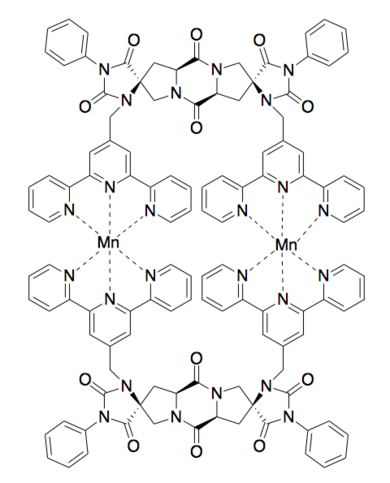
Металлический переплет
Биядерная связь металлов [10]
Молекулярные каркасы
Стержни, используемые для измерения расстояния с помощью спиновых зондов . [3]
Передача электронов
Донор-Мост-Акцептор [11]
Другие применения
Возможные приложения, которые в настоящее время исследуются, включают связывание и инактивацию холерного токсина и перекрестное связывание поверхностных белков различных вирусов ( ВИЧ , вирус Эбола ). Далее группа Кристиана Шафмайстера разработала молекулярные шарниры, которые могут быть использованы для создания молекулярных машин , таких как наноклапаны или системы хранения данных . [12]
Смотрите также
Ссылки
- ^ Кристиан Э. Шафмейстер, Захари З. Браун и Шарад Гупта «Программируемые формой макромолекулы» Отчеты о химических исследованиях , (2008), 41(10), 1387-1398 doi :10.1021/ar700283y
- ^ ab Захари З. Браун и Кристиан Э. Шафмейстер, "Синтез гекса- и пентазамещенных дикетопиперазинов из стерически затрудненных аминокислот" Organic Letters , (2010), 12(7), 1436-1439 doi :10.1021/ol100048g
- ^ abc Грегори Х. Берд, Сорая Порнсуван, Сунил Саксена и Кристиан Э. Шафмейстер, «Распределение расстояний изогнутых биспептидных олигомеров с концевой меткой с помощью электронного спинового резонанса» ACSNano (2008), 2(9), 1857-1864 doi :10.1021/nn800327g
- ^ Захари З. Браун, Дженнифер Аллева и Кристиан Э. Шафмейстер, «Твердофазный синтез функционализированных бис-пептидов» Биополимеры , (2011), 96(5), 578-585 doi :10.1002/bip.21591
- ^ Кристофер Г. Левинс и Кристиан Э. Шафмейстер, «Синтез функционализированных наноразмерных молекулярных стержней определенной длины», Журнал Американского химического общества , (2003), 125(16), 4702-4703 doi :10.1021/ja0293958
- ^ Захари З. Браун и Кристиан Э. Шафмейстер, «Использование эффекта внутренней соседней группы альфа-аминокислот для синтеза чрезвычайно затрудненных дипептидов», Журнал Американского химического общества , (2008), 130(44), 14382-14383 doi :10.1021/ja806063k
- ^ Махбубе Хейрабади и Кристиан Шафмейстер и др., «Спиролигозимы для переэтерификации: дизайн и связь структуры с активностью», Журнал Американского химического общества , (2012), 134, 18345-18353 doi :10.1021/ja3069648
- ^ Мэтью Ф. Л. Паркер и Кристиан Э. Шафмеситер и др., «Ускорение ароматической перегруппировки Кляйзена с помощью разработанного спиролигозимного катализатора, имитирующего каталитическую диаду кетостероидной изомеразы», Журнал Американского химического общества , (2014), 136(10), 3817-3827 doi :10.1021/ja409214c
- ^ Захари З. Браун, Кавита Акула и Кристиан Шафмейстер и др., «Имитатор альфа-спирали спиролигомера, который связывает HDM2, проникает в клетки человека и стабилизирует HDM2 в клеточной культуре» PLOSOne (2012), 7(10), doi :10.1371/journal.pone.0045948
- ^ Шивайя Ваддипалли, Чонсонг Сюй, Сэньчжи Чжао, Яньфэн Фань, Кристиан Э. Шафмейстер и Майкл Дж. Здилла «Архитектурные спиролигомеры, разработанные для шаблонизации биядерных металлических комплексов» Неорганическая химия , (2013), 52, 6457-6463 doi :10.1021/ic4003498
- ^ Субхасис Чакрабарти, Мэтью Ф. Л. Паркер, Кристофер В. Морган, Кристиан Э. Шафмейстер и Дэвид Х. Вальдек, «Экспериментальные доказательства опосредованного водой переноса электронов через бис-аминокислотные донорно-мостиковые-акцепторные олигомеры», Журнал Американского химического общества , (2009), 131(6), 2044-2045 doi :10.1021/ja8079324
- ^ Левинс К. Г., Шафмейстер К. Э. Синтез изогнутых и линейных структур из минимального набора мономеров. Журнал органической химии, 70 , стр. 9002, 2005. doi :10.1002/chin.200605222